Intensive Care Medicine
POINTS ESSENTIELS
- L’anesthésie en urgence pré hospitalière (AUPH) est une intervention à haut risque qui peut avoir un impact positif significatif sur le devenir du patient.
- Une sélection soigneuse du patient est d’une importance primordiale. Les indications majeures incluent les patients avec des voies respiratoires altérées, une défaillance ventilatoire, ceux nécessitant une neuro protection spécifique et ceux des patients dont l’évolution clinique antérieure suggère le besoin d’une induction anesthésique en urgence soit avant le transport à l’hôpital soit peu de temps après l’arrivée à l’hôpital.
- Les conditions climatiques, la disponibilité du matériel, la position du patient, la configuration des lieux, et les compétences de l’équipe peuvent tous contribuer à augmenter les difficultés d’une délivrance de l’anesthésie en sécurité dans le contexte pré hospitalier.
- Le choix des médicaments pour l’induction et la maintenance doivent être adaptés à l’état hémodynamique et aux conditions sous-jacentes de chaque patient.
- L’utilisation d’une immobilisation du rachis cervical, d’une pression du cricoïde, et de l’utilisation de la kétamine comme agent d’induction font l’objet de controverses. Toutefois une évolution de la pratique basée sur l’évidence aide dans ces domaines.
INTRODUCTION
L’anesthésie en urgence pré hospitalière (AUPH) correspond à l’induction de l’anesthésie et à la sécurisation des voies aériennes en environnement pré hospitalier. C’est une forme modifiée de l’induction en séquence rapide (ISR) et de l’intubation. L’AUPH comporte de hauts risques dus à la fois aux patients et à l’environnement. De nombreux facteurs doivent être pris en compte pour diminuer les risques. L’anesthésie pré hospitalière a été décrite comme une « intervention souhaitable chez un nombre relativement limité de patients car elle peut être la cause d’une morbidité et d’une mortalité inutile si elle est mal faite. »1.Le rapport de l’Enquête Nationale Confidentielle de 2007 sur le Devenir et la Mort des Patients (NCEPOD) « Traumatisme : qui soigne ? » s’est intéressé aux domaines qui peuvent contribuer à prévenir la mort dans les traumatismes majeurs. Ce rapport met en évidence qu’une préservation inadaptée des voies aériennes fut réalisée dans 42 sur 438 cas et que 72,9% de ceux ayant un traumatisme crânien sévère et un score de Glasgow (GCS) inférieur à 9 n’ont pas subi de AUPH.2
POURQUOI ? POUR QUI ?
Les risques associés à la réalisation d’une AUPH doivent être mis en balance avec les bénéfices escomptés sur la base d’un patient individuel. Il y a des différences régionales et internationales dans la pratique concernant les interventions pré hospitalières. Les deux extrêmes de ces différences ont été rapportées comme étant le « stay and play », visant à stabiliser le patient sur place, versus un transfert rapide, le « scoop and run ». Il y a peu d’évidence qu’un système ait des avantages sur l’autre.2 De nombreux facteurs doivent être pris en compte pour chaque cas dans lesquels l’AUPH est envisagée. Ces facteurs incluent des considérations géographiques, les modes de transport et la compétence de l’équipe qui intervient, ainsi que la répartition des blessures ou des maladies. Ces facteurs sont des déterminants importants dans la sélection des patients chez lesquels les bénéfices de l’AUPH l’emportent sur les risques.
Facteurs liés au patient à prendre en compte dans la sélection des patients.
- Le besoin d’une protection des voies aériennes chez des patients les ayant ou susceptibles de les avoir compromises
- La nécessité d’une aide ventilatoire. Une défaillance ventilatoire peut parfois être mieux effectivement améliorée par l’intubation et l’institution d’une ventilation mécanique ;
- La nécessité d’une neuroprotection afin de prévenir une lésion cérébrale secondaire.
- Une évolution clinique possible (c’est-à-dire un patient ayant un score de Glasgow diminué qui est agité et dont on pense qu’il nécessitera une anesthésie lors de son admission à l’hôpital pour faciliter la réalisation d’une imagerie ou d’un traitement. L’enquête NCEPOD rapportait dans le document « Trauma : qui soigne ? » que 31,7% des patients gravement traumatisés avec un score de gravité – 16, nécessitaient une intubation dans les 30 minutes suivant leur arrivée.1 Il en était conclu que cela conduisait à une pire évolution clinique. Donc, dans les cas où une aggravation de l’évolution clinique est suspectée au point qu’une anesthésie soit habituellement requise immédiatement lors de l’arrivée aux soins secondaires, alors une AUPH serait effectuée ordinairement sur place.
- Pour des raisons humanitaires (c’est-à-dire en présence de blessures sévères telles que des fractures nécessitant une immobilisation ou des brûlures graves)
- Le mode de transport, l’équipe de transport, et la durée nécessaire pour transférer le patient aux soins définitifs devraient également être considérés lorsque l’on évalue les bénéfices de l’AUPH. Dans des environnements de courte durée de transfert (tels que les environnements urbains britanniques), le bénéfice d’un transfert rapide à l’hôpital peut être un atout par rapport aux interventions pré hospitalières.3 La position du patient et des différents membres de l’équipe à l’intérieur du véhicule de transport devraient aussi être envisagée car l’accès au patient est souvent réduit au cours du transport. Par exemple, une blessure thoracique qui peut nécessiter une thoracostomie en route doit être soigneusement appréciée si le côté blessé est situé au contact immédiat de la paroi de l’ambulance ou de l’avion et donc ne pas être immédiatement accessible.
L’AUGMENTATION DES RISQUES ET LEUR ATTENUATION
Les risques de pratiquer une AUPH peuvent être répartis en facteurs liés à l’environnement, liés à l’opérateur et aux facteurs humains, ainsi qu’aux facteurs dus au patient. Ces facteurs sont souvent entremêlés.
Les facteurs liés à l’environnement
Une diversité de facteurs liés à l’environnement influence les risques d’AUPH.
1. Conditions environnementales. En comparaison avec les conditions de travail dans un environnement habituellement contrôlé de chaleur et de luminosité, la tentative d’AUPH comporte des facteurs de stress supplémentaires. Des bruits parasites, un excès ou un manque de lumière, le vent, la pluie, des gens du public, des mouvements du véhicule, un terrain en pente, des fuites de carburant, etc… peuvent ajouter à la difficulté ressentie par l’opérateur. Il peut en résulter une diminution de l’aptitude technique à effectuer la tâche et une perte de la perception de la situation, dont une capacité réduite à reconnaître la survenue d’erreurs.
Les conditions d’environnement auront aussi un impact sur la température du patient du fait de l’exposition aux éléments et à l’immobilité engendrée par la blessure ou la maladie ou une situation physiquement piégée. Toute réduction de la température centrale sera augmentée à la suite de l’anesthésie. Une diminution de la température centrale contribuera à une coagulopathie et un mauvais pronostic du traumatisme.4 Des mesures pour maintenir activement la température corporelle en réduisant les pertes de chaleur, mettant en oeuvre un réchauffement actif, et en réduisant la durée du maintien sur site sont impératives dans cette population. Le choix d’un lieu peut parfois atténuer certains de ces problèmes.
Des modifications de la lumière naturelle peuvent parfois aussi être source de problèmes. Un soleil brillant peut amener une constriction de la pupille de l’opérateur, réduisant de ce fait la visualisation des cordes vocales dans l’obscurité relative de l’oropharynx. Le positionnement du patient en lui détournant la tête de la direction de la lumière du soleil et des modifications adaptées de l’environnement peuvent créer de l’ombre.
2. L’accès au patient. Les patients qui requièrent une intubation dans un contexte pré hospitalier sont rarement trouvés dans une situation adéquate. Les exemples incluent des caves, de petits lits, l’intérieur de véhicules, des rives escarpées, des flancs de colline rocheux et d’étroits passages. Plusieurs risques sont inhérents à une tentative d’intubation dans des lieux avec accès restreint au patient. Si possible, le patient sera placé dans une situation où « l’accès à 360° » peut être obtenu avant de tenter l’AUPH. Pour rendre la tentative d’intubation la plus normale possible et de ce fait réduire le risque d’échec de l’intubation, le patient est placé à une hauteur à laquelle l’opérateur peut s’agenouiller ou se tenir debout. Cela peut être sur un chariot ou un brancard, qui peuvent être adaptés à la hauteur appropriée.
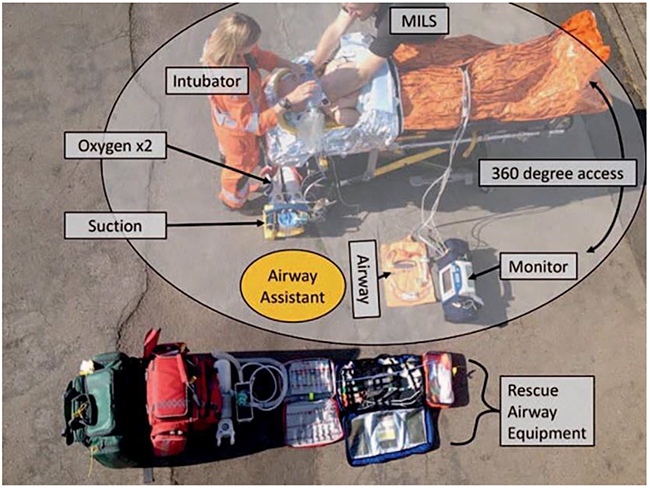
Figure 1. Dépot des équipements avec leur position et celle du personnel soulignée par les rectangles (en anglais). La position du responsible des voies aériennes montrée par l’ovale jaune. La stabilisation manuelle en ligne devrait être utilisée si une atteinte de la colonne cervicale est suspectée pour prévenir les mouvements excessifs durant l’intubation.
3. Disponibilité du kit. Dans un environnement de local hospitalier organisé, matériel et médicaments sont aisément disponibles et rapidement accessibles. En pré hospitalier, tous les équipements nécessaires doivent être transportés sur le site. La standardisation de kits en sacs et de fréquents exercices d’entraînement pour familiariser les membres de l’équipe avec le contenu et la disposition de l’ouverture du kit sont essentiels; cela permettra à tout membre de l’équipe pré hospitalière de savoir s’en servir. Le kit devrait contenir les appareils de ventilation et compléments, guides d’intubation, aspiration, oxygène, systèmes de respiration et de ventilation, monitorage, et médicaments (soit pré préparés ou contenus dans des seringues étiquetées : voir table 2). Un tracé capnographique gradué est préconisé au Royaume Uni et devrait être considéré comme obligatoire avant d’entreprendre une AUPH. Dans une étude de Li et coll.5, 3% des intubations en urgence se traduisent par une intubation oesophagienne. Dans une étude américaine, l’utilisation du tracé du CO2 de fin d’expiration réduisait le taux de mise en place erronée de sondes d’intubation de 9% à 0%6. Les autres facteurs qui permettent d’aider à détecter une intubation oesophagienne sont l’utilisation de la vidéo laryngoscopie (qui permet la visualisation du passage de la sonde entre les cordes vocales), l’auscultation de la poitrine avec un stéthoscope, et l’habitude avec « comment le sentir » lorsque l’on ventile à la main un patient avec une sonde endotrachéale correctement placée .
Facteurs humains liés à l’opérateur
- Confort et sécurité. Comme discuté ci-dessus, le confort et la sécurité de l’intubateur et du reste de l’équipe sont importants pour réduire le risque. Un équipement protecteur personnel, incluant un habillement adapté au temps et à la température est important, autant que la situation et le positionnement du patient.
- Aptitude de l’équipe. L’anesthésie pré hospitalière est une intervention à haut risque qui ne devrait pas être tentée par ceux qui ont un entraînement ou une expérience insuffisants. Il est primordial qu’il y ait un programme d’entraînement rigoureux, que les aptitudes soient entretenues, et qu’il y ait des révisions régulières de pratique.1 Tous ceux impliqués dans l’AUPH devraient travailler à mettre au point des protocoles (Procédures opérationnelles standard, POS) qui seraient bien intégrés, de telle sorte que la totalité de l’équipe sache qu’à la fois son rôle et le protocole standardisé sont faits à l’intérieur de leur organisation.
- Surcharge cognitive. L’intervention pré hospitalière comporte bien souvent de nombreux sauveteurs en scène, incluant des professionnels de santé, d’autres professionnels de l’urgence, et le public. Fréquemment, il existe une activité concurrentielle, et il a parfois plus qu’une seule victime. La diminution d’erreurs est obtenue par l’utilisation d’une check-list verbale par question-réponse. Les protocoles et check-list d’équipement, simplifient les processus et limitent le choix pour réduire les charges cognitives ultérieures.8 La charge cognitive est réduite en confirmant la disponibilité de l’équipement, des médicaments (incluant le calcul des doses), et les plans d’action d’urgence en cas d’échec de l’intubation et d’autre problèmes éventuels.1 L’utilisation de check-lists peut aussi assurer que ceux qui effectuent l’AUPH restent focalisés de façon convenable sur leur tâche. Un exemple de check-list est fourni dans le tableau 1.
Facteurs liés au patient
Les patients qui subissent une AUPH n’ont pas eu d’évaluation pré opératoire standard. Au contraire des patients opérés en chirurgie programmée ils ne pourront pas être optimisés pour l’anesthésie, et une information sur l’examen préalable de l’accès aux voies aériennes ne sera pas disponible. Ils constituent un groupe à haut risque, avec fréquemment un problème physiologique significatif, tel qu’une hypovolémie, une hypoxie, une hypothermie, et une acidose métabolique. L’atténuation de ces facteurs peut être extrêmement difficile et n’est pas toujours réalisable.
1. Hypovolémie. L’induction d’une anesthésie chez des patients hypovolémiques est hasardeuse. L’AUPH chez des patients traumatisés dont l’hypovolémie est insuffisamment corrigée est associée à une augmentation de la mortalité. Ces patients devraient idéalement bénéficier d’une réanimation avec des produits sanguins appropriés avant l’induction de l’anesthésie. Une étude contrôlée des dommages de la réanimation souligne l’importance d’une réanimation appropriée avec des produits sanguins appropriés pour diminuer les effets délétères d’un saignement majeur, incluant acidémie et coagulopathie, par rapport au groupe témoin.9Avant de réaliser un contrôle définitif de l’hémorragie, des valeurs physiologiques adéquates à atteindre incluent une pression artérielle moyenne de 50mmHg, une pression systolique de plus de 80mmHg, ou le retour d’un pouls périphérique palpable.10 L’acidose, suivie par l’estimation d’un objectif de l’excès de base, peut être corrigée par une bonne réanimation.
Les agents anesthésiques peuvent de plus aggraver le profil hémodynamique du patient via une vasodilatation induite par l’agent, une dépression myocardique, et la perte d’une compensation sympathique. En outre, la ventilation en pression positive dans ce contexte pourra réduire la pré charge.
Un accès veineux adapté est vital. On considère comme idéal de disposer de deux sites d’accès veineux sûrs et de bon calibre et une perfusion de quelque type branchée pour toutes les inductions anesthésiques. Cela permettra à la fois l’administration rapide d’un bolus de 250 ml de liquide si nécessaire et de rincer facilement les médicaments qui ont été administrés. La nécessité de doses adaptées d’agents d’induction serait à considérer. Comme discuté plus loin, les vasopresseurs seraient à éviter en cas d’hypovolémie si possible.
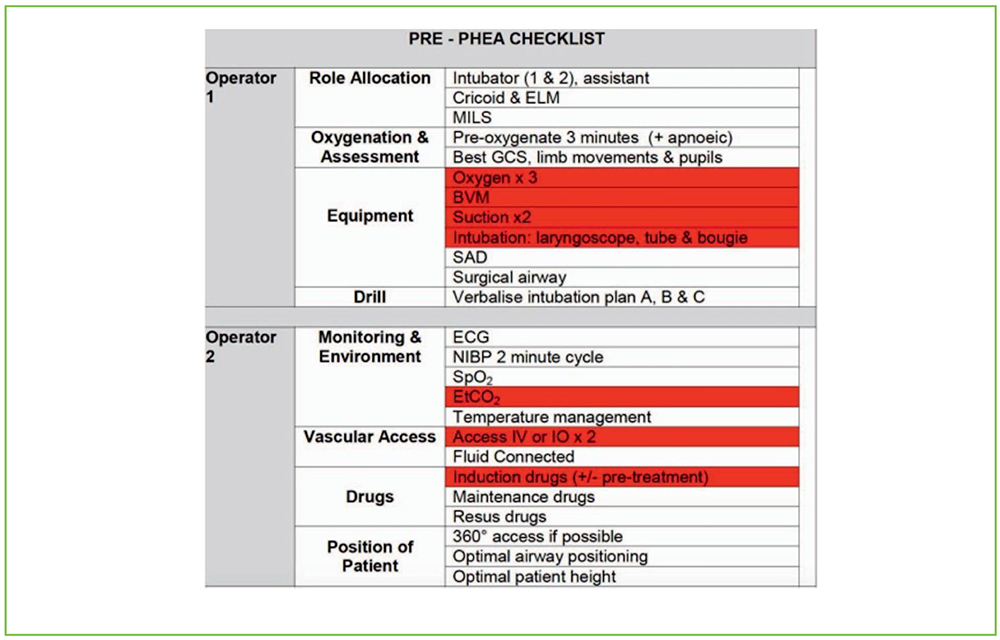
Tableau 1. Exemple de liste de verification AUPH avec les éléments de base pour “induction immediate” surlignés en rouge. ELM: manipulation laryngée externe. MILS: stabilization manuelle en ligne, SAD: dispositif supra glottique. Tiré de: South Western Ambulance Service NHS Foundation Trust, Trust Clinical Guideline ID CCG02, ‘‘Pre-hospital Emergency Anaesthesia (PHEA),’’ issued September 1, 2015

Tableau 2. Doses d’agents anesthésiques ajustées pour la condition du patient (Adapté de Ref. 14)
2. Hypoxie. Des efforts doivent être faits pour optimiser l’efficacité de la pré oxygénation. Une pré oxygénation efficace dans l’environnement pré hospitalier peut être difficile mais elle est au mieux réalisé en combinant un haut flux d’oxygène par voie nasale à un circuit de Waters. Le premier peut être poursuivi pendant la phase d’apnée et peut accroître la période d’apnée jusqu’à dix minutes.11 Pour ceux chez qui une pré oxygénation est difficile en raison de l’agitation, une sédation adaptée peut être utilisée pour rendre effective la pré oxygénation avant d’entreprendre l’AUPH. La Kétamine à 0,5 à 1mg/kg intraveineuse (ou 4-5 mg/kg par voie intra musculaire) est la plus communément utilisée dans ce but. Alors que le midazolam peut aussi être efficace, il est utilisé moins habituellement dans ce cas parce qu’il implique une réduction de l’ouverture des voies aériennes.
Bien que, classiquement, une séquence d’induction rapide n’incluerait pas une ventilation manuelle, chez le patient en état critique, la ventilation assistée est communément utilisée pendant et après l’induction de l’anesthésie. Le risque d’insufflation gastrique et d’inhalation qui en résulte peut-être réduit en maintenant la pression inspiratoire en dessous de 25 cmH2O.12
3. Hypothermie. Les patients doivent être gardés au chaud avec une protection appropriée par rapport au temps. Dans bien des cas, un réchauffement actif afin de maintenir la température est aussi nécessaire.
4. Voies aériennes. Tous les accès aux voies aériennes seront présumés difficiles en pré hospitalier. Beaucoup d’équipes de réanimation en Grande Bretagne utilisent en routine un vidéo laryngoscope et un mandrin pour toutes les intubations. Cela réduit non seulement la formation de l’équipe pour avoir une approche standardisée mais diminue d’un tiers la difficulté du processus si l’intubation est difficile, en permettant une progression rapide dans un algorithme d’intubation difficile.
Pour les traumatisés ayant une suspicion de lésion du rachis cervical, un dispositif utilisé pour l’immobilisation, tel que des colliers cervicaux et des blocages, diminueront significativement le degré de réalisation optimale de la laryngoscopie et pourraient être remplacés par une stabilisation manuelle dans l’alignement avant l’induction de l’anesthésie.2
AGENTS D’INDUCTION
Le but serait de délivrer toujours une anesthésie sûre et équilibrée, adaptée au patient et à l’expérience de l’opérateur. De nombreuses formules différentes ont été proposées pour offrir l’association optimale des doses de médicaments.13-15 Certaines sont discutées ci-dessous. Il est largement admis que le bloc neuromusculaire puisse être utilisé. Une large étude d’intubations faites par des paramédicaux montrait un taux de succès global de 67,5% qui était augmenté à 81% en utilisant un sédatif et à 96,7% en utilisant un bloc neuromusculaire.1 Un bloc neuromusculaire adapté a aussi été démontré augmenter significativement la probabilité de succès de procédures sur la trachée en cas de situations où il est impossible d’intuber et d’oxygéner.1 Cela est particulièrement important car il serait très rare pour un patient de tolérer d’être réveillé dans ce scénario où l’AUPH était indiquée.
Formule « 3, 2, 1 »
La formule 3,2,1 référant aux doses de fentanyl, kétamine, et rocuronium, respectivement, a été suggérée comme base de l’anesthésie pré hospitalière dans les traumatismes.12 Cela pourrait être adapté ultérieurement pour s’adapter à différentes situations. Une formule 1 :1 :1 a été suggérée pour des patients instables du point de vue cardiovasculaire. La suppression du fentanyl pour des patients très instables a également été proposée, en ne gardant que l’administration de rocuronium chez un patient comateux en péri arrêt (tableau 2).
Une formule de fentanyl, kétamine, et rocuronium a été démontrée produire les meilleures conditions d’intubation avec une stabilité hémodynamique améliorée comparée à l’étomidate et au suxaméthonium.16 De plus, il y a des preuves pour penser qu’un blocage surrénalien peut survenir même après une dose unique d’étomidate.16 Dans un essai entre étomidate versus kétamine, 232 patients randomisés ont une insuffisance surrénalienne démontrée. L’insuffisance surrénalienne fut plus fréquente dans le groupe étomidate avec un odds ratio de 6,7 (95% d’intervalle de confiance 3,5-12,7).17
Des craintes sont apparues concernant la longue durée d’action du rocuronium comparée avec le suxaméthonium utilisé dans une classique séquence d’intubation rapide. Cependant, chez les patients les plus sévèrement traumatisés, le réveil des patients si une tentative d’intubation échoue n’est pas une option sûre ni viable. Aussi, un accès difficile aux voies aériennes est connu comme étant davantage un problème chez un patient partiellement endormi chez lequel le suxaméthonium a été utilisé.12
La kétamine possède une large marge d’erreur et maintien un certain tonus sympathique. Cela en fait un agent très utile dans un traumatisme, mais la prudence est de mise chez le sujet âgé car en cas de co-morbidités cardiovasculaires sous-jacentes le comportement sympathique produit par la kétamine peut être assez mal toléré.18 De plus, chez les patients fortement hypo volémiques qui sont déplétés en catécholamines, la kétamine peut induire une hypotension en dépit de ses effets sympathomimétiques.19
Arrêt cardiaque
Chez les patients ayant un retour spontané à la circulation à la suite d’un arrêt cardiaque, il est important de maintenir une stabilité cardiovasculaire. Dans ce cas de figure, certains auteurs ont suggéré l’utilisation de midazolam 0,1 mg/kg, fentanyl 2 mcg/kg et rocuronium 1 mg/kg13 pour l’induction, car cela peut éviter la tachycardie et donc améliorer la perfusion myocardique, aussi bien que réduire les effets hypertensifs de l’intubation en évitant une augmentation de la post charge.
Traumatisme crânien isolé
Chez les patients avec un traumatisme crânien sévère, le maintien d’une pression sanguine systolique supérieure à 90 mm Hg a été démontré réduire la mortalité. Afin de prévenir une lésion cérébrale secondaire, une anesthésie balancée est requise. Celle-ci peut être obtenue par fentanyl, propofol et rocuronium, bien que la kétamine associée au fentanyl convienne également (voir le paragraphe « Controverses habituelles »).14 Habituellement, une perfusion ou des bolus répétés de vasopresseur seront nécessaires pour maintenir une pression sanguine systolique adéquate après l’induction.
AGENTS POUR LA MAINTENANCE
Les praticiens devraient être conscients que l’induction est seulement le début de l’anesthésie. Dans la période post AUPH immédiate, il est essentiel de réévaluer les patients, d’optimiser leur état et de préparer à l’avance leur transport. Ce dernier point inclue la planification et la délivrance du maintien de l’anesthésie. Il est très facile de perdre un moment à partir de l’instant où l’intubation a été réalisée. Le guide de l’Institut National de la Santé et de la Qualité des Soins (NICE) pour l’AUPH recommande que le délai d’appel aux services d’urgence pour l’induction d’une AUPH soit inférieur à 45 minutes. La même recommandation suggère que le délai entre l’AUPH et le moment de quitter le site soit aussi inférieur à 15 minutes. Pour éviter cela, l’inertie post intubation doit être évitée.20
Plusieurs associations d’agents peuvent être utilisées pour la maintenance de l’anesthésie, incluant des bolus de kétamine, de midazolam et de morphiniques ou de perfusion de propofol et de morphiniques. Le choix définitif des agents de maintenance sur l’état du patient individuel et l’expérience de l’opérateur. Des soins particuliers sont nécessaires pour s’assurer que les perfusions de maintien ne sont pas obstruées (i.e. par un bandage, ou une inflation trop fréquente du brassard de prise de tension non invasive). Des doses répétées d’un curare non dépolarisant de longue durée d’action seraient à employer.
CONTROVERSES HABITUELLES
Immobilisation du rachis cervical
L’immobilisation du rachis cervical a été l’objet de controverses durant plusieurs années, et la NICE a émis de multiples recommandations sur le sujet à mesure que de nouvelles évidences étaient apparues.14 L’immobilisation du rachis cervical repose sur le principe que lors d’un traumatisme, il peut y avoir une lésion du rachis cervical, avec le risque de lésions supplémentaires en cas de mobilisation du rachis cervical. Certains auteurs ont argué du fait que la force initiale significative appliquée au rachis produit une lésion rachidienne et une lésion médullaire, sans mobilisation subséquente de faible force.21 De plus, ils reconnaissent que des colliers rigides peuvent augmenter la pression intra cérébrale en réduisant le flux veineux alors que beaucoup de traumatisés à risque de lésion du rachis cervical ont aussi habituellement des lésions cérébrales associées, ce qui est un facteur significatif à considérer.19 Dans le contexte de l’AUPH, l’immobilisation du rachis cervical avec un collier produit souvent une réduction significative du meilleur degré de laryngoscopie obtenu. La recommandation NICE la plus récente suggère qu’à tous les stades de l’évaluation, une immobilisation manuelle du rachis cervical en position sagittale devrait être utilisée, en particulier au cours de toute intervention sur les voies aériennes.20 Les patients non-coopérants ou agités, aussi bien que les enfants, seront autorisés à trouver une position confortable. Dans ces groupes, les colliers ne sont pas recommandés, et la stabilisation dans l’alignement par traction manuelle devrait être utilisée si possible. Les colliers sont contre-indiqués chez les patients avec une atteinte des voies aériennes et des déformations cervicales telle que la spondylarthrite ankylosante.22 En conclusion, le maintien de la liberté des voies aériennes doit toujours avoir la priorité sur l’immobilisation cervicale.
Utilisation en routine de la pression cricoïdienne
En 1961, Sellick23 décrivit le premier l’application en direction postérieure d’une pression sur le cartilage cricoïde pour occlure le haut oesophage, et prévenir ainsi une régurgitation du contenu gastrique dans le pharynx. Depuis lors, la valeur de la pression sur le cricoïde est discutée en raison du manque de preuve évidente de bénéfice et une certaine existence d’un risque potentiel. Les preuves à l’encontre de son utilisation en routine consistent en rapport d’observations d’inhalation fatale en dépit de la pression sur le cricoïde,24-25 d’un effet négatif sur l’ouverture des voies aériennes et sur la ventilation,26 rendant plus difficile la visualisation du larynx, et produisant des traumatismes des voies aériennes.27 Dans une étude extensive récente basée sur l’analyse de 1 195 observations, Caruana et coll.27 n’ont pas trouvé de relation statistiquement significative entre la pression cricoïde pour l’intubation pré hospitalière et une laryngoscopie difficile. Cependant, les mêmes auteurs décrivaient une incidence statistiquement augmentée de traumatismes des voies aériennes en relation avec une laryngoscopie avec pression du cricoïde. Ellis et bien d’autres ont donc suggéré que les praticiens retiennent à la fois une attention de problèmes éventuels liés à une application de pression cricoïdienne et un seuil bas pour supprimer ou réduire la pression au cours de l’AUPH.30-31
Kétamine dans les traumatismes crâniens
La kétamine est fréquemment utilisée chez les traumatisés en raison de ses effets connus sur le maintien du tonus sympathique. Il a été historiquement suggéré que son utilisation est associée à une augmentation du flux sanguin cérébral, entraînant en conséquence une augmentation de la pression intra cérébrale, cette dernière ayant un effet clairement délétère dans les lésions aigues du cerveau. Toutefois, une étude plus récente sur l’utilisation de la kétamine dans les traumatismes crâniens a réfuté cette notion, suggérant au contraire que son utilisation produit une diminution de la consommation cérébrale d’oxygène,30 qu’il n’y a pas d’augmentation de la pression intra crânienne dans le contexte d’une ventilation contrôlée, et que cela pourrait en fait augmenter la perfusion cérébrale. La kétamine pourrait donc être considérée comme sans danger et potentiellement bénéfique à utiliser chez des patients avec des lésions cérébrale.31
Conclusion
L’AUPH est une intervention à haut risque qui peut avoir un impact positif significatif sur le devenir du patient si elle est réalisée de façon appropriée. Ce didacticiel apporte une vue générale des facteurs à prendre en considération pour une AUHP, incluant la sélection des patients, les conditions d’environnement, les compétences de l’équipe, et le choix des agents pour l’induction et le maintien de l’anesthésie. D’autres lectures suggérées incluent le transfert et le transport du patient (ATOTW 319 et 330) et l’utilisation de la kétamine (ATOTW 381).
REFERENCES
- Association of Anaesthetists of Great Britain and Ireland. AAGBI: Safer prehospital anaesthesia 2017. Anaesthesia. 2017;72:379-390. https://www.aagbi.org/sites/default/files/Safer%20pre_hospital%20anaesthesia2017_0.pdf. Accessed May 20, 2018.
- National Enquiry Into Patient Outcome and Death. Trauma: who cares? http://www.ncepod.org.uk/2007report2/ Downloads/SIP_summary.pdf. Published 2007. Accessed May 20, 2018.
- Smith RM, Conn AK. Prehospital care—scoop and run or stay and play? Injury. 2009;40(suppl 4):S23-S26.
- Kauver DS, Wade CE. The epidemiology and modern management of traumatic hemorrhage: US and international perspectives. Crit Care. 2009;5:S1.
- Royal College of Anesthetists and Difficult Airway Society. 4th National Audit Project (NAP4): major complications of airway management in the United Kingdom report and findings. https://www.rcoa.ac.uk/node/4211. Published March 2011. Accessed May 5, 2018.
- Silvestri S, Ralls GA, Krauss B, et al. The effectiveness of out-of-hospital use of continuous end-tidal carbon dioxide monitoring on the rate of unrecognized misplaced intubation within a regional emergency medical services system. Ann Emerg Med. 2005;45;497-503.
- Li J, Murphy-Lavoie H, Bugas C, et al. Complications of emergency intubation with and without paralysis. Am J Emerg Med. 1999;17:141-143.
- Lockey DJ, Crewdson K, Lossius HM. Pre-hospital anaesthesia: the same but different. Br J Anaesth. 2014;113(2):211-219. https://doi.org/10.1093/bja/aeu205. Accessed May 20, 2018.
- Cantle PM, Cotton BA. Balanced resuscitation in trauma management. Surg Clin North Am 2017;97:999-1014.
- Gerhardt RT, Strandenes G, Cap AP, et al. Remote damage control resuscitation and the Solstrand Conference: defining the need, the language, and a way forward. Transfusion. 2013;53:9S-16S.
- Chrimes N, Fritz P. The vortex approach. Safe Apnoea time website. http://vortexapproach.org/safeapnoeatime/#apox. Published 2016. Accessed May 20, 2018.
- Awes EG, Campbell I, Mercer D. Inflation pressure, gastric insufflation and rapid sequence induction. Br J Anaesth. 1987;59:315-318.
- Lyon RM, Perkins AB, Chatterjee D, et al. Significant modification of traditional rapid sequence induction improves safety and effectiveness of pre-hospital trauma anaesthesia. Crit Care. 2015;19:134.
- Miller M, Groombridge CJ, Lyon R. Haemodynamic changes to a midazolam–fentanyl–rocuronium protocol for pre- hospital anaesthesia following return of spontaneous circulation after cardiac arrest. Anaesthesia. 2017;72:585-591.
- Hossfeld B, Bein B, Boettiger BW, et al. Recommended practice for out-of-hospital emergency anaesthesia in adults: statement from the Out-of-Hospital Emergency Anaesthesia Working Group of the Emergency Medicine Research Group of the German Society of Anaesthesiology and Intensive Care. Eur J Anaesthesiol. 2016;33(12):881-897.
- Oglesby A. Should etomidate be the induction agent of choice for rapid sequence intubation in the emergency department? Emerg Med J. 2004;21:655-659.
- Jabre P, Combes X, Lapostolle F, et al. Etomidate versus ketamine for rapid sequence intubation in acutely ill patients: a multicentre randomised controlled trial. Lancet. 374:9686:293-300.
- Joint Formulary Committee, ed. BNF (British National Formulary) 74. Chapter 15 ‘‘Anaesthesia’’, London, UK: Pharmaceutical Press; 2017-2018:1234.
- Miller M, Kruit N, Heldreich C, et al. Response after rapid sequence induction with ketamine in out-of-hospital patients at risk of shock as defined by the shock index. Ann Emerg Med. 2016;68(2):181-188.e2.
- NICE guidance [NG39]. Major trauma: assessment and initial management. https://www.nice.org.uk/guidance/ng39/ chapter/Recommendations. Published February 2016. Accessed August 16, 2018.
- Benger J, Blackham J. Why do we put cervical collars on conscious trauma patients? Scand J Trauma Resusc Emerg Med. 2009;17:44
- NICE guideline [NG41]. Spinal injury: assessment and initial management. https://www.nice.org.uk/guidance/ng41/ chapter/Recommendations. Published February 2016. Accessed May 20, 2018.
- Sellick BA. Cricoid pressure to control regurgitation of stomach contents during induction of anaesthesia. Lancet. 1961;2:404-406.
- Robinson JS, Thompson JM. Fatal aspiration (Mendelson’s) syndrome despite antacids and cricoid pressure. Lancet. 1979;2:228-230.
- Williamson R. Cricoid pressure. Can J Anaesth. 1989;36:601.
- Hartsilver EL, Vanner RG. Airway obstruction with cricoid pressure. Anaesthesia. 2000;55:208-211.
- Caruana E, Chevret S, Pirracchio R. Effect of cricoid pressure on laryngeal view during prehospital tracheal intubation: a propensity-based analysis. Emerg Med J. 2017;34:132-137.
- Ellis DY, Harris T, Zideman D. Cricoid pressure in emergency department rapid sequence tracheal intubations: a risk- benefit analysis. Ann Emerg Med. 2009;50(6):653-665.
- Harris T, Ellis, D, Foster L, et al. Cricoid pressure and laryngeal manipulation in 402 pre-hospital emergency anaesthetics: essential safety measure or a hindrance to rapid safe intubation? Resuscitation. 2010;81(7):810-816.
- Morris C, Perris A, Klein J, et al. Anaesthesia in haemodynamically compromised emergency patients: does ketamine represent the best choice of induction agent? Anaesthesia. 2009;64:532-539.
- Himmelseher S, Durieux ME. Revising a dogma: ketamine for patients with neurological injury? Anesth Analg. 2005;101:524-534.



