Obstetric Anaesthesia
QUESTIONS
Avant de poursuivre, essayer de répondre aux questions suivantes. Les réponses avec des explications se trouvent à la fin de l’article. Répondre par VRAI ou FAUX:
- Au sujet de la cardiomyopathie du péripartum (CMPP):
- L’étiologie est bien connue
- La dysfonction diastolique est une évolution courante
- Récupération totale dans 80% des cas
- Il s’agit souvent d’un diagnostic d’exclusion
- Les résultats suivants de l’ECG sont associés à la grossesse
- Déviation à droite de l’axe du coeur
- Sous décalage du segment ST
- Onde Q dans la dérivation III
- Inversion de l’onde T dans les dérivations inférieures
- Extrasystoles
- La CMPP:
- Survient au cours du 1er trimestre de la grossesse
- Peut s’observer jusqu’à 5 mois après l’accouchement
- Les patientes atteintes ont une FEVG > 45%
- Elle est associée à un thrombus pariétal
- La mortalité peut dépasser 50%
- Les facteurs de risques de survenue d’une CMPP sont:
- Age maternel avancé (>35ans)
- Multiparité
- Utilisation des tocolytiques
- Primiparité
- Origine ethnique
- Concernant la prise en charge de la CMPP:
- Les bêtabloquants amélioraient le pronostic
- Elle doit être pluridisciplinaire
- La CMPP peut malheureusement arriver au cours des grossesses ultérieures
- Le traitement anticoagulant est contre indiqué
- Les anti arythmiques doivent être évités
CAS CLINIQUE
Une femme de 37 ans 4ème geste 3ème pare se présente à 36 semaines d’aménorrhée aux urgences pour une dyspnée nocturne paroxystique à type d’orthopnée avec oedèmes des membres inferieurs. Ses trois précédentes grossesses se sont déroulées sans problème avec à chaque fois un accouchement par voie basse. Dans ses antécédents médicaux on note une hypothyroidie et une obésité morbide (IMC 40). Elle ne présente aucun ATCD cardiaque connu ni familial. Elle ne consommait ni drogue ni alcool de façon significative.
À l’examen la patiente est tachypnéique et tachycarde au repos, avec une tension artérielle normale. La saturation en oxygène était de 92% en air ambiant. Il y avait des râles crépitants aux bases pulmonaires à l’auscultation. L’analyse de gaz du sang artériel indique une alcalose respiratoire avec une hypoxémie légère. L’électrocardiogramme (ECG) montre une tachycardie sinusale et un bloc de branche gauche, la radiographie du thorax une cardiomégalie avec un épanchement dans la scissure horizontale et une hyperclarté du lobe supérieur.
L’échocardiographie transthoracique indique un dysfonctionnement ventriculaire gauche sévère, avec une fraction d’éjection de 15-17%, une cardiomyopathie dilatée (diamètre à la fin de diastole ventriculaire gauche 81mm), une insuffisance mitrale sévère, une insuffisance tricuspidienne modérée et une HTAP modérée.
INTRODUCTION
La cardiomyopathie du postpartum (CMPP) est une affection rare qui survient au dernier trimestre de la grossesse et en postpartum. Elle est caractérisée par une insuffisance cardiaque qui survient en absence de toute cause identifiable. Elle est associée à un taux de morbidité mortalité élevé. Un diagnostic rapide et une prise en charge agressive conditionnent le pronostic.
INCIDENCE
La vraie incidence de la CMPP est inconnue. Les incidences rapportées varient entre 1 pour 3000 à 1 pour 10000 grossesses.
ETIOLOGIE ET PHYSIOPATHOLOGIE
L’étiologie de la CMPP n’est pas connue. Plusieurs mécanismes pourraient être impliqués : facteurs immunologiques, une réponse hormonale anormale, des anomalies inflammatoires, une myocardite ou une prédisposition génétique.
La CMPP se manifeste principalement comme une dysfonction ventriculaire systolique allant jusqu’à la réduction globale de la contraction du myocarde et donc de la fraction d’éjection du ventricule gauche. Il s’en suit des mécanismes compensatoires avec une hypertrophie ventriculaire gauche et augmentation du volume télé diastolique et du volume d’éjection systolique. Quand ces mécanismes sont dépassés l’insuffisance cardiaque s’installe.
FACTEURS DE RISQUE DE CMPP
- Age maternel > 30 ans
- Multiparité
- Groupe ethnique – descendants africains
- Obésité
- Grossesse multiple
- HTA gravidique
- HTA essentielle
- Tocolyse par bêtamimétiques
- Cocaïne
SIGNES CLINIQUES ET DIAGNOSTIC
La dyspnée d’effort et l’orthopnée sont communes au 3ème trimestre de la grossesse. Le diagnostic de CMPP peut être retardé si ces symptômes sont à tort attribués aux modifications physiologiques normales de la grossesse. Les symptômes de la CMPP incluent : dyspnée, orthopnée, dyspnée nocturne paroxystique, palpitations, hémoptysie et oedèmes périphériques. Ils se présentent sous forme d’insuffisance ventriculaire gauche aigue ou sub aigue.
Des tachyarythmies peuvent s’observer avec tachycardie supra ventriculaire, fibrillation auriculaire et rarement tachycardie ventriculaire. Le risque de thromboembolie est accru dû à une potentielle formation de thrombus pariétal.
La CMPP est un diagnostic d’exclusion. Les parturientes avec les cardiopathies congénitales ou acquises peuvent se présenter avec des symptômes similaires au dernier trimestre de la grossesse ou au cours du travail. Par ailleurs les parturientes présentant une coronaropathie méconnue ou une autre pathologie cardiaque sont moins capables de tolérer les modifications physiologiques hémodynamiques, normales de la grossesse.
Le diagnostic de la CMPP repose sur 4 critères1
- Insuffisance cardiaque survenant entre le dernier trimestre de la grossesse et le 5ème mois postpartum
- Absence d’autre cause identifiable d’insuffisance cardiaque
- Absence de symptômes ou de maladie cardiaque avant la grossesse tardive
- Insuffisance ventriculaire gauche définie par une FEVG < 45% ou une fraction de raccourcissement < 30%
Les critères cardiomyopatiques 2-4 survenant plus tôt que le 3ème trimestre de la grossesse sont considérés comme une cardiomyopathie associée à la grossesse. La physiopathologie est similaire à celle de la CMPP².
DIAGNOSTIC DIFFERENTIEL
Le diagnostic différentiel de la CMPP inclut :
- Embolie pulmonaire
- Sepsis sévère
- Embolie amniotique
- Préeclampsie/ HTA gravidique
- Arythmie
- Anémie sévère
- Infarctus du myocarde
- Cardiomyopathie dilatée ou autres étiologies (voir tableau 1)
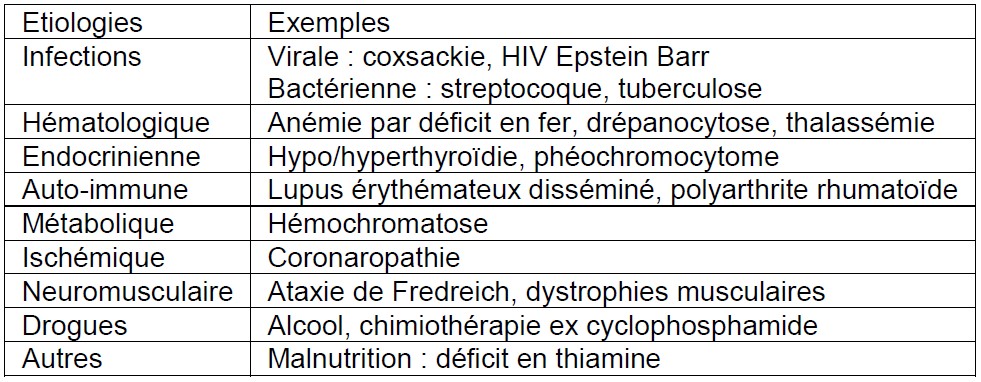
Tableau 1: Causes de cardiomyopathie dilatée
EXAMENS PARACLINIQUES
- ECG
- Echodoopler transthoracique
- IRM cardiaque
- Coronarographie
- Recherche virale
- Dosage BNP (B-type Natriuretic Peptide) : marqueur sensible mais peu spécifique
PRONOSTIC
Le pronostic est sévère et la CMPP est l’un des facteurs de surmortalité maternelle3. L’un des indicateurs de pronostic est le degré d’insuffisance cardiaque à l’admission défini par la classification de NYHA (New York Heart Association) ou par l’échographie transthoracique.
Le taux de mortalité est entre 15 et 50%. 30 à 50% auront une évolution favorable et retrouver une FEVG >50%.
TRAITEMENT
Le diagnostic précoce de la CMPP conditionne sa meilleure prise en charge.
Une prise en charge multidisciplinaire par une équipe expérimentée est essentielle et doit associer un obstétricien, un cardiologue particulièrement impliqué dans les pathologies obstétricales, et un anesthésiste. Quand la CMPP survient pendant la grossesse, la prise en charge de la mère prime et une délivrance prématurée est parfois indispensable. Il est dans ce cas nécessaire de discuter avec le néonatologue sur le moment idéal d’extraction foetale et les répercussions de la pathologie maternelle sur le bébé. De la même manière, il faudra prévenir précocement le réanimateur de la possibilité d’admission de la mère en postpartum. Le niveau de maternité devant prendre en charge cette parturiente dépend du moment de survenu de la CMPP.
Traitement médicamenteux
Le traitement de la CMPP est similaire à celui de toute insuffisance cardiaque quelque soit la cause et associe le maintien de l’oxygénation, la restriction hydro sodée, le traitement de la surcharge ventriculaire par les vasodilatateurs et les diurétiques.
Il a été prouvé que les inhibiteurs de l’enzyme de conversion (IEC) permettent d’améliorer la mortalité de l’insuffisance cardiaque et sont recommandés en première intention dans le traitement de la CMPP. Les antagonistes des récepteurs de l’angiotensine (ARA), constituent une alternative chez les patientes intolérantes aux IEC. Les ARA et IEC sont contre indiqués pendant la grossesse en raison du risque de malformation foetale. L’administration d’IEC aux deuxième et troisième trimestres de la grossesse accroit le risque de fausse couche spontanée, de malformation rénale congénitale, d’oligo-amnios et d’autres anomalies congénitales. Les IEC et ARA ne sont pas recommandés chez les mères allaitantes en raison du risque d’hypotension néonatale. 4
Le traitement en post-partum par un inhibiteur de l’IEC reste indiqué aussi longtemps que le ventricule gauche est défaillant. À plus long terme les IEC peuvent améliorer le remodelage cardiaque.
Le traitement par les dérivés nitrés, comme le dinitrate d’isosorbide, peut être utilisé en toute sécurité pendant la grossesse. Ces médicaments réduisent la postcharge, la précharge et les pressions de remplissage cardiaque.
Les bêta-bloquants améliorent la survie des patientes et préviennent les tachyarythmies.
La digoxine est considérée comme sûre pendant la grossesse et peut être utilisée pour son effet inotrope positif et pour le traitement des fibrillations auriculaires. Les concentrations plasmatiques de digoxine doivent être surveillées attentivement.Les diurétiques de l’anse, par exemple le furosémide, peuvent réduire la congestion pulmonaire et les oedèmes périphériques et peuvent être utilisés en toute sécurité pendant la grossesse et l’allaitement.
Les inhibiteurs calciques sont généralement évités en raison de leurs propriétés inotropes négatives. Les antagonistes de l’aldostérone, tels que le spironolactone ne sont pas recommandés pendant la grossesse.
La biopsie endomyocardique peut être effectuée afin de déterminer si l’immunoglobuline intraveineuse peut être bénéfique. Des éléments de preuve sur de petits essais permettent de suggérer cette thérapie ciblée et d’autres comme la bromocriptine et la pentoxifylline, peuvent être bénéfiques si une biopsie montre une composante 5, 6,7 inflammatoire. Toutes les CMPP ne sont pas associées à une myocardite inflammatoire et le traitement à l’immunoglobuline n’est pas recommandé de manière empirique.
En raison du risque de thromboembolie veineuse et de thrombus mural associé à la CMPP, la prophylaxie par les héparines de bas poids moléculaire (HBPM) est indiquée. Si des séquelles thromboemboliques ou un thrombus mural ont été identifiés, une héparinothérapie curative est indiquée.
Traitement non pharmacologique
Les patientes en détresse vitale peuvent nécessiter une ventilation non-invasive ou intubation, une ventilation assistée et des amines vasopressives.
Dans les cas graves une pompe intra-aortique, un dispositif d’assistance ventriculaire gauche ou une ECMO (Extracorporeal Membrane Oxygénation) peuvent être nécessaires. La transplantation cardiaque peut être indiquée pour les patients en état grave qui ne répondent pas aux traitements pharmacologiques.
Un défibrillateur interne et un pace maker peuvent être nécessaires après la phase aiguë.
Counselling pré-conception
Elle devrait être effectuée à toutes les femmes ayant des antécédents de CMPP. Il y a un risque important de CMPP lors de grossesses ultérieures. Les femmes ayant une insuffisance cardiaque post CMPP (NYHA III et IV), ou celles avec une fraction d’éjection ventriculaire gauche (FEVG) inférieure à 30% sont les plus à risque lors de grossesses ultérieures. Ces femmes à risque doivent avoir des informations sur les risques des grossesses ultérieures et des conseils sur la contraception ainsi que la nécessité d’interrompre une éventuelle grossesse.
Prise en charge anesthésique
La CMPP pose de nombreux défis pour l’anesthésiste. La technique d’anesthésie sera influencée par l’urgence de l’accouchement et l’état physiologique de la parturiente. Les femmes chez qui on soupçonne une CMPP, ou des antécédents de CMPP devraient être revues par un anesthésiste en temps opportun en vue de planifier le déroulement du travail, l’accouchement et les soins post-partum.
Le choix du mode d’accouchement devrait tenir compte des antécédents obstétricaux de la patiente, de son état hémodynamique actuel et de sa réponse au traitement médical. L’accouchement par voie basse est une option pour les patientes atteintes de CMPP compensée. Les techniques permettant de limiter l’augmentation des catécholamines plasmatiques, les résistances vasculaires systémiques et la charge de travail du myocarde sont conseillées.
La compression aorto-cave doit être évitée à tout moment en évitant le décubitus dorsal strict. Un monitorage ECG, saturation artérielle en oxygène et pression artérielle, doit être initié précocement avec si possible un monitorage invasif de pression artérielle. Afin de limiter le stress cardiovasculaire, l’analgésie péridurale est recommandée en tout début de travail. Cela permettra non seulement de réduire la réponse sympathique causée par des contractions douloureuses, mais aussi de diminuer la post-charge et d’atteindre une anesthésie chirurgicale si l’intervention est nécessaire.
L’extraction foetale peut être instrumentale afin de réduire la charge de travail du myocarde et les effets cardiovasculaires néfastes des manoeuvres de Valsalva prolongées pendant la poussée.
Les deux techniques anesthésie générale et locorégionale ont été décrites pour la césarienne.8 Le monitorage peropératoire devrait inclure la pression artérielle invasive. La surveillance du débit cardiaque fournira des informations supplémentaires qui pourront aider dans la gestion périopératoire.
Les objectifs de la prise en charge anesthésique sont les suivants:
- Maintenir la perfusion myocardique en évitant:
- Arythmies
- Les épisodes d’hypotension ou de tachycardie
- Optimiser le débit cardiaque
- Maintenir la précharge, mais éviter la surcharge liquidienne
- Maintenir / améliorer la contractilité du myocarde
- Prévenir l’augmentation de post-charge
L’anesthésie péridurale avec des bolus titrés ou la péri-rachianesthésie combinée avec une faible dose en rachianesthésie devront permettre d’atteindre ces objectifs. L’anesthésie locorégionale centrale réduit la postcharge et évite l’utilisation d’agents anesthésiques généraux qui permettent de réduire la contractilité du myocarde. Les opioïdes en péridurale ou rachianesthésie permettent une bonne analgésie postopératoire réduisant ainsi les médiateurs sympathiques post-partum augmentés en post-charge. Des baisses significatives des résistances vasculaires systémiques doivent être évitées afin que la perfusion coronaire soit maintenue. En cas d’anesthésie péridurale, l’attention devrait être accordée à la dernière injection d’anticoagulants.
En cas d’anesthésie générale, l’induction doit être aussi lente que possible afin de minimiser aussi bien l’hypotension que l’hypertension artérielle. La réponse pressive de la laryngoscopie et l’intubation doit être atténuée par l’administration d’une dose appropriée d’opioïde à action rapide comme l’alfentanil ou le rémifentanil. Les inotropes, tels que la dobutamine, les sensibilisateurs de protéines contractiles de calcium comme le levosimendan ou les inhibiteurs de la phosphodiestérase comme le milrinone, peuvent être nécessaires pour compenser la dépression myocardique d’agents anesthésiques intraveineux et volatiles. Les vasopresseurs peuvent également être nécessaires pour contrecarrer la vasodilatation et maintenir la perfusion coronaire. La précharge doit être maintenue et un monitorage cardiaque mini-invasif ou invasif peut fournir des informations utiles pour guider ces thérapies.
Les utérotoniques doivent être utilisés avec prudence en raison de leurs effets secondaires:
- L’ocytocine peut causer une diminution marquée de la résistance vasculaire systémique et à des doses plus élevées a un effet antidiurétique.
- L’ergométrine peut entraîner des augmentations significatives de la post-charge
Après la délivrance, la patiente doit être placée en unité de soins intensifs avec monitorage hémodynamique invasif continu, la gestion prudente du remplissage et une analgésie suffisante.
RESUME
- La cardiomyopathie du postpartum est une situation rare avec des taux de mortalité élevés
- La CMPP a des critères diagnostics stricts
- Un diagnostic précoce permet d’améliorer le pronostic
- La prise en charge est pluridisciplinaire
REPONSES
1.
- F
- F
- F
- F
- T
L’étiologie est inconnue. Il peut s’agir de facteurs immunologiques, de modifications inflammatoires, d’une myocardite ou d’une prédisposition génétique.
La CMPP affecte de façon prédominante la fonction systolique.
La vraie incidence est inconnue.
La morbidité mortalité est élevée. 30-50% des patients vont s’améliorer et retrouver une FEVG ≥50%.
Le diagnostic de CMPP est un diagnostic d’exclusion.
2.
- F
- T
- F
- T d. T
- T
La déviation axiale peut s’observer durant la grossesse du fait d’un déplacement de l’apex. Une onde Q en dérivation III est une variante normale dans la population générale et n’est pas spécifique de la grossesse
3.
- F
- T
- F
- T
- T
La CMPP est définie comme la survenue d’une insuffisance cardiaque en fin de grossesse ou dans les 5 mois post-partum. L’insuffisance ventriculaire gauche dans la CMPP est définie par une fraction d’éjection ventriculaire gauche (FEVG) < 45% ou une fraction de raccourcissement (FR) < 30%.
4.
- T
- T
- T
- F
- T
Les facteurs de risque de CMPP incluent également la multipartite et l’origine ethnique (ex des descendants africains).
5.
- T
- T
- F
- F
- T
L’anti coagulation réduit le risque de maladie thromboembolique.
Les troubles du rythme doivent être évités pour optimiser la perfusion coronarienne, la contraction auriculaire et ventriculaire, le volume d’éjection systolique et donc la post-charge.
REFERENCES
- Sliwa K, Hilfiker-Kleiner D, Petrie MC, et al. Current state of knowledge on aetiology, diagnosis, management, and therapy of peripartum cardiomyopathy: a position statement from the Heart Failure Association of the European Society of Cardiology Working Group on peripartum cardiomyopathy. Eur J Heart Fail 2010;12:767-78.
- Elkayam U, Akhter MW, Singh H, et al. Pregnancy-associated cardiomyopathy: clinical characteristics and a comparison between early and late presentation. Circulation 2005;111:2050-5.
- Steer P, Gatzoulis M and Baker P. Heart Disease and Pregnancy. London: RCOG Press 2006
- Drug and safety undate May 2009, vol 2 issue 10:3. http://www.mhra.gov.uk/safetyinformation/drugsafetyupdate/CPN088003.
- Mason JW, O’Connell JB, Herskowitz A, et al. A clinical trial of immunosuppressive therapy for myocarditis. The Myocarditis Treatment Trial Investigators. N Engl J Med 1995;333:269-75.
- Sliwa K, Blauwet L, Tibazarwa K, et al. Evaluation of bromocriptine in the treatment of acute severe peripartum cardiomyopathy: a proof-of-concept pilot study. Circulation 2010;121:1465–73.
- Sliwa K, Skudicky D, Candy G, Bergemann A, Hopley M, Sareli P. The addition of pentoxifylline to conventional therapy improves outcome in patients with peripartum cardiomyopathy. Eur J Heart Fail 2002;4:305–9.
- Soni B, Gautam P L, Grewal A, Kaur H. Anaesthetic management of two cases of peripartum cardiomyopathy. J Obstet Anaesth Crit Care 2011;1:41-5



