General Topics
PUNTOS CLAVES
- Ketamina es un agente anestésico disociativo que a diferentes dosis puede ser usado como un analgésico, sedante, inductor de la anestesia y como agente para el mantenimiento de la anestesia.
- Ketamina tiene ventajas específicas sobre algunos otros agentes sedantes y anestésicos. Los reflejos de la vía aérea y el tono son a menudo preservados durante la sedación con Ketamina y además tiene un excelente perfil hemodinámico.
- Ketamina tiene un papel único en medicina prehospitalaria, de emergencias y cuidados críticos y es comúnmente usada por anestesiólogos alrededor del mundo.
- Las investigaciones han sugerido que el uso de isómeros ópticos de la ketamina pueden ayudar a reducir los efectos indeseados.
INTRODUCCION
La Ketamina es un potente agente analgésico y anestésico disociativo que ha sido usado desde su descubrimiento y síntesis en 1962. La popularidad de la ketamina es debida a su capacidad única de producir rápidos efectos sedantes, analgésicos y amnésicos junto con sus beneficiosas características secundarias. Estas últimas incluyen bronco dilatación y mantenimiento de tanto los reflejos de la vía aérea como del tono del sistema nervioso simpático.1 Estudios recientes han sugerido también propiedades neuroprotectoras2 y anti-inflamatorias3 previamente desconocidas
Debido a sus propiedades únicas y a su versatilidad, la ketamina ha ganado una popularidad creciente en la medicina prehospitalaria y de emergencias así como también está siendo usada ampliamente por anestesiólogos y anestesistas alrededor del mundo. Los usos mas nuevos incluyen protocolos analgésicos a bajas dosis, terapia adyuvante en bloqueos anestésicos locales, indicaciones en vías aéreas hiperreactivas así como también como sedación para procedimientos de rutina y complejos en quirófanos, departamento de emergencia y unidades de cuidados críticos.
A pesar de las ventajas potenciales de la ketamina, no ha demostrado ser universalmente popular debido a su efecto de “emergencia” potencialmente desagradable, su potencial como droga de abuso y la introducción de otros fármacos sedantes y analgésicos.
La investigación usando isómeros de la ketamina tales como ‘S-(þ)-ketamina’, un agonista mas potente del receptor N-metil-D-aspartato (NMDA), permitió el uso de dosis mas bajas con efectos similares.4 Esto al parecer resulta en una mas baja incidencia de los tradicionales efectos psicoactivos, mientras se mantienen los efectos benéficos del fármaco.5
Este artículo revisará la farmacología y los diferentes usos de la ketamina con referencia a la literatura actual
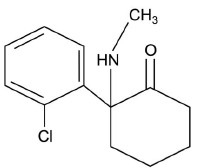
Figura 1. Estructura química de la ketamina. Hay un centro quiral en el anillo ciclohexanona dando los isómeros S y R
FARMACOLOGIA
La ketamina es un derivado de los agentes anestésicos ciclo-hexamino (fenciclidina) usados extensamente en los 1950s. Es un antagonista no competitivo de los receptores NMDA la cual bloquea el sitio de unión de la fenciclidina en el receptor NMDA deteniendo de este modo la despolarización de la neurona. Estos receptores NMDA están localizados a nivel medular, talámico, límbico y cortical. La ketamina interfiere entonces con el flujo aferente sensorial a los centros superiores del sistema nervioso central, afectando la respuestas al dolor y emocional así como la memoria, por lo cual es referido como un “anestésico disociativo”6 La ketamina tiene también algunos efectos secundarios en los receptores opioides lo cual ayuda a propagar su efecto analgésico, así como también en receptores adrenérgicos alfa y beta.
Fórmula estructural
La ketamina (Figura 1) contiene un centro quiral en el carbono C-2 del anillo ciclohexanona; esto significa que dos isómeros ópticos: la S-(þ)-ketamina y la R-(—)-ketamina. El isómero S es farmacológicamente más activo.
En el Reino Unido la ketamina está disponible generalmente como una solución racémica, una mezcla de los isómeros R-(—) y S-(þ) en cantidades iguales. Está disponible en una variedad de concentraciones: 10, 50 y 100 mg ml-1. El isómero óptico S-( )-ketamina (en concentraciones de 5 y 25 mg x ml-1) no está corrientemente disponible en el Reino Unido pero si está disponible en un buen número de países de Europa.
Farmacocinética
Distribución
La ketamina es altamente liposoluble pero tiene una baja disponibilidad para la unión a proteínas. Esto permite una rápida transferencia a través de la barrera hemato-encefálica, conduciendo a concentraciones que son generalmente 4 a 5 veces mas grandes que las plasmáticas. La vida media de distribución es de 7 a 11 minutos.
Metabolismo and Eliminación
La ketamina es fundamentalmente metabolizada en el hígado (80%) a norketamina, la cual en si misma tiene propiedades analgésicas débiles, alrededor del 20% al 30% de la potencia de la ketamina. Los niveles pico de norketamina aparecen en la sangre dentro de los 30 minutos después de la administración intravenosa (IV). La norketamina es entonces hidrolizada principalmente vía gluconoroconjugación y excretada en la orina y la bilis.5
Farmacodinamia
Sistema Nervioso Central
La ketamina produce un estado de trance-como un estado cataléptico, en el cual hay analgesia potente y sedación. Los síntomas de la emergencia afectan al 30% a 50% de las personas. La incidencia es más común con las dosis más altas. Los síntomas pueden incluir una sensación de inquietud, alucinaciones, sueños vívidos, sensación de flotar y delirio.
Cardiovascular
La ketamina parece estimular el sistema nervioso simpático conduciendo a gasto cardiaco incrementado, taquicardia y presión arterial elevada. Debería ser usada entonces con precaución en pacientes con enfermedad cardiaca isquémica. El mecanismo exacto de esto no es conocido; sin embargo, se ha propuesto que la ketamina puede inhibir la re-captación de las catecolaminas circulantes. Se ha notado en pacientes con depleción crónica de catecolaminas, tales como los críticamente enfermos, que la ketamina sola produce un efecto inotrópico negativo. En pacientes con control autonómico normal el efecto inotrópico negativo directo es a menudo contrarrestado por la respuesta simpática central,1 produciendo un incremento global o el mantenimiento de la presión arterial.6
Respiratorio
En contraste con otros agentes anestésicos y sedantes disponibles, el tono de la vía aérea y tanto los reflejos faríngeos y laríngeos son a menudo preservados durante el uso de ketamina. Sin embargo, en niños menores de 12 meses, los reflejos de la vía aérea son más variables e impredecibles.7 La ketamina puede tener un ligero efecto depresor respiratorio vía una disminución en el efecto respiratorio estimulante usual de los niveles elevados de la PaCO2 . Esto es especialmente notable después de la administración de grandes bolos IV donde se han reportado períodos transitorios de apnea.8 La ketamina ha mostrado también causar bronco dilatación, haciéndola el agente de elección para pacientes con crisis asmáticas comprometedoras de la vida que requieren ventilación mecánica.
Otros Efectos
La ketamina incrementa el tono muscular, la glucosa sanguínea y los niveles de cortisol y prolactina plasmáticos.6 Un potencialmente problemático efecto colateral es la salivación incrementada y algunos autores promueven la administración de anti-sialagogos, comúnmente atropina.9
USOS Y EVIDENCIA CORRIENTE
Sedación
La ketamina está siendo usada crecientemente en medicina pre-hospitalaria y de emergencias para sedación y analgesia. Es idealmente apropiada para el manejo de evento traumáticos tales como reducción de fracturas y el tratamiento de quemaduras. El estado disociativo característico visto con la ketamina puede ser alcanzado con un rango de dosis entre 0,25 y 1,5 mg x kg—1 IV.
Para sedación para procedimientos en el departamento de emergencias, se recomienda una dosis de carga administrada en 30 – 60 segundos. Esto produce sedación dentro de 1 minuto, con una duración de 10 – 15 minutos. Existe gran variación en las dosis recomendadas, desde 0,25 a 1,0 mg x kg—1 IV para adultos y 0,25 a 2,0 mg x kg—1 IV para niños.4 Debería notarse que las dosis en los rangos mas altos son comúnmente usadas para la inducción de la anestesia general. Una dosis simple es adecuada para los procedimientos mas cortos, pero para procedimientos mas largos el estado disociativo puede ser mantenido con bolos intermitentes de 0,5 mg x kg—1. Se han desarrollado pautas clínicas prácticas detalladas para el uso de ketamina en el departamento de emergencias10 pero como sucede con el uso de cualquier otro fármaco sedante, se requiere experticia relevante y adecuada monitorización. La monitorización mínima, donde esté disponible, consiste de electrocardiograma continuo, presión arterial no invasiva, saturación de oxígeno y ETCO2 .
La ketamina puede ser usada en forma segura en combinación con otros fármacos como propofol para la inducción o sedación. La coadministración de estos fármacos reduce los requerimientos de cada uno alrededor del 50%,4 reduciendo la incidencia y severidad de los efectos colaterales de ambos agentes. Se ha propuesto que a través de sus acciones simpático-miméticas, la ketamina reduce la hipotensión inducida por propofol, mientras que la coadministración de propofol reduce la incidencia de agitación post-procedimiento vista con ketamina sola. Estudios aleatorios controlados han mostrado recientemente una mejor sedación cuando ambos fármacos son usados juntos comparado con propofol solo.11
Para casos donde el acceso IV es difícil, se ha descrito el uso intramuscular, oral o intranasal de ketamina con buen efecto. El tiempo de aparición del efecto es usualmente más largo para estas rutas cuando se comparan con la administración IV y las dosis requeridas muestran una variabilidad más grande debido a variaciones en la vascularización y absorción gastrointestinal (ver Tabla 1). El uso oral de ketamina, bien sea sola o en combinación con paracetamol y diazepam, puede ser recomendado para el cambio de curas, especialmente en pacientes quemados, minimizando así las visitas al quirófano. Hay algún grado de taquifilaxia con el uso repetido
Los principales efectos colaterales que limitan el uso de la ketamina durante los procedimientos mas cortos son la agitación y los síntomas de emergencia. Ambos son mas comunes con las dosis más altas. Se ha demostrado que las benzodiacepinas son efectivas para reducir la incidencia del fenómeno de emergencia. Se ha descrito muy bien el uso de uso de todas estas: midazolam (0,07-0,1 mg kg-1), diazepam (0,15-0,3 mg kg-1) y lorazepam (2 a 4 mg) .8 Se ha demostrado también que la recuperación de los pacientes en un ambiente tranquilo y controlado con re-evaluación continua reducen la incidencia y severidad de los síntomas de emergencia siguientes a la administración de ketamina..

Tabla 1. Rutas de administración de ketamina y rango de dosis en niños y adultos (Reproducido de Marland and Ellerton 4) Las dosis mencionadas arriba producen un continuum de efectos desde sedación leve hasta una inducción anestésica completa. Como con la administración de cualquier medicamento sedante, se requiere experticia relevante y monitorización adecuada. En niños se han propuesto dosis variables para las rutas intranasal, intraósea e intramuscular y hay una falta de consenso en la literatura de las dosis específicas. Algunos ejemplos de regímenes de dosificación pediátrica son suministrados en algunos de los artículos de referencia.29
aNota: La ketamina debería ser titulada al efecto clínico requerido. bDosis analgésica y sedante. cDosis anestésica. Note que hay alguna superposición entre las dosis sedantes y anestésicas.
ESTUDIO DE CASO 1: ATENCION PREHOSPITALARIA
Una niña sana de 6 años fue vista caer de una pared de 1,82 Mt de altura sobre un piso de concreto y se está quejando de dolor severo en su tobillo derecho. Ella está a 45 minutos del hospital más cercano y un paramédico especialista de la tripulación de la ambulancia está atendiéndola. Ella no perdió la conciencia y no hay reporte de trauma craneoencefálico alguno. La evaluación primaria es la siguiente:
<C>: sin hemorragia catastrófica
A y B: via aerea permeable, respirando espontáneamente, saturacion de oxigeno 99% en aire ambiente
C: Hemodinámicamente estable, pulsos periféricos presentes pero llenado capilar prolongado en el pie derecho (5 segundos versus 2 segundos para los demás).
D: Escala de Coma de Glasgow 15, pupilas simétricas y reactivas, glicemia normal.
E: Fractura-dislocación del tobillo derecho, sin otras lesiones aparentes.
Debido a la disminución de la perfusión en su pie y de la distancia al hospital, se tomó la decisión de reducir la fractura en la escena.
Considere las opciones disponibles para sedación y analgesia que permitan la manipulación.
En este caso se usó una combinación de fentanil y ketamina para inducir un estado disociativo. Después de una monitorización completa (electrocardiograma, oximetría de pulso, presión arterial no invasiva y ETCO2) se administró una dosis inicial de 0,5 mcg x kg-1 de fentanil y 0,2 mg x kg-1 de ketamina. Se aplicó tracción suave pero no debido a dolor. Entonces se administró una dosis adicional de 0,25 mcg x kg-1 de fentanil y 0,2 mg x kg-1 de ketamina con muy buen efecto, permitiendo una reducción exitosa, la cura y ferulización con una férula de vacío. La transferencia se llevó a cabo sin eventualidades.
Inducción y Mantenimiento de la Anestesia
La ketamina está siendo común y crecientemente usada en ambientes hospitalarios y pre-hospitalarios como un agente para la inducción y mantenimiento anestésico para situaciones de emergencia. En inducción de secuencia rápida, una dosis IV de 1 a 2 mg x kg-1 produce anestesia disociativa dentro de 1 a 2 minutos después de la administración. Esto es generalmente mas prolongado que el corto tiempo “brazo-cerebro” para inconciencia visto con los mas tradicionales agentes inductores IV tales como propofol o tiopentona. Sin embargo, en circunstancias donde el control hemodinámico es importante, tales como trauma o sepsis, la ketamina tiene ventajas significativas. También se ha demostrado que tiene otros beneficios importantes incluyendo el que permite una pre-oxigenación mejorada en pacientes agitados cuando se pueden dar dosis reducidas (0,25 – 0,5 mg x kg-1) previo a la inducción total de la anestesia.12 Una dosis reducida de ketamina para la inducción debería ser considerada en pacientes en shock debido a la preocupación acerca de una acción simpático-mimética inadecuada en este grupo de pacientes
El uso de ketamina para anestesia total intravenosa (TIVA) en combinación con relajantes musculares ha sido descrito menos frecuentemente en la literatura. Se ha reportado el uso de ketamina tanto como agente único y en conjunto con otros hipnóticos tales como propofol y benzodiacepinas. Las potenciales indicaciones para TIVA con ketamina incluyen shock cardiogénico, hipovolemia y taponamiento pericárdico, particularmente en áreas de bajos recursos donde el acceso a fármacos vasoactivos puede estar limitado. También se ha descrito la TIVA con ketamina en anestesia pediátrica con buen efecto.8
La anestesia puede ser mantenida usando bolos intermitentes de ketamina IV (0,5 mg x kg-1) o por infusión continua a 10 – 30 mcg x kg-1 min-1 titulada de acuerdo al efecto. Descontinuando la infusión 20 a 30 minutos antes del fin de la cirugía permite una adecuado aclaramiento. Vale la pena destacar que la monitorización con electroencefalografía e índice Biespectral no tiene rol en la monitorización de la profundidad anestésica inducida por ketamina.
Analgesia
La ketamina es un potente analgésico. Actúa como un antagonista NMDA, lo cual, como se discutió previamente, produce analgesia disociativa. Sin embargo, se ha demostrado que a dosis mas bajas desensibiliza las vías del dolor y modula los receptores opioides.13 Varios estudios han demostrado que la administración de dosis pequeñas de ketamina peri-operatoriamente puede reducir los requerimientos de opioides hasta en un 50%.14
Ejemplos de regímenes de analgesia peri-operatoria incluyen las infusiones intra-operatorias de ketamina, regímenes de bajas dosis y analgesia controlada por el paciente. Todas han sido descritas en detalle en una revisión de Cochrane del 2006.14 Esta revisión provee evidencia de la eficacia de la ketamina peri-operatoria en suministrar analgesia efectiva; sin embargo, no concluye sobre dosis óptimas o método de administración. En un estudio aleatorio controlado de pacientes post-operatorios de cirugía abdominal mayor quienes estaban monitorizados en la unidad de cuidados intensivos, se administró ketamina inicialmente en bolo de 0,5 mg x kg-1 seguido de una infusión de 2 mcg x kg-1 x min-1 durante las primeras 24 horas, seguido de 1 mcg x kg-1 x min-1 por las próximas 24 horas. 15 Esto resultó en una reducción significativa del uso de morfina post-operatoriamente.
En el departamento de emergencias y en el ambiente pre-hospitalario se han descrito los regímenes de bajas dosis de ketamina para el manejo del dolor. Las dosis típicamente sugeridas están entre 0,1 y 0,2 mg x kg-1 IV. En un estudio, se dio una dosis de ketamina en bolo de 0,1 mg x kg-1 IV junto con opioides a pacientes con una variedad de presentaciones, incluyendo dolor abdominal, laceraciones, fracturas y dislocaciones.16 Esto produjo analgesia efectiva durante 120 minutos y redujo los requerimientos de opioides y, aunque se presentaron algunos efectos colaterales en el grupo tratado con ketamina, la mayoría fueron considerados menores y tolerables.
A través de la desensibilización de las vías centrales del dolor, hay alguna evidencia que sugiere que la ketamina puede ser útil en pacientes sometidos a cirugía y son usuarios crónicos de opioides. Varios estudios en estas poblaciones han demostrado una reducción en el uso de opioides de mas de 48 horas y mejoraron las escalas de dolor a las 6 semanas después de la ketamina IV intra-operatoria. 17 Recientemente ha habido también interés en el uso intra-operatorio de ketamina para prevenir el dolor crónico post-quirúrgico. Un meta-análisis reciente revisó los estudios buscó los estudios en los que se usaban bajas dosis de ketamina versus placebo intra-operatoriamente y siguieron los pacientes hasta 3, 6 y 12 meses.18 Los resultados mostraron que el dolor post-quirúrgico fue reducido a los 3 y a los 6 meses, aunque no hubo diferencia significativa entre los grupos a los 12 meses. Aunque los estudios iniciales son promisorios, se requieren estudios mas grande y rigurosos para explorar el papel potencial que la ketamina juega en el dolor post-quirúrgico persistente.
Vías Aéreas Híper-reactivas
La ketamina tiene efectos broncodilatadores y ha sido efectiva en pacientes con broncoespasmo agudo. Se cree que el efecto de la ketamina en las vías aéreas se ejerce a través de la modulación de la cascada inflamatoria. Una revisión reciente mostró que puede haber un rol para la ketamina en el asma que no responde a tratamiento convencional.19 Los autores notaron que los pacientes que recibieron ketamina mejoraron clínicamente, tuvieron requerimientos mas bajos de oxígeno y en algunos casos evitaron la ventilación invasiva. Los pacientes ventilados mecánicamente quienes recibieron ketamina para broncoespasmo severo mostraron un mejor intercambio gaseoso, presiones inspiratorias reducidas, mejor ventilación minuto y a menudo pasaron a ser destetados exitosamente de la ventilación. No se reportaron efectos adversos mayores con ketamina en esta revisión de 244 pacientes. La revisión incluyó una mezcla de reporte de casos, series de casos, estudios observacionales y estudios controlados al azar. En los estudios se usaron dosis de carga altamente variables desde 0,1 a 2,0 mg x kg-1 y, dependiendo de la respuesta inicial, la dosis usada para infusión continua varió de 0,15 a 2,5 mg x kg-1 x h-1. Debido al tamaño pequeño de la muestra y a la amplia variedad de las dosis de carga e infusión, se requiere más investigación en esta área.
Usos en Cuidados Críticos
La ketamina tiene un buen número de aplicaciones potenciales dentro de la medicina crítica, incluyendo sedación, analgesia y el tratamiento del broncoespasmo persistente. Se ha reportado que el Ketofol (la combinación de ketamina con propofol) ha sido efectivo para sedaciones de corto tiempo en la población de cuidados críticos. 20 Es importante apreciar que en pacientes críticamente enfermos el efecto inotrópico negativo de la ketamina puede predominar sobre la respuesta cardiovascular positiva o neutral usual a la ketamina. Se han reportado incidentes de disminución inesperada de la presión arterial y/o del gasto cardíaco posterior a la administración de ketamina en algunos pacientes críticamente enfermos; sin embargo, un estudio multicéntrico grande de pacientes sépticos críticamente enfermos no reveló efectos adversos cuando se usó ketamina.21 Se ha sugerido que la ketamina puede tener ventajas potenciales comparada a otros agentes en pacientes con sepsis severa (ver caso de estudio 2). Hay evidencia que sugiere que puede ejercer un efecto protector anti-inflamatorio, recudiendo los efectos sistémicos de la sepsis incluyendo la hipotensión y la acidosis metabólica.22
Se pensó inicialmente que la ketamina estaba contraindicada en pacientes con lesiones cerebrales traumáticas o presión intracraneal elevada. Sin embargo, algunos estudios han mostrado que la ketamina puede ser útil como sedante en este grupo de pacientes. Su uso ha sido asociado con preservación de la presión de perfusión cerebral durante las intervenciones estimulantes en una población de pacientes críticos con lesiones cerebrales.23 Su uso en lesiones craneanas traumáticas sigue siendo polémico pero evidencia reciente (clasificada como nível 2b, GRADO C de Oxford) sugiere que la ketamina no incrementa la presión intracraneal en pacientes con lesión cerebral traumática severa que son sedadas y ventiladas y puede incluso disminuirla.24 Se requiere mas investigación en este campo antes que su uso pueda ser ampliamente recomendado.
CASO DE ESTUDIO 2: SEPSIS
Un hombre de 67 años se presenta al servicio de emergencias con un cuadro de tos productiva, confusión y fiebre de 2 días de evolución. Está hemodinámicamente inestable con hipotensión y taquicardia. Se le diagnosticó septicemia secundaria a una presumible neumonía severa adquirida en la comunidad (CURB65 ¼ 4). El tratamiento inicial consistió en líquidos IV y terapia con antibióticos. A pesar de esto, su condición clínica continúa deteriorándose con empeoramiento de la hipoxemia, hipotensión y acidosis metabólica. Es transferido a la unidad de cuidados críticos para iniciar ventilación mecánica y soporte cardiovascular.
Considere los agentes de inducción disponibles junto con los riesgos y beneficios de usar cada uno de ellos.
En este caso, el agente anestésico escogido fue la ketamina a una dosis de 1,5 mg x kg-1. Esto se debió a su estabilidad cardiovascular cuando se comparó con los agentes inductores alternativos. Hay también alguna evidencia que sugiere que la ketamina tiene algunas propiedades anti-inflamatorias.
Precauciones y Limitaciones
Se considera que la ketamina tiene un muy buen perfil de seguridad. LA sobredosis de ketamina se ha manifestado con sedación prolongada en estudios de casos de niños que inadvertidamente recibieron 5 a 100 veces la dosis recomendada.6 Se han reportado algunos pocos estudios de casos de depresión respiratoria severa durante la administración rutinaria de ketamina con otros medicamentos; sin embargo, primordialmente solo se han reportado episodios de apnea transitorios posterior a grandes bolos IV.
Las contraindicaciones absolutas de la ketamina IV que son mencionadas por el Formulario Nacional Británico25 son hipertensión, pre-eclampsia o eclampsia, enfermedad cardiaca severa, síncope, presión intracraneal elevada y porfiria aguda. La ketamina tampoco es recomendada en niños menores de 3 meses y en pacientes con esquizofrenia. Por favor refiérase a las secciones anteriores en este artículo para mas detalles del uso de ketamina en pacientes con presión intracraneal elevada y/o lesión craneana traumática.
Países en Desarrollo
Actualmente la ketamina es usada ampliamente en todo el mundo debido a su versatilidad, disponibilidad y perfil bajo de efectos colaterales. Ha habido discusión acerca de su potencia de mal uso y si se requieren controles mas estrictos mundialmente. En 2015 la Organización Mundial de la Salud concluyó que debido a la dependencia de la ketamina en algunos países “controlar la ketamina internacionalmente puede limitar el acceso a cirugía esencial y de emergencia, lo cual constituiría una crisis de salud pública en países donde no existen alternativas asequibles”.
La ketamina es uno de los agentes anestésicos mas disponibles en países de ingresos medios y bajos.26 Un reporte reciente encontró que en 12 países de ingresos medios y bajos, solamente el 53% de los centros de salud tenían acceso confiable a máquinas de anestesia funcionales y solo 52% tenían acceso continuo a oximetría de pulso. En promedio, 21% a 45% no tiene equipo básico para el manejo de la vía aérea. En esta encuesta, la anestesia general inhalatoria fue ofrecida solo por el 58% de los respondientes pero entre 70% y 90% reportaron un acceso confiable a la ketamina.
Un estudio que intentó cuantificar el uso de la ketamina en países de ingresos medios y bajos encontró una tasa de complicaciones serias (por ej. muerte, paro cardiaco, apnea, laringoespasmo y aspiración) de solo 0,15% en mas de 12.000 administraciones de ketamina durante cirugías de electivas y de emergencia.27 Esta tasa baja de complicaciones fue a menudo en el contexto de monitorización y destrezas del proveedor variables, sugiriendo que el margen de seguridad del uso de la ketamina en estas situaciones es alto.
Ejemplos adicionales que muestran los usos variados de ketamina en países de ingreso medios y bajos pueden ser encontrados en el Tutorial de la Semana 27 realizado por Craven y Alkhafaji.28
RESUMEN
La ketamina es un fármaco versátil con un perfil único que le permite ser usada exitosamente en una multitud de situaciones alrededor del mundo. Sus dosis variables significan que puede ser usada tanto como agente de inducción con un buen perfil hemodinámico o en mas bajas dosis como un sedante o analgésico confiable. Tiene un rol vital en la medicina prehospitalaria y de emergencias. Como un adyuvante durante la anestesia puede ayudar a reducir los requerimientos de opioides postoperatoriamente. Su uso en cuidados críticos incluye sedación y manejo de asma refractaria; sin embargo, se requiere mas investigación para dilucidar su papel en los pacientes con trauma y lesiones craneales. En el mundo en desarrollo es un fármaco vital y altamente valorado que permite la realización de intervenciones y operaciones que de otra manera pueden ser imposibles, especialmente cuando los recursos son limitados.
La ketamina sufre todavía del estigma tradicional de médicos y del público en general y a menudo se limita su uso debido a preocupación sobre sus efectos sicológicos colaterales. La disponibilidad incrementada de preparaciones del isómero S-(þ)- puro puede ayudar a incrementar su popularidad.
REFERENCIAS
- Kurdi MS, Theerth KA, Deva RS. Ketamine: current applications in anesthesia, pain and critical care. Anesth Essays Res. 2014;8(3):283-290.
- Ori C, Freo U, Merico A, et al. Effects of ketamine-enantiomers anesthesia on local glucose utilization in the rat. Anesthesiology. 1999;91(3A)A772.
- Kawasaki T, Ogata M, Kawasaki C, et al. Ketamine suppresses pro-inflammatory cytokine production in human whole blood in vitro. Anesth Analg. 1999;89(3):665-669.
- Marland S, Ellerton J. Ketamine: use in anesthesia. Review. CNS Neurosci Ther. 2013;19(6):381-389.
- Luft AN, Mendes FF. Low S(þ) ketamine doses: a review. Rev. Bras. Anestesiol. 2005;55 (4):460-469.
- Best W, Bodenschatz C, Beran D. World Health Organisation Critical Review of Ketamine. 36th WHO Expert Committee on Drug Dependence report, 6.2. Geneva, Switzerland: World Health Organisation. 2014.
- Dolansky G, Shah A, Mosdossy G, Rieder M. What is the evidence for the safety and efficacy of using ketamine in children? Paediatr Child Health. 2008;13(4):307-308.
- Pai A, Heining M. Ketamine. Cont Educ Anesth Crit Care Pain: CEACCP 2007;7(2):59-63.
- Heinz P, Geelhoed GC, Wee C, Pascoe EM. Is atropine needed with ketamine sedation? A prospective, randomised, double blind study. Emerg Med J: EMJ. 2006;23(3):206-209.
- Green SM, Roback MG, Kennedy RM et al. Clinical practice guideline for emergency department ketamine dissociative sedation: 2011 update. Ann Emerg Med. 2011;57(5):449-461.
- Andolfatto G, Abu-Laban RB, Zed PJ, et al. Ketamine propofol combination (ketofol) versus propofol alone for emergency department procedural sedation and analgesia: a randomized double-blind trial. Ann Emerg Med. 2012;59(6):504-512.
- Mosier JM, Joshi R, Hypes C, Pacheco G, Valenzuela T, Sakles JC. The physiologically difficult airway. West J Emerg Med. 2015;16(7):1109-1117.
- Sleigh J, Harvey M, Voss L, Denny B. Ketamine—more mechanisms of action than just NMDA blockade. Trends Anaesth Crit Care. 2014;4(2):76-81.
- Bell RF, Dahl JB, Moore RA, Kalso EA. Perioperative ketamine for acute postoperative pain. Cochrane Database Syst Rev. 2006;Jan 25(1):CD004603.
- Guillou N, Tanguy M, Seguin P, et al. The effects of small-dose ketamine on morphine consumption in surgical intensive care unit patients after major abdominal surgery. Anesth Analg. 2003;97(3):843-847.
- Bowers KJ, McAllister KB, Ray M, Heitz C. Ketamine as an adjunct to opioids for acute pain in the emergency department: a randomized controlled trial. Acad Emerg Med. 2017;24(6):676-685.
- Gorlin AW, Rosenfeld DM, Ramakrishna H. Intravenous sub-anesthetic ketamine for perioperative analgesia. J Anaesthesiol Clin Pharmacol. 2016;32(2):160-167.
- McNicol ED, Schumann R, Haroutounian S. A systematic review and meta-analysis of ketamine for the prevention of persistent post-surgical pain. Acta Anaesthesiol Scand. 2014;58(10):1199-213.
- Goyal S, Agrawal A. Ketamine in status asthmaticus: a review. Ind J Critl Care Med. 2013;17(3):154-161.
- Hamimy W, Abdelaal A. The application of a new regimen for short term sedation in ICU (ketofol)—case series. Egypt J Anaesth. 2012;28(3):179-182.
- Jabre P, Combes X, Lapostolle F, et al. Etomidate versus ketamine for rapid sequence intubation in acutely ill patients: a multicentre randomised controlled trial. Lancet. 2009;374(9686):293-300.
- Yoon SH. Concerns of the anesthesiologist: anesthetic induction in severe sepsis or septic shock patients. Korean J Anesthesiol. 2012;63(1):3-10.
- Bar JG, Guilburd Y, Guilburd J. Ketamine effectively prevents intracranial pressure elevation during endotracheal suctioning and other distressing interventions in patients with severe traumatic brain injury. Crit Care Med. 2009;37(12):A402.
- Zeiler FA, Teitelbaum J, West M, et al. The ketamine effect on ICP in traumatic brain injury. Neurocrit Care. 2014;21(1):163-173.
- Joint Formulary Committee. British National Formulary. http://www.medicinescomplete.com. Accessed October 26, 2017.
- Dong TT, Mellin-Olsen J, Gelb AW. Ketamine: a growing global health-care need. Br J Anaesth. 2015;115(4):491-493.
- Green SM, Clem, KJ, Rothrock SG. Ketamine safety profile in the developing world. Acad Emerg Med. 1996;3(6):598- 604.
- Craven R, Alkhafaji R. Ketamine in Anaesthetic Practice, ATOTW 27. World Anaesthesia Tutorial of the week. 2006.
- Poonai N, Canton K, Ali S, et al. Intranasal ketamine for procedural sedation and analgesia in children: A systematic review. Ma Z-L, ed. PLoS ONE. 2017;12(3)



