Basic Sciences
Points clés
- La vasopressine, un nonapeptide endogène, est une hormone neuroendocrine impliquée dans l’homéostasie de l’osmolalité sérique et de la tension artérielle. Elle exerce ses effets par la vasoconstriction et l’augmentation de la réabsorption d’eau au niveau rénal.
- Chez le patient en choc septique, une perfusion continue de vasopressine est recommandée, dans le document Surviving Sepsis Guidelines (2016), en tant que vasopresseur de seconde ligne pour augmenter la tension artérielle et réduire les besoins en noradrénaline.
- La preuve de son efficacité dans le choc septique n’est pas clairement démontrée mais elle pourrait se montrer bénéfique dans certains sous-groupes de patients.
- La terlipressine et la desmopressine sont deux analogues de la vasopressine utilisés dans le traitement des hémorragies de varices œsophagiennes, dans celui du diabète insipide d’origine centrale de même que chez le patient hémophile ou dans la maladie de von Willebrand.
Introduction
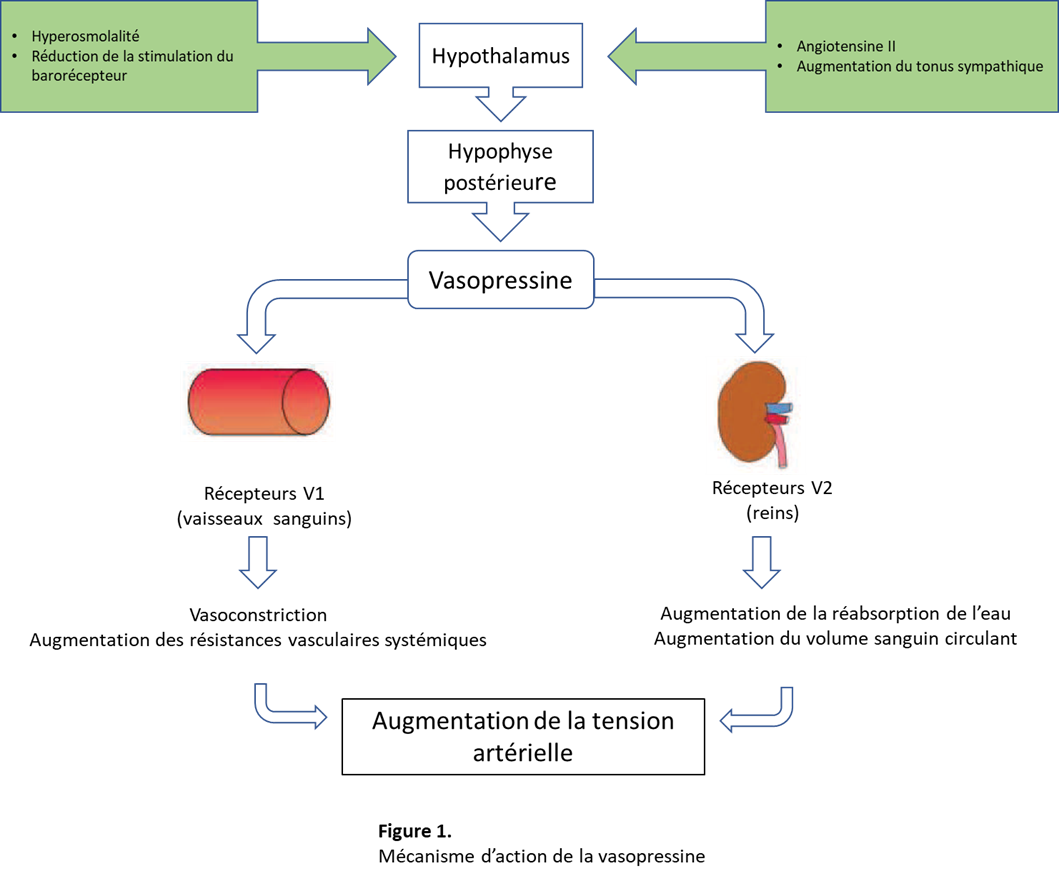
La vasopressine, encore appelée hormone anti-diurétique ou arginine vasopressine, est une hormone endogène impliquée dans l’homéostasie de l’osmolalité sérique et de la tension artérielle. Elle est secrétée par l’hypophyse postérieure et agit sur différents types de récepteurs. Dans des conditions physiologiques, son effet prédominant est d’augmenter la réabsorption de l’eau au niveau des tubes collecteurs du rein, ce qui induit une réduction de l’osmolalité sérique et une augmentation du volume sanguin circulant.1 La figure 1 illustre le mécanisme de cet effet. Existent également d’autres sous-types de récepteurs responsables d’effets physiologiques différents dont une puissante vasoconstriction. Ces derniers représentent une cible potentielle pour les applications cliniques.
La prise en charge du choc septique est une de ces applications cliniques potentielles. La vasoconstriction induite par la vasopressine n’est pas médiée par les catécholamines ce qui en soit représente une option thérapeutique supplémentaire chez ce groupe de patients. Les preuves de son efficacité permettant de recommander son utilisation restent équivoques. L’étude VAAST(2008)2 représente le premier essai clinique contrôlé randomisé étudiant les effets de la vasopressine. Elle a démontré un effet significatif d’épargne sur les besoins en noradrénaline mais n’a pas fait la preuve d’une réduction de la mortalité. Des études ultérieures, dont l’essai VANISH (2016)3 et l’importante méta-analyse de Nagendran et al (2019)4, réalisée à partir des données individuelles des patients, n’ont pas non plus permis de montrer une amélioration des taux de mortalité chez ce groupe de patients mais pourraient avoir fait la preuve d’un effet bénéfique sur d’autres paramètres cliniques.
Ce tutoriel couvre les aspects scientifiques élémentaires de la vasopressine de même que ses effets chez le sujet sain et en situation pathologique. Sa pharmacodynamie et ses applications cliniques sont passées en revue, en ce compris l’état actuel des connaissances qui justifient son utilisation.
Effets physiologiques chez le sujet sain
L’organisme régule très précisément l’osmolalité sérique qu’il maintient entre 275 to 295 mmol/kg. Cette dernière, exprimée en mmol/kg, représente le nombre total de particules dissoutes dans un kilogramme de solvant. Le volume total d’eau corporelle est directement lié à l’osmolalité en raison de la perméabilité à l’eau des membranes cellulaires. La soif, et l’apport en eau qui y est associé, l’excrétion de particules participant à l’osmolalité et la vasopressine, représentent les mécanismes principaux impliqués dans la régulation de l’osmolalité sérique.
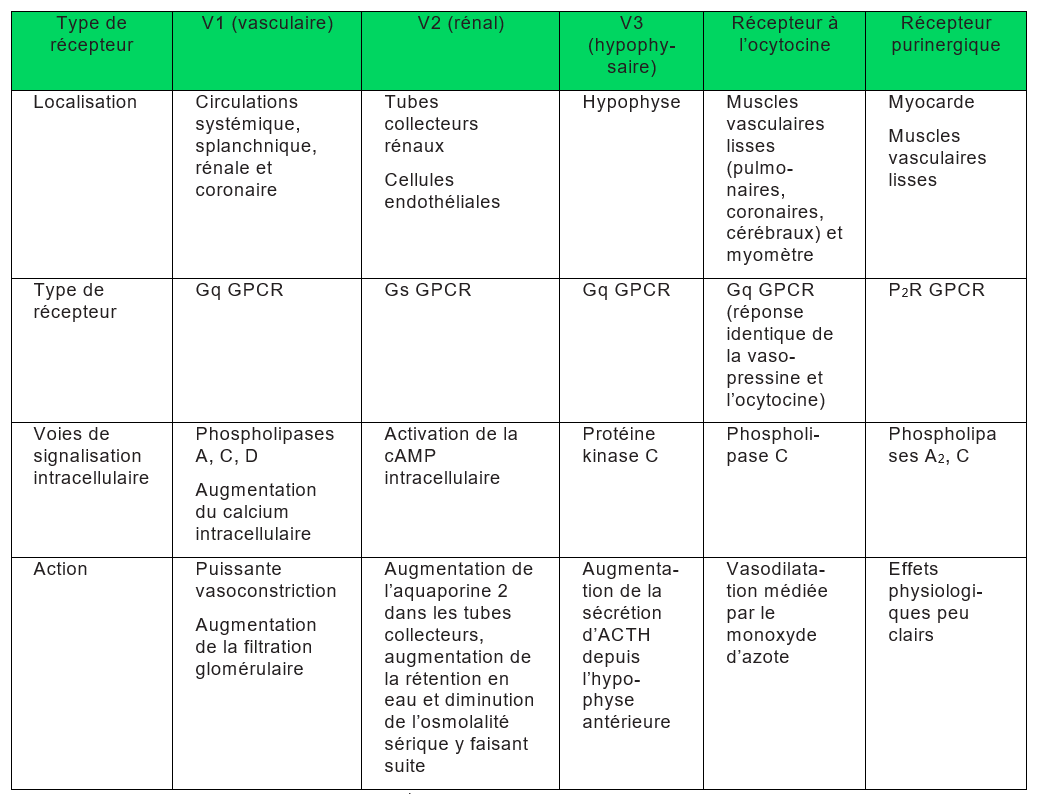
La vasopressine, nonapeptide court, est une hormone neuroendocrinienne produite par des neurones magnocellulaires des noyaux supra-optique et paraventriculaire de l’hypothalamus. Elle est acheminée dans l’infundibulum par les axones correspondants pour être stockée ensuite au sein de l’hypophyse postérieure. En réponse à une augmentation de l’osmolalité sérique, la vasopressine est libérée dans la circulation sanguine à partir de cette même hypophyse postérieure. Sa libération est aussi induite par la stimulation su système sympathique, par une réduction de l’activité des barorécepteurs et par l’action de l’angiotensine II.1,5 Les récepteurs via lesquels elle exerce ses effets de même que leurs mécanismes d’action sont illustrés dans le tableau 1.
Pharmacocinétique
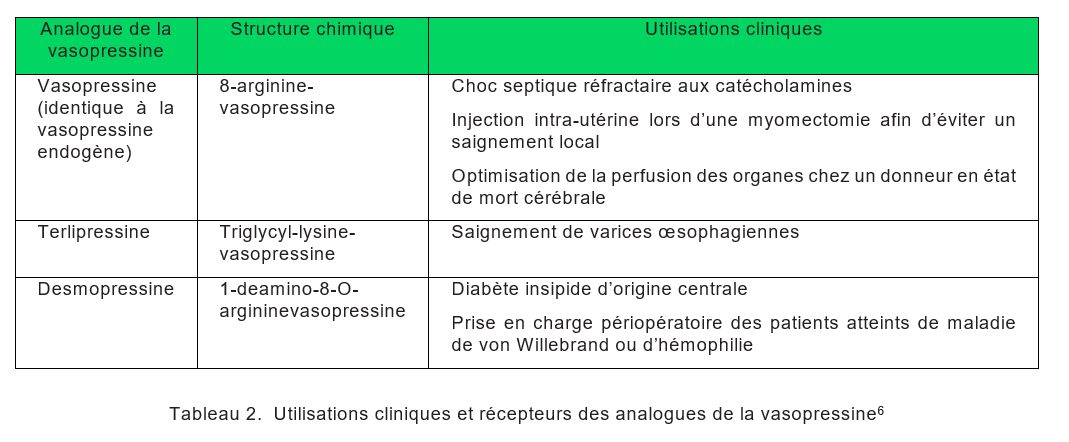
Trois analogues synthétiques de la vasopressine sont disponibles en clinique. Le tableau 2 reprend les utilisations cliniques et les récepteurs de ces analogues.
Absorption
La desmopressine est le seul analogue de la vasopressine qui ne nécessite pas une administration intraveineuse. L’absorption par voie sublinguale est de 0.25%, par voie orale de 0.08 à 0.16% et par voie intranasale de 10%.
Distribution
La vasopressine et ses analogues ont un faible volume de distribution. Ce dernier pour la vasopressine, la terlipressine et la desmopressine est de 0.14 L/Kg, 0.5 L/Kg et de 0.2 à 0.32 L/Kg respectivement. La vasopressine ne se lie pas aux protéines.
Métabolisme
La vasopressine endogène est métabolisée par les vasopressinases hépatiques et a une demi-vie de 10 à 35 minutes. La terlipressine, quant à elle, a une demi-vie de 50 à 70 minutes et, suite à une dégradation enzymatique minime, celle de la desmopressine est encore plus longue, se situant entre 2 et 3 heures.
Excrétion
Soixante-cinq pour cent d’une dose de vasopressine ou de desmopressine administrée est excrétée sous forme inchangée dans les urines.6
|
Tableau 1. Récepteurs à la vasopressine1 (ACTH : hormone adrénocorticotropique, GPCR, récepteur couplé à une protéine G) |
Effets secondaires
Le tableau 3 reprend les effets secondaires principaux observés lors de l’utilisation de la vasopressine ou de ses analogues.
Applications cliniques
La vasopressine dans le choc septique réfractaire aux catécholamines
Le document Surviving Sepsis Guidelines (2016)8 fait état des recommandations dont l’efficacité dans la prise en charge du sepsis a été démontrée sur base d’études. Ces recommandations concernent le remplissage liquidien, l’antibiothérapie et l’utilisation des vasopresseurs. La noradrénaline est actuellement l’agent de première intention dans ces recommandations. La vasopressine quant à elle est recommandée en second ligne, en cas de résistance aux catécholamines. Les recommandations telles qu’énoncées dans le document sont les suivantes: « À la noradrénaline, nous suggérons l’ajout de la vasopressine jusqu’à 0.03 U/min (recommandation basée sur un niveau de preuve scientifique modéré) ou de l’adrénaline (recommandation basée sur un faible niveau de preuve scientifique) dans l’intention d’augmenter la pression artérielle moyenne (PAM) jusqu’à la valeur cible, ou l’ajout de la vasopressine jusqu’à 0.03 U/min (recommandation basée sur un niveau de preuve scientifique modéré) dans l’intention de réduire la dose the noradrénaline utilisée.».

En pratique clinique, on constate souvent l’utilisation d’une dose de 0.01 à 0.04 U/min.6 L’utilisation de doses plus élevées a été associée à des taux accrus d’ischémie des membres et des extrémités ainsi que d’ischémie mésentérique. Il n’y a pas de recommandations claires quant au moment auquel la vasopressine doit être commencée dans le choc septique réfractaire aux catécholamines. L’instauration de la vasopressine est aussi fonction de l’interprétation que fait le clinicien de ce qu’est une situation de choc réfractaire aux catécholamines.
Il a été démontré que les taux de vasopressine dans le choc septique étaient plus bas que ce qui était attendu. L’expression de déficit relatif en vasopressine est utilisée pour décrire cette observation.9 L’explication de ce taux bas de même que sa signification clinique n’est pas élucidée. L’étude clinique contrôlée randomisée VASST, comparant la noradrénaline et la noradrénaline avec de la vasopressine à une dose de 0.03 U/min chez les patients en choc septique, n’a pas montré de différence entre les groupes en terme de pronostic.2 Une analyse en sous-groupes a cependant démontré que les patients sous noradrénaline à une dose inférieure 15 µg/min avec ajout de vasopressine avaient un taux de survie plus élevé.
Dans l’étude VANISH3 ont été inclus 409 patients en choc septique randomisés pour être traités soit avec de la vasopressine (avec de l’hydrocortisone ou un placebo) ou de la noradrénaline (avec de l’hydrocortisone ou un placebo). À nouveau, aucune amélioration ne fut démontrée sur la mortalité mais une réduction du recourt à l’ épu-ration extra-rénale fut démontrée dans le groupe recevant de la vasopressine. Cela s’explique potentiellement par son effet préférentiel de vasoconstriction de l’artériole glomérulaire efférente par rapport à l’artériole afférente, ceci conduisant à une augmentation de la pression glomérulaire.
Une méta-analyse incluant 9 études et un total de 1324 patients a confirmé l’incertitude à démontrer un bénéfice en terme de mortalité à partir des données qui existent.4 Alors que la plupart des études montrent un effet d’épargne sur les besoins en catécholamines, la preuve d’effets bénéfiques sur la mortalité et la morbidité n’a pu être établie. Les recommandations faites sont donc basées sur un faible niveau de preuve et d’importantes variations sont constatées entre les pratiques cliniques.
La vasopressine dans l’arrêt cardiaque
Un intérêt pour la vasopressine s’est développé dans la prise en charge de l’arrêt cardiaque ce qui a conduit à plusieurs essais cliniques contrôlés randomisés. Une revue Cochrane de 26 études de la sorte, totalisant 21 704 patients, s’est penchée sur l’utilisation de l’adrénaline, de la vasopressine ou d’une combinaison des deux chez les patients victimes d’un arrêt cardiaque extra-hospitalier ou intra-hospitalier. Par comparaison avec l’adrénaline à hautes-doses en tant qu’agent unique, l’utilisation de la vasopressine seule ou en conjonction avec l’adrénaline n’a pas démontré de bénéfice sur le retour à une circulation spontanée ni sur la survie à l’arrivée à l’hôpital ou sur la survie avec un pronostique neurologique favorable. En cela, il n’y a donc pas à l’heure actuelle de niveau de preuve adéquat permettant de recommander l’utilisation de la vasopressine.10 C’est suite à cela que la vasopressine a été retirée en 2015 des recommandations de l’Advanced Cardiac Life Support (ACLS) dans l’arrêt cardiaque.
La vasopressine en chirurgie
Le facteur de von Willebrand est une glycoprotéine de grande taille impliquée dans l’hémostase. Elle est nécessaire à l’adhésion plaquettaire et joue un rôle de pont entre le sous-endothélium endommagé et les plaquettes activées. Il joue également un rôle inhibiteur sur la dégradation du facteur VIII, ce qui en soit favorise l’hémostase.11 Par leur effet sur les récepteurs endothéliaux V2 qui activent la voie de l’AMP cyclique, la vasopressine et la desmopressine activent, jusqu’à 5 fois, la libération du facteur de von Willebrand.12 C’est la raison pour laquelle la desmopressine est utilisée dans la prise en charge périopératoire des patients atteints de maladie de von Willebrand ou d’hémophilie A. Il est important de noter que, dans certains types de maladie de von Willebrand (type IIb), le taux de plaquettes peut paradoxalement chuter à la suite de l’administration de desmopressine. Il peut donc être nécessaire de contrôler le taux de plaquettes en pré-opératoire afin d’évaluer la réponse à l’administration de desmopressine. Les doses nécessaires dans cette indication sont jusqu’à 15 fois supérieures à celles utilisées dans le diabète insipide.
La vasopressine est aussi utilisée en cas de myomectomie ou d’autres procédures chirurgicales sur l’utérus. La vasoconstriction faisant suite à son injection intra-utérine directe réduit le saignement local mais induit également fréquemment une augmentation correspondante de la tension artérielle dont il est important que l’anesthésiste soit informé.
La vasopressine dans le don d’organe
Une dysrégulation hormonale profonde est présente chez le sujet en état de mort cérébrale à la suite d’intenses perturbations physiologiques. On constate une augmentation du taux de catécholamines et une diminution de celui du cortisol, de la vasopressine, de l’insuline et des hormones thyroïdiennes. Chez les sujets en état de mort cérébrale potentiellement donneurs d’organes, on tente dès lors de minimiser les effets délétères que ces perturbations peuvent provoquer. Les experts en transplantation peuvent donc recommander l’utilisation de la vasopressine chez ces patients dans le but d’améliorer la fonction des organes transplantés et en cela le pronostic des patients. L’utilisation de la vasopressine est souvent conseillée même en l’absence de diabète insipide. Malgré la logique derrière son utilisation, le niveau de preuve est faible et essentiellement basé sur des opinions d’experts. C’est pour cette raison que les recommandations à son utilisation varient au niveau local et qu’il est nécessaire de faire appel à l’avis des experts en transplantation.13
La terlipressine dans le saignement des varices œsophagiennes
Le saignement sur varices œsophagiennes est une complication potentiellement mortelle de l’hypertension portale. Des veines sous-muqueuses du tiers inférieur de l’œsophage se dilatent de façon importante à la suite de l’augmentation de pression portale. Elles peuvent alors saigner profusément dans la lumière œsophagienne. La terlipressine a un rôle bénéfique chez ces patients par son effet agoniste sur les récepteurs V1.14 La vasoconstriction splanchnique induite réduit la pression veineuse portale et en cela réduit la pression dans les varices œsophagiennes. Suite à cette diminution du saignement, davantage de temps peut être consacré à la stabilisation initiale du patient avec ensuite traitement définitif par voie endoscopique.
Une méta-analyse de 201815 portant sur 3344 patients, inclus dans un total de 34 essais cliniques contrôlés randomisés, a montré que la terlipressine améliorait de façon significative le contrôle du saignement dans les 48 heures, réduisait la mortalité intra-hospitalière, diminuait le risque de complications par rapport à la vasopressine et aboutissait à une amélioration supplémentaire du pronostic lorsqu’elle était combinée à la ligature endoscopique des varices.
Au Royaume-Uni, on recommande l’administration d’une dose intraveineuse de 2 mg toutes les 4 heures jusqu’au contrôle du saignement, réduite à 1 mg toutes les 4 heures si nécessaire jusqu’à un maximum de 48 heures.7 Les firmes pharmaceutiques recommandent une réduction de la dose chez les patients de faible poids corporel. Il est important de suivre les recommandations établies au niveau local.
La desmopressine dans le diabète insipide d’origine centrale
Le diabète insipide d’origine centrale se caractérise par l’incapacité à sécréter de la vasopressine endogène ce qui induit polyurie, polydipsie et nycturie. Hypovolémie, déshydratation et perturbations électrolytiques s’ensuivent en l’absence de traitement à cause de l’impossibilité pour l’organisme de maintenir une balance hydrique adéquate. Les causes de diabète insipide d’origine centrale peuvent être une intervention chirurgicale, un trauma crânien, une infection, une pathologie tumorale ou encore une maladie héréditaire.16
La vasopressine fut utilisée pour la première fois dans le traitement du diabète insipide en 1913 sous la forme d’extraits provenant de l’hypophyse postérieure qui contenaient de la vasopressine et de l’ocytocine. Ce n’est qu’au cours des années 70 que la desmopressine fut utilisée, cette dernière conférant beaucoup d’avantages par rapport à la vasopressine. Par comparaison à la vasopressine, la desmopressine a des effets vasoconstricteurs moindres mais a une action antidiurétique plus prononcée. Ces caractéristiques, en plus d’une durée d’action plus longue, de la possibilité de prise par voie orale et d’effets secondaires moindres, font de la desmopressine une option thérapeutique supérieure.16 Chez l’adulte, la prise par voie orale, administrée en 3 doses, peut varier de 0.2 à 1.2 mg par jour. Les doses intraveineuse, sublinguale et intranasale varient en fonction de leur profil pharmacocinétique.7
En résumé
La vasopressine est une hormone endogène ayant des rôles importants dans l’homéostasie liquidienne et la régulation de la tension artérielle. Elle a plusieurs indications cliniques suites à ses nombreux effets physiologiques dont ceux affectant le système cardiovasculaire, la balance liquidienne et l’homéostasie. Son utilisation dans le choc septique réfractaire aux catécholamines est reconnue mais les preuves scientifiques de ses avantages sont limitées. Elle représente cependant une nouvelle option thérapeutique dans ce groupe de patients car elle n’est pas dépendante de l’action du système sympathique.
Références
- Holmes CL, Landry DW, Granton JT. Science review: vasopressin and the cardiovascular system part 1—receptor physiology. Crit Care. 2003;7(6):427-434.
- Russell JA, Walley KR, Singer J, et al. Vasopressin versus norepinephrine infusion in patients with septic shock. N Engl J Med. 2008;358(9):877-887.
- Gordon AC, Mason AJ, Thirunavukkarasu N, et al. Effect of early vasopressin vs norepinephrine on kidney failure in patients with septic shock: the VANISH randomized clinical trial. 2016;316(5):509-518.
- Nagendran M, Russell JA, Walley KR, et al. Vasopressin in septic shock: an individual patient data meta-analysis of randomised controlled trials. Intensive Care Med. 2019;45:844-855.
- Danziger J, Zeidel ML. Osmotic homeostasis. Clin J Am Soc Nephrol. 2015;10(5):852-862.
- Smith S, Edwards C, Sasada M. Drugs Used in Anaesthesia and Critical Care. 4th ed. Oxford, UK: Oxford University Press; 2011.
- Kaufmann JE, Oksche A, Wollheim CB, et al. Vasopressin-induced von Willebrand factor secretion from endothelial cells involves V2 receptors and cAMP. J Clin Invest. 2000;106(1):107-116.
- Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis Campaign: international guidelines for management of sepsis and septic shock: 2016. Crit Care Med. 2017;45:486-552.
- Landry DW, Levin HR, Gallant EM, et al. Vasopressin deficiency contributes to the vasodilation of septic shock. 1997;95(5):1122-1125.
- Kalra S, Zargar AH, Jain SM, et al. Diabetes insipidus: the other diabetes. Indian J Endocrinol Metab. 2016;20(1):9-21.
- Zhou X, Tripathi D, Song T, et al. Terlipressin for the treatment of acute variceal bleeding: a systematic review and meta-analysis of randomized controlled trials. Medicine (Baltimore). 2018;97(48):e13437.
- Joint Formulary Committee. British National Formulary. 78th ed. London, UK: BMJ Group and Pharmaceutical Press; 2019.
- Hilzenrat N, Sherker AH. Esophageal varices: pathophysiology, approach, and clinical dilemmas. Int J Hepatol. 2012;2012:795063.
- Finn J, Jacobs I, Williams TA, et al. Adrenaline and vasopressin for cardiac arrest. Cochrane Database Syst Rev. 2019(1):CD003179.
- Peyvandi F, Garagiola I, Baronciani L. Role of von Willebrand factor in the haemostasis. Blood Transfus. 2011;9(2):3-8.
- Hahnenkamp K, Böhler K, Wolters H, et al. Organ-protective intensive care in organ donors. Dtsch Arztebl Int. 2016;113(33-34):552-558.



