Paediatric Anaesthesia
PUNTOS CLAVE
- La fístula traqueo-esofágica (FTE) con o sin atresia esofágica (AE) tiene una incidencia a nivel mundial de 1 en 3000-4000 nacidos vivos, siendo la mayoría de los casos diagnosticados postnatalmente. Hasta un 50% de los infantes tienen otras anomalías congénitas asociadas a la FTE/AE.
- Previo a la reparación quirúrgica, se debe realizar una valoración preoperatoria minuciosa, con especial atención al estado respiratorio y cardiaco del neonato, incluyendo un ecocardiograma para detectar lesiones de cardiopatía congénita.
- Las consideraciones intraoperatorias para la reparación de la FTA/AE incluyen el anticipar dificultades con el manejo de la vía aérea, técnica quirúrgica, potencial pérdida sanguínea y los planes para el manejo posoperatorio.
- Si bien el desenlace en neonatos con FTE/AE ha mejorado significativamente debido a los avances quirúrgicos, en el manejo anestésico y en cuidados intensivos, la tasa de mortalidad sigue siendo alta en entornos de bajos recursos.
INTRODUCCIÓN
La fístula traqueo-esofágica (FTE) con o sin atresia esofágica (AE) es una anomalía congénita con una incidencia de 1 en 3000-4000 nacimientos a nivel mundial.1 Si bien, la FTE se puede presentar de forma aislada, hasta un 50% de los infantes tienen asociado otras anomalías congénitas, siendo la más común la cardiopatía congénita. Además, hasta un 25% de los infantes son diagnosticados con VACTERL (anomalías Vertebrales, Ano imperforado, defectos Cardiacos, fístula Traqueo-Esofágica, agenesia Renal y anomalías de extremidades (Limbs), más frecuentemente displasia del radio). 2 (Ver Figura 1)
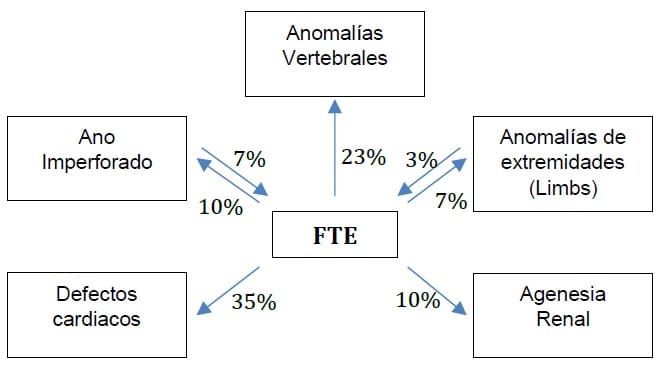
Figura 1. Frecuencia de defectos de síndrome VACTERL y FTE2
Los médicos deben saber que los niños con fístula traqueo-esofágica sindrómica, especialmente aquellos con cardiopatía congénita compleja, van a requerir cirugías adicionales y que su manejo perioperatorio será más complejo. Nuestra capacidad como anestesiólogos para anticipar las dificultades en el manejo preoperatorio, intraoperatorio y posoperatorio juega un papel importante en el tratamiento y supervivencia de estos niños.
Anatomía de la fístula traqueo-esofágica
Durante la cuarta semana de vida embrionaria, la tráquea se diferencia del esófago. Si hay una separación incompleta de la tráquea del piso del intestino anterior, se presentan las malformaciones traqueo-esofágicas. De acuerdo al sistema de clasificación de Gross, hay seis variantes anatómicas de la FTE con y sin AE (Tipos A-F, Figura 2).3 En la Tipo C, la cual es la lesión más común y se da en más del 90% de los casos, existe una fístula entre la tráquea y el segmento esofágico inferior, por debajo de la carina, mientras que el saco esofágico superior tiene una terminación ciega en el mediastino.3
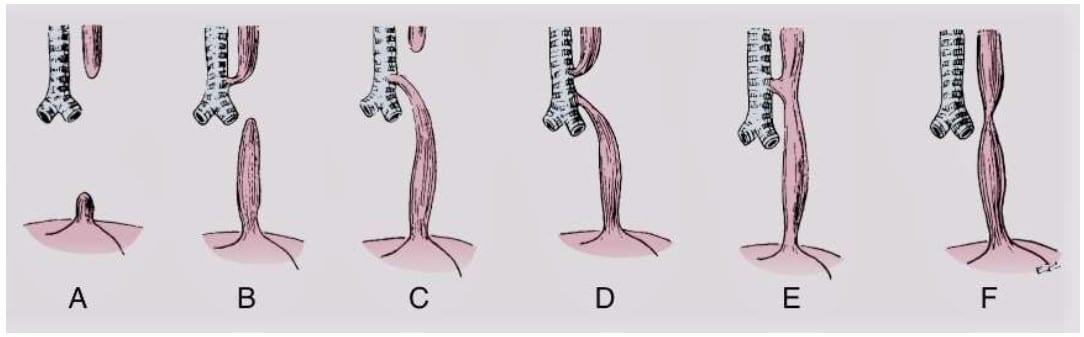
Figura 2. Variantes de la FTE con y sin AE3. Reproducido con permiso de Elsevier.
Diagnóstico
A diferencia de muchas otras anomalías congénitas, la FTE no se diagnostica fácilmente prenatalmente. El hallazgo ultrasonográfico más comúnmente asociado a FTE/AE es el polihidramnios secundario a la obstrucción esofágica e incapacidad para deglutir el líquido amniótico. Sin embargo, el polihidramnios es un signo inespecífico y es causado por anomalías congénitas en menos del 20% de los casos.3 Como resultado, los casos de FTE/AE, tanto en entornos de altos y bajos recursos, son diagnosticados postnatalmente cuando los pacientes se presentan con salivación excesiva y asfixia con la alimentación. Para confirmar la presencia de AE, se inserta un catéter de succión al neonato, ya sea por vía oral o nasal, y el catéter no se logra introducir más de 10 cm en el esófago. El diagnóstico puede ser confirmado con una radiografía de tórax, la cual muestra el catéter en el saco ciego superior (Figura 3).
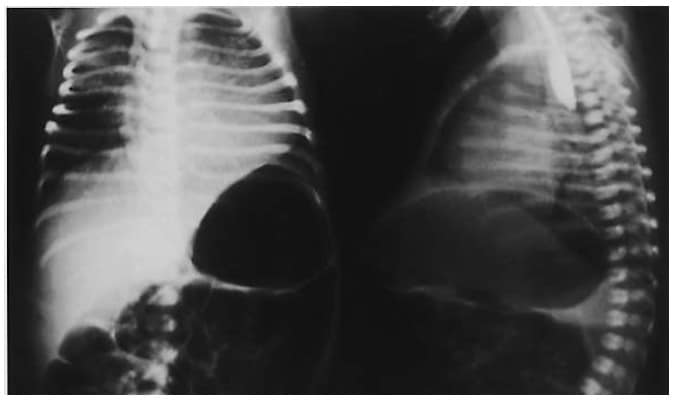
Figura 3. Lesión Tipo C con distensión gástrica. Esófago con terminación ciega en la proyección lateral. Reproducido con permiso de Elsevier.3
En los entornos de bajos recursos, los pacientes son referidos de clínicas periféricas hacia un centro de salud de tercer nivel para el tratamiento definitivo, esto puede tomar varios días. Este periodo de tiempo se asocia de manera frecuente con aspiración, neumonía y en ocasiones con sepsis.4 Dependiendo de la condición física del neonato al llegar al centro de salud de tercer nivel, no es infrecuente que la reparación quirúrgica se retrase desde 3 días hasta 2 semanas luego del nacimiento. Idealmente, durante este periodo, se coloca una sonda nasogástrica en el saco esofágico superior y se succiona de forma intermitente utilizando una baja presión de succión. Se corrigen los trastornos hidroelectrolíticos y se maneja la sepsis con antibióticos. Previo a la reparación definitiva, especialmente en presencia de anatomía compleja, en ocasiones es necesario realizar una esofagostomía cervical para drenar el saco esofágico superior y colocar un tubo de gastrostomía para alimentación enteral.4 La reparación definitiva se realiza posteriormente, cuando la condición del neonato se haya estabilizado.
VALORACIÓN PREOPERATORIA
No es infrecuente que los neonatos con FTE se presenten con complicaciones respiratorias, ya que son propensos a la aspiración. La radiografía de tórax puede mostrar infiltrados. La prevención y/o el tratamiento de las complicaciones pulmonares son primordiales para reducir la morbimortalidad. Para minimizar el riesgo de desarrollar neumonitis por aspiración, se llevan a cabo las siguientes intervenciones: nada vía oral (NPO), se mantiene al neonato en posición vertical, y se realiza una succión intermitente del saco esofágico superior para disminuir el acúmulo de saliva.
Una valoración preoperatoria minuciosa debe enfocarse en determinar la presencia de cualquier anomalía congénita preexistente, especialmente defectos cardiacos, y valorar cualquier posible implicación anestésica. La alta prevalencia de cardiopatía congénita hace que el ecocardiograma preoperatorio sea una necesidad. Defectos cardiacos tales como el defecto del septum ventricular, defecto del septum atrial y la tetralogía de Fallot se asocian de manera común a la FTE, y esto tiene un impacto sobre el manejo anestésico. Además, un ecocardiograma puede revelar anomalías del arco aórtico, lo cual afecta la técnica quirúrgica. Se ha reportado que hasta un 5% de los pacientes tienen un arco aórtico derecho, requiriendo una toracotomía izquierda.5
Si bien la valoración respiratoria y cardiaca preoperatoria es esencial, si un neonato tiene cualquier anomalía VACTERL, se deben realizar pruebas diagnósticas para valorar la presencia de anomalías coexistentes. Si hay presencia de un hoyuelo sacro es beneficioso obtener un ultrasonido lumbar para evaluar la anatomía neuroaxial, especialmente si se planea colocar un catéter epidural caudal para analgesia posoperatoria. Adicionalmente, se debería obtener un ultrasonido renal para descartar hidronefrosis u otras anomalías renales, las cuales podrían afectar el manejo anestésico.
MANEJO INTRAOPERATORIO
Previo a la reparación quirúrgica, se debe desarrollar un plan intraoperatorio detallado, el cual tome en cuenta la técnica quirúrgica, el manejo de vía aérea y la potencial pérdida sanguínea.
Técnica quirúrgica
Hay dos abordajes principales para la reparación de la FTE/AE; el abordaje quirúrgico tradicional por medio de una toracotomía abierta y el abordaje con toracoscopia. La toracoscopia es mínimamente invasiva y se realiza utilizando pequeñas cámaras de fibra óptica por cirujanos con entrenamiento especial en esta técnica. La principal ventaja de la toracoscopia es la reducción en las secuelas musculo-esqueléticas, como la escápula “alada”. Sin embargo, debido a la compresión pulmonar ipsilateral por el neumotórax quirúrgico para obtener un adecuado espacio de trabajo, es común la desaturación y la disminución del retorno venoso por la compresión directa de estructuras vasculares, tales como la vena cava inferior y el atrio derecho. La absorción de dióxido de carbono puede producir hipercapnia y acidosis, lo cual puede ser mal tolerado por los neonatos.
Para la técnica abierta, la cual es la técnica de elección en países en vías de desarrollo (debido a que no se cuenta con equipo o entrenamiento para la reparación por toracoscopia) el paciente se coloca en la posición de decúbito lateral. Usualmente, el neonato se coloca en la posición de decúbito lateral izquierdo para el abordaje con toracotomía derecha, a menos de que haya evidencia de la presencia de un arco aórtico derecho, en cuyo caso se realiza una toracotomía izquierda. Una reparación abierta total se puede lograr como un procedimiento de una sola etapa, donde se liga la fístula y se hace una anastomosis primaria del esófago. Si la fístula se encuentra a nivel de la carina, puede ser necesario la ventilación a un solo pulmón, predisponiendo al infante a hipoxemia, hipercapnia y a desarrollar un incremento en la resistencia vascular pulmonar. El pulmón debe ser re-expandido de manera cuidadosa para eliminar atelectasias previo al cierre.
Manejo Anestésico
El manejo anestésico en la sala de operaciones debe incluir monitoreo de rutina (ECG, Presión arterial, ETCO2, sonda de temperatura y un oximetro de pulso a menos que exista una lesión cardíaca ductus-dependiente, en cuyo caso se necesitan dos oximetros de pulso para medir la saturación pre y post-ductal). Si está disponible, es de utilidad colocar una línea arterial, para monitoreo hemodinámico continuo y análisis de gases arteriales. Preferiblemente, la línea arterial se coloca en la extremidad superior izquierda, ya que el brazo derecho se encuentra elevado y tiene acceso limitado durante la toracotomía derecha. Se deben colocar al menos dos vías intravenosas periféricas, y debe haber sangre cruzada disponible en la sala de operaciones. Si existe una alta probabilidad de requerir nutrición parenteral en el posoperatorio, se debe colocar un catéter venoso central.
El objetivo durante la inducción es intubar al infante minimizando la distensión gástrica. Si no se toman medidas para evitar la distensión gástrica, puede hacer muy difícil, si no es que imposible la ventilación y esto puede conducir a un colapso hemodinámico. Hay varias maneras de asegurar la vía aérea. El abordaje conservador implica la intubación despierto para evitar la ventilación por presión positiva con bolsa-mascarilla; sin embargo, se debe prestar atención a la posibilidad de un aumento de la presión intracraneal o de hemorragia intraventricular en los prematuros. Otra técnica es la inducción de anestesia general con agentes inhalados mientras se mantiene la ventilación espontánea y que luego el cirujano realice una broncoscopia rígida. El papel de la broncoscopia es determinar la localización exacta y el tamaño de la fístula, así como ayudar con la colocación del tubo endotraqueal distal a la fístula pero por encima de la carina.2,3 Si está disponible la broncoscopia de fibra óptica luego de la colocación del tubo endotraqueal, se puede usar para colocar correctamente el tubo endotraqueal. Se identifica la carina y se retrae el tubo endotraqueal (con el fibrobroncoscopio dentro del tubo endotraqueal) hasta que se visualice la fístula y luego se avanza el tubo endotraqueal apenas distal a la fístula. La colocación del tubo endotraqueal puede ser difícil, especialmente cuando la FTE se encuentra a nivel de la carina. En estos casos, se puede colocar un catéter de Fogarty dentro de la fístula y al inflar el balón del catéter ayuda a prevenir la distensión gástrica y la ventilación inadvertida a través de la fístula.
Una vez colocado, hay varias maneras de confirmar la correcta colocación del tubo endotraqueal, justo distal a la fístula:
- Auscultación de ruidos respiratorios.
- Intubación de bronquio principal derecho (o izquierdo) con retirada gradual hasta establecer ventilación bilateral, idealmente 1 cm por encima de la carina.
- Radiografía de tórax.
- Ultrasonido.
- Si hay una gastrostomía, burbujeo o ausencia de esto cuando el tubo está por encima o por debajo de la comunicación de la fístula.
En la actualidad, la necesidad para gastrostomías varía dependiendo en los recursos del entorno. En países desarrollados las gastrostomías no se realizan de forma rutinaria debido a que gas de la tráquea puede omitir los pulmones y salirse a través del estómago, causando una pérdida de la ventilación efectiva. En entornos de bajos recursos, donde puede no estar disponible la broncoscopia, el cirujano realiza de manera rutinaria la gastrostomía, esto posterior a la inducción inhalada con respiración espontánea. Esto se sigue con la intubación endotraqueal con una técnica inhalatoria profunda o usando una técnica con relajantes musculares y ventilación manual cuidadosa. La gastrostomía inicial permite la salida de gas, evitando así la distensión gástrica y minimizando el riesgo de aspiración.
Una vez que se asegura la vía aérea y se ha obtenido un acceso intravenoso y arterial adecuado, el paciente se coloca en la posición de decúbito lateral y se acolchonan los puntos de presión. El mantenimiento de una adecuada oxigenación puede ser un gran problema en el intraoperatorio. El acúmulo de sangre o secreciones en el tubo endotraqueal puede conducir a obstrucción de la vía aérea, requiriendo succión traqueal frecuente. La manipulación quirúrgica de la vía aérea y el colapso del lóbulo pulmonar superior debido al uso de retractores puede causar episodios de hipoxemia. La comunicación estrecha con el equipo quirúrgico es de suma importancia, y el equipo para intubación debe estar fácilmente disponible, esto en caso de una extubación accidental o necesidad para una re-intubación urgente.
CONSIDERACIONES POSOPERATORIAS
Luego de la reparación quirúrgica de la FTE por medio de toracotomía, los neonatos de término sin comorbilidades pueden ser extubados en el posoperatorio. Los infantes con otras anomalías congénitas o que requieran reparaciones más complejas de la FTE puede requerir permanecer intubados en el posoperatorio por algunos días en la unidad de cuidados intensivos neonatales. Se utiliza un catéter nasofaríngeo para succión, y este debe sujetarse con esparadrapo o suturarse para prevenir que se inserte más allá del sitio de la anastomosis esofágica.
En entornos de bajos recursos, los pacientes usualmente se manejan en la unidad general de cuidados intensivos, ya que usualmente no se cuenta con una unidad de cuidados intensivos neonatales.6 La ventilación en el posoperatorio usualmente se realiza con un ventilador versátil adaptado para neonatos y no específicamente con un ventilador neonatal. Esto plantea múltiples desafíos en cuanto a la configuración del ventilador para una ventilación adecuada. El desafío para la ventilación adecuada puede agravarse por la disponibilidad inconstante para medición de gases arteriales y por personal de enfermería sin entrenamiento en cuidados intensivos neonatales.
Las técnicas de anestesia regional como la epidural caudal ha sido utilizada para el manejo del dolor, pero en la mayoría de lugares la analgesia posoperatoria se mantiene con opioides y paracetamol. En algunos países en vías de desarrollo, el cirujano realiza el bloqueo de nervios intercostales.
Complicaciones posoperatorias
Si bien el desenlace de los neonatos con FTE/AE ha mejorado significativamente debido a los avances en el manejo quirúrgico, anestésico y de cuidados intensivos, las complicaciones posoperatorias todavía son comunes. Las complicaciones posoperatorias tempranas incluyen estenosis esofágicas y fugas anastomóticas. Algunas fugas pueden requerir manejo quirúrgico si no cierran espontáneamente. Las estenosis esofágicas pueden requerir múltiples dilataciones con globo, pero la mayoría de estenosis tempranas responden con 2 o 3 dilataciones. Luego de la reparación de una FTE, es recomendado el seguimiento endoscópico por tres años. Si hay signos de esofagitis, el seguimiento se extiende por otros tres años y se obtienen biopsias para determinar si hay esófago de Barrett, una lesión precancerosa.7
El reflujo gastroesofágico persistente es probablemente el problema más frecuente a largo plazo y ocurre mayor frecuencia cuando la reparación primaria fue tardía. Si los síntomas gastroesofágicos son severos, puede ser necesaria la intervención quirúrgica con una funduplicatura de Nissen. Además, muchos pacientes con FTE/AE tienen dismotilidad esofágica, lo cual puede conducir a desarrollar obstrucción esofágica y falla para progresar.
Una complicación más rara, pero que puede definir el desenlace a largo plazo luego de la reparación de la FTE/AE es la traqueomalacia. La traqueomalacia puede causar un colapso de la vía aérea, produciendo estridor, apnea o neumonía recurrente. La traqueomalacia tiende a mejorar después de los primeros 3 a 5 años de vida, pero si es severa puede requerir tratamiento quirúrgico con traqueopexia o aortopexia.7,8
En general, las tasas de mortalidad son menores a 10% en países desarrollados. El sistema de Spitz predice el pronóstico de pacientes con FTE/AE basándose en su peso al nacer y la presencia o ausencia de una cardiopatía congénita mayor (Tabla 1). Los infantes con bajo peso al nacer y anomalías cardíacas tienen la mayor tasa de morbimortalidad.3

Tabla 1. Tasas de supervivencia de Spitz, 2006.
En entornos de bajos recursos, las tasas de mortalidad siguen siendo elevadas y varían entre un 40% y hasta 80%.6 Las altas tasas de mortalidad se han atribuido a la presentación tardía la cual usualmente se asocia con neumonía por aspiración. Otros factores que pueden contribuir a la mortalidad incluyen mínimos cuidados de soporte, tal como falta de cuidados intensivos neonatales y nutrición parenteral para la alimentación temprana. Las complicaciones en el posoperatorio temprano incluyen sepsis e insuficiencia respiratoria. Las complicaciones en el posoperatorio tardío en supervivientes son las mismas descritas en países desarrollados. Al igual que con otras anomalías congénitas, los niños con FTE/AE requieren apoyo multidisciplinario a largo plazo con un seguimiento adecuado para disminuir complicaciones a futuro.
REFERENCIAS Y LECTURA ADICIONAL
- Goyal, A; Jones, M.O; Couriel, J.M; Losty, P.D. Oesophageal atresia and trachea-oesophageal fistula. Archives of Disease in Childhood-Fetal and Neonatal Edition. 2006; 91(5) F381-F384.
- Hung O, Murphy MF. Management of the difficult and failed airway. 2ndedn. New York: McGraw-Hill Medical, 2011.
- Davis PJ, Cladis PF, Motoyama EK. Smith’s anesthesia for infants and children. 8thedn. Philadelphia: Mosby Publishing, 2011.
- Adebo OA. Oesophageal atresia and 5rachea-oesophageal fistula: review of a 10 year personal experience. West AfrJ Med 1990; 9(3): 164- 169.
- Harrison MR, Hanson BA, Mahour GH, Takahashi M, Weitzman JJ, The significane of right aortic arch in repair of esophageal atresia and tracheoesophageal fistula. J PediatrSurg 1977; 12:861-869.
- Ameh EA, Bickler SW, Lakhoo K, Nwomeh BC, Poenaru D. Oesophageal Atresia. Paediatric surgery: A comprehensive Text for Africa. Global Help Publication 2010; 306-309.
- Kovesi T, Rubin S. Long-term complications of congenital esophageal atresia and/or tracheoesophageal fistula. Chest 2004; 126:915-925.
- Schalamon J, Lindahl H, Saarikoski H et al. Endoscopic follow-up in esophageal atresia-for how long is it necessary? J PediatrSurg 2003; 38:702-704.



