General Topics
PUNTOS CLAVE
- La enfermedad de Moyamoya (EM) es una enfermedad venoclusiva cerebrovascular de etiología desconocida.
- Las manifestaciones de la EM son muy diversas, desde asintomática hasta ataques isquémicos transitorios, infartos cerebrales, hemorragia intracerebral y convulsiones.
- La revascularización quirúrgica de los pacientes con EM sintomáticos se considera superior al manejo medico con mejores pronósticos neurológicos y mayor reducción del riesgo de infarto cerebral isquémico o hemorrágico.
- El principal objetivo del manejo anestésico de la cirugía de bypass extra craneano-intracraneano (BEI) es balancear la oferta contra la demanda del oxígeno cerebral para asegurar una adecuada protección cerebral.
- Una vigilancia meticulosa con un control estrecho de los parámetros fisiológicos durante todo el periodo perioperatorio son la esencia para manejar la oferta y demanda cerebral de oxígeno para protegerlo.
- La monitoria invasiva de la presión arterial es esencial en el BEI. Comúnmente se usa también la monitoria del EEG procesado y potenciales evocados somatosensoriales.
- Cuidar los pacientes en el postoperatorio en cuidado intensivo por 24 a 48 hrs es importante para mantener un control estrecho de la presión arterial e identificar precozmente cualquier complicación incluyendo deterioro neurológico y alteraciones de la permeabilidad de la arteria temporal.
INTRODUCCION
La enfermedad de Moyamoya (EM) es vasculopatía oclusiva de índole progresivo con etiología desconocida de incidencia rara y de carácter crónico. La revascularización quirúrgica ha demostrado ser superior al tratamiento médico para prevenir los infartos isquémicos y hemorrágicos de la EM. Su manejo perioperatorio es un reto para los anestesiólogos. Es crucial conocer la fisiopatología subyacente de la enfermedad y mantener una perfusión cerebral y neuro protección adecuada para reducir los eventos cerebrovasculares. El manejo perioperatorio tiene un impacto directo sobre los desenlaces de esta cirugía.
ANTECEDENTES Y CARACTERISTICAS DE EM
La EM es una vasculopatía cerebral oclusiva tanto en niños como adultos. Se caracteriza por cambios estenóticos y oclusivos unilaterales o bilaterales en la porción distal de las arterias carótidas internas y las porciones proximales de la arteria cerebral anterior y de las de arteria cerebral media, y rara vez de las arterias cerebrales posteriores. Se pueden formar vasos colaterales anormales que generan la apariencia patognomónica una maraña de un modo de cigarrillo en una angiografía que se denomina Moyamoya en japonés.1-3
La EM la demografía de los pacientes varía considerablemente entre las diferentes etnias. Las poblaciones asiáticas en particular la japonesa tiene una alta incidencia de 0.54 por cada 100,000 personas y una relación mujer hombre de 1.8. en cambio, En Estados Unidos hay una incidencia de 0.086 por cada 100,000 personas. 2 En las etnias asiáticas, la EM es una enfermedad primaria de predisposición familiar y distribución bimodal picos observados a la edad de los 10 40 años. La isquemia cerebral es el evento precipitante más común tanto en adultos como en niños con una presentación de infartos cerebrales ataques isquémicos transitorios (AITs) cefalea o convulsiones. Otra presentación común es la hemorragia intracraneal mañana, siendo 7 veces más alta en adultos que en niños. En las poblaciones caucásicas la EM se presenta como una isquemia, secundaria a otras enfermedades cómo es posicionar radioterapia y arteriosclerosis y ocurre principalmente en adultos. 1,4

El comité de investigación de EM del Ministerio de salud, trabajo y bienestar del Japón desarrollaron unos criterios diagnósticos en el año 2012 que se muestran en la tabla 1. 5

La EM sea relacionado con una variedad de enfermedades enunciadas en la tabla 21 estos pacientes se presentan con vasculopatía característica y se le denomina síndrome de Moyamoya.
La EM comúnmente lleva a un deterioro en los primeros 2 años después de su presentación inicial en el 20% de los adultos y el 75% de los niños. No se han identificado métodos para detener su progreso. La revascularización quirúrgica es el tratamiento recomendado para los pacientes con EM que presentan síntomas isquémicos o hemorrágicos ya que reducen el riesgo de nuevos infartos, mejoran el desempeño diario y preservan las funciones altas del cerebro.
Si el tratamiento quirúrgico se considera de muy alto riesgo, se puede considerar la administración de agentes antiplaquetarios para los cuadros isquémicos. 5-7 Otros medicamentos comúnmente utilizados para controlar los síntomas incluyen los vasodilatadores como los calcio antagonista, y los anticonvulsivantes1,5. El manejo de los pacientes con EM asintomáticos está mal definido siendo el único consenso en la modificación del estilo de vida coma control de los factores de riesgo y exámenes periódicos de resonancias nucleares magnéticas y angiografías cerebrales. los antiplaquetarios no se recomiendan em los pacientes asintomáticos debido al riesgo de desarrollar infartos hemorrágicos. la revascularización quirúrgica puede ser considerada en pacientes asintomáticos cuando haya alteraciones hemodinámicas cerebrales si se estima que haya un bajo riesgo de morbilidad quirúrgica. En la actualidad existe un registro de EM de pacientes asintomáticos para generar la evidencia de manejo y guías en estos pacientes. 8
Manejo quirúrgico para EM
Las cirugías de revascularización cerebral pueden ser ya sea para aumento del flujo o restitución del flujo. 3 En EM, La revascularización se hace para aumentar el flujo sanguíneo del cerebro isquémico ya sea por un bypass directo, indirecto o una combinación de ellos. Todas estas opciones han sido reportadas de manera exitosa según las situaciones. 5 Un bypass directo es la anastomosis de una rama de la carótida externa comúnmente la arteria temporal superficial (ATS) a una rama de la carótida interna. La arteria cerebral media es la más usada en particular la rama M4 qué es el segmento terminal cortical. Este tipo de bypass aumenta inmediatamente el flujo al cerebro isquémico. Este es el procedimiento más comúnmente realizado en adultos, pero en niños reviste mayor dificultad por los vasos de menor calibre. 2
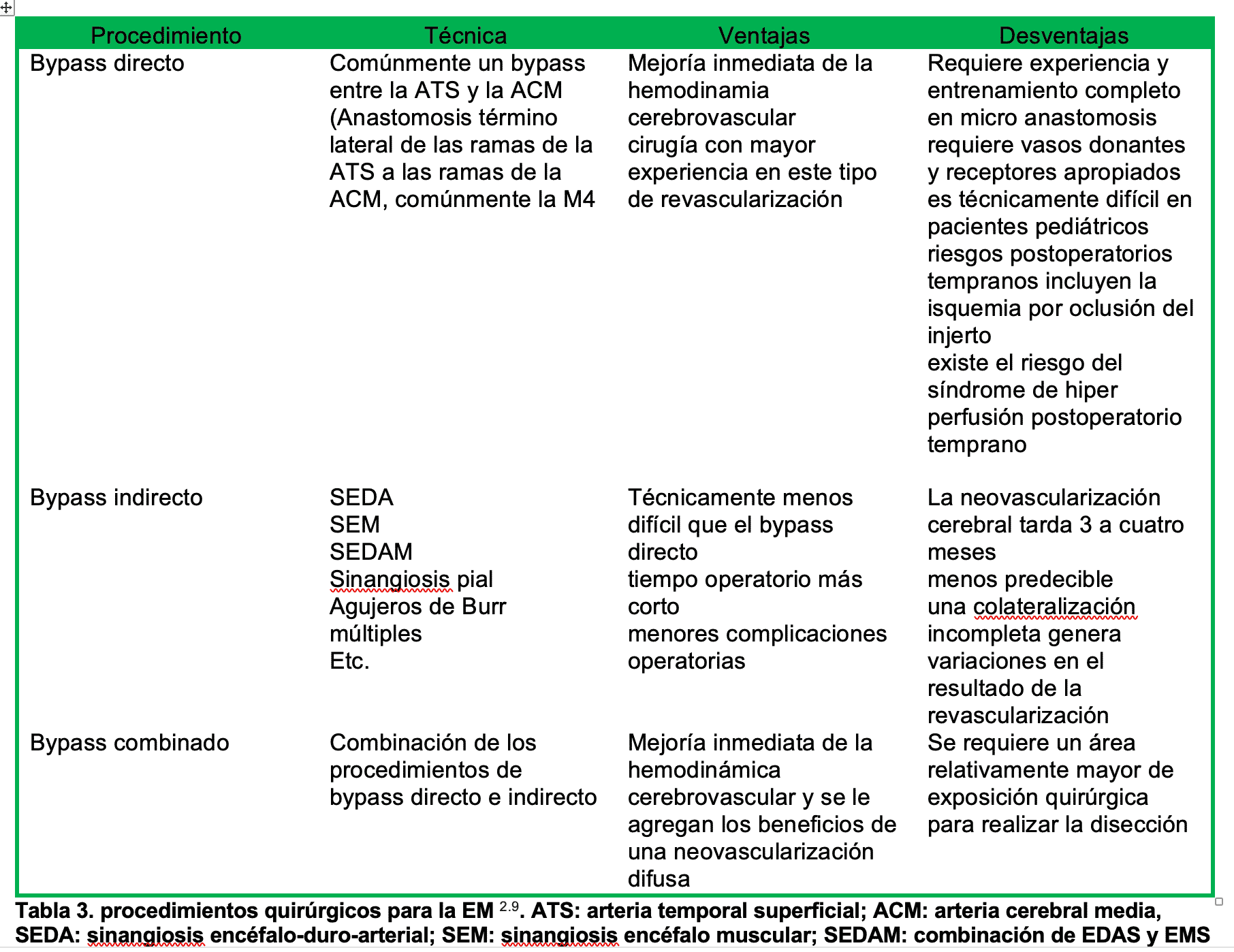
Un bypass indirecto pretende incrementar el flujo sanguíneo colateral a través de la angiogénesis, creando un contacto directo entre una fuente de tejido vascularizado extra craneano y las meninges. 3 Esto se hace comúnmente por una encefaloduroarteriosinangiosis, en la cual la ATS se desplaza y se anastomosa a los bordes abiertos de la duramadre o también como una encefalomiosinangiosis en la cual el músculo temporal se adosa a la superficie del cerebro. 2 El tipo de revascularización escogido depende del grupo etario, los síntomas, las comorbilidades y la preferencia del cirujano. Cómo lo habitual es que ambos lados de la vasculatura cerebral estén involucrados la cirugía se hace en 2 pasos revascularizándose el lado más sintomático primero. Estos procedimientos se discuten en la tabla 3. 2,9 En los adultos los bypass directos han demostrado ser más eficaces para la prevención de los infartos cerebrales que los indirectos, mientras que en los niños por la dificultad técnica de los bypass directos y por lograr mejor angiogénesis se prefieren los bypass indirectos en este grupo etario.
Evaluación preoperatoria
Una evaluación preoperatoria comprensiva que es indispensable. Múltiples comorbilidades Con implicaciones anestesiológicas pueden asociarse con la EM. es importante la evaluación de los síntomas preexistentes ya que una historia de AITs frecuentes indican un flujo sanguíneo cerebral precario que exige un manejo operatorio meticuloso y es un factor de riesgo para complicaciones. 2 Una hipertensión compensatoria puede ocurrir con la estenosis y oclusión cerebral vascular y las presiones basales preoperatorias son importantes para guiar las metas hemodinámicas intraoperatoria. en algunos centros los pacientes con EM son admitidos previamente para una hidratación agresiva la víspera de la cirugía procurando mantener una mayor estabilidad hemodinámica intraoperatoria especialmente durante la inducción. como las comorbilidades en la EM son comunes esta población de pacientes comúnmente tiene prescritos múltiples medicaciones crónicas. Una conciliación medicamentosa adecuada debe ser considerada de manera preoperatoria. comúnmente se recomienda continuar los anticonvulsivantes y los bloqueadores del canal de sodio. Para los medicamentos antiplaquetarios discutirlos con el neurocirujano es importante ya que muchos centros continúan la aspirina hasta el día de cirugía mientras que otros lo suspenden de 7 a 10 días antes con o sin terapia puente como heparina de bajo peso molecular. la aspirina habitualmente se reinicia en el primer día postoperatorio si la hemostasia el satisfactoria. 2,3,11
Consideraciones intraoperatorias y metas anestésicas
La principal meta anestésica en el manejo de los pacientes con EM es balancear la oferta de oxígeno cerebral con la demanda. Los pacientes programados para los bypass extra craneano-intracraneano comúnmente han agotado su reserva de oxígeno cerebral, con una microcirculación dilatada al máximo y unas ratas de extracción de oxígeno elevadas, generando múltiples consideraciones preoperatorias en estos pacientes.
Premediación e inducción
En los niños el llanto YO hiperventilación generan hipocapnia que conlleva paso conseguido cerebral y por consiguiente isquemia por lo que la premedicación con sedantes debe ser considerada tanto en niños como en pacientes ansiosos. Por otro lado, la sobre sedación puede causar hipo ventilación e hipercapnia generando robo intracerebral ya que las colaterales en la EM son poco vaso activas mientras que los otros vasos normales pueden vaso dilatarse y de manera paradójica secuestran la sangre. El midazolam oral o intravenoso se usa comúnmente en pediatría siendo una alternativa la dexmedetomidina nasal. Debe hacerse monitoria de la saturación arterial y considerarse el uso de oxígeno suplementario. los ansiolíticos no farmacológicos pueden ser útiles como lo son la presencia de los padres durante la inducción o el uso de vídeos o música.
Una inducción estable es benéfica para mantener la perfusión cerebral. En los pacientes pediátricos, en pacientes calmados y cooperativos o en pacientes ligera o moderadamente sedados una inducción inhalada Consejo FA no puede ser ideal para evitar la hiperventilación y la hipotensión. Opcionalmente si se logra un acceso venoso una inyección intravenosa con propofol, tiopental o etomidato pueden usarse. El uso cuidadoso de opioides intravenosos como fentanil (2-3 mg/kg) o remifentanil (0.5-1 mcg/kg) y/o lidocaína (1mg/kg) pueden considerarse para atenuar la respuesta hemodinámica a la laringoscopia. Si hay hipotensión inducida por la inducción, los vasoconstrictores como la fenilefrina deben estar disponibles inmediatamente y es razonable infundir profilácticamente estos para permitir una titulación rápida y reducir los episodios hipotensivos. Los relajantes musculares no despolarizantes con mínima liberación de histamina son adecuados para la inducción.
Monitoría
La monitoría intraoperatoria incluye los estándares de la American Society of Anesthesiologists (electrocardiografía, presión arterial no invasiva, saturación arterial de oxígeno, la capnografía y la temperatura) y debe agregarse la monitoria intraarterial de la presión para monitorear continua y muestreo sanguíneo. La consideración del uso de va a ser profesores como noradrenalina validan la inserción de un catéter venoso central posterior a la inducción (a menos que haya factores que lo contraindiquen). pueden usarse dispositivos de neuro monitoreo incluyendo electroencefalografía, potenciales evocados somatosensoriales o motores, Doppler trans craniano, saturación de oxígeno del bulbo yugular y espectroscopia del infrarrojo según la experiencia institucional, aunque el beneficio de estas técnicas en estos procedimientos no se ha establecido adecuadamente. 3
En nuestra institución la discusión preoperatoria con los neurocirujanos del plan quirúrgico es una práctica estándar que incluye el conocer los vasos donantes y recipientes, la probable duración del planteo de los vasos, la necesidad de supresión de picos y otras dificultades quirúrgicas esperadas. En las cirugías que involucran un bypass TSA-M4 utilizamos el índice biespectral para monitorizar la profundidad anestésica y preparar la posibilidad te necesitar la supresión de picos.
Sí la anastomosis es un segmento proximal de la cerebral media el electroencefalograma y los potenciales evocados somatosensoriales y motores se usan para monitorizar la isquemia cerebral ya que el clampeo transitorio puede comprometer el flujo sanguíneo a otras partes vitales del cerebro.
Medicamentos anestésicos
Para el mantenimiento de la anestesia se ha utilizado tanto anestesia total intravenosa como inhalada en diferentes instituciones sin lograr definir la ideal. algunos estudios han encontrado que flujos sanguíneos regionales de la corteza son más altos, la presión intracraneana es más baja y hay una mayor reducción del robo intracerebral con el propofol que con los anestésicos inhalados. 2 Sin embargo, no hay diferencia significativa en la incidencia y complicaciones post operatorios entre las 2 técnicas. el uso de remifentanilo ha demostrado proveer una hemodinamia más estable en la inducción, mantenimiento y despertar de la anestesia. 12,13 Globalmente no existe evidencia suficiente para demostrar la superioridad de una técnica anestésica sobre la otra.
Control hemodinámico y manejo de fluidos
Mantener la “normotensión” basado en la presión arterial basal es muy importante a través de todo el periodo preoperatorio y vital para los desenlaces neurológicos post operatorios. la meta hemodinámica intraoperatoria es de 10 al 20% de la presión arterial basal. el manejo cuidadoso de la presión arterial es esencial para mantener un flujo sanguíneo cerebral adecuado y reducir el riesgo de infartos isquémicos o hemorrágicos. esto es especialmente importante en los niños ya que ellos tienen una demanda metabólica cerebral aumentada, una extracción de oxígeno mayor y una respuesta auto regulatoria menor comparar a la de los adultos.3 La hipotensión puede llevar a isquemia cerebral perioperatoria, trombosis postoperatoria del injerto, y debe ser tratada con vasoconstrictores como efedrina o fenilefrina. la hipertensión puede exacerbar el sangrado en particular en el sitio de anastomosis y generar la ruptura de vasos colaterales frágiles que pueden producir hemorragia intracerebral. la hipertensión debe ser agresivamente monitoreada y corregida asegurando un nivel adecuado de anestesia y usando medicaciones adicionales como labetalol, esmolol u opioides dependiendo de la causa.
La meta del manejo de fluidos es la normovolemia, principalmente con cristaloides si no hay una pérdida significativa de sangre, aunque algunos proponen la hipervolemia para mitigar la hipotensión. Si hay una pérdida significativa de sangre deben medirse la hemoglobina y el hematocrito y deben ser corregidos según necesidad. una meta de hematocrito del 30 al 42% se ha sugerido para mantener el balance entre la capacidad de transporte de oxígeno y la viscosidad sanguínea, ya que los extremos en cualquiera de estos pueden inducir isquemia en los pacientes con EM. 2,11
Ventilación
La meta para la ventilación intraoperatoria es la normocapnia y la oxigenación normal. esta última es un requerimiento básico para un aporte adecuado de oxígeno cerebral. el dióxido de carbono es un poderoso modulador del tono cerebrovascular. En los pacientes con EM las áreas del cerebro suplidas por los vasos enfermos están en mayor riesgo de isquemia cerebral en los que tanto la hipercapnia como la hipocapnia tienen impactos negativos en la percusión cerebral ya sea induciendo un fenómeno de robo o de vasoconstricción cerebral respectivamente.
Temperatura
Hay consenso de mantener una temperatura corporal normal. evitar la hipertermia se recomienda comúnmente ya que en un aumento de la tasa metabólica cerebral aumenta el consumo de oxígeno y puede precipitar episodios de isquemia. aunque una hipertermia leve (~33°C) durante el clampeo de los vasos teóricamente puede ofrecer un grado de neuro protección reduciendo la rata metabólica cerebral hay preocupación de su capacidad de inducir vaso espasmo, y no hay evidencia de su impacto favorable en los desenlaces.2,3,11
Métodos neuro protectores durante la anastomosis arterial
Durante el bypass directo es necesario el clampeo el vaso receptor mientras se hace la anastomosis término lateral. en los procedimientos para el aumento del bajo flujo en la EM el vaso o recipiente es típicamente el segmento cortical M4 que nutre un área relativamente superficial del cerebro qué tiene una circulación colateral aceptable. para estos procedimientos el clampeo arterial es relativamente corto de menos de 30 minutos. se sugiere el aumento de la presión arterial por encima de un 20% del basal para mantener y mejorar el flujo colateral. menos frecuentemente sí la anastomosis es a un segmento más proximal de las cerebral media la inducción de una supresión de picos aumentando las concentraciones de propofol guiadas por monitoria bio espectral o electroencefalográfica se recomienda para reducir la demanda de cerebral de oxígeno.
Despertar y cuidado postoperatorio
Un despertar hemodinámicamente estable y tranquilo es deseable para prevenir las complicaciones hemorrágicas o isquémicas. una reversión adecuada del bloqueo neuromuscular y analgesia adecuada permiten asegurar la normocapnia, reducir el estrés, evitar la agitación, reducir la náusea y vómito y mantener la permeabilidad del injerto. una evaluación clínica neurológica debe realizarse tan pronto como sea posible. Los pacientes típicamente son vigilados por lo menos 1 noche en una unidad de cuidado intensivo neurológico para una observación estrecha para signos o síntomas de complicaciones en las primeras 24 a 48 horas. se hace énfasis en evitar colocar presión en el lado de la cabeza donde se hizo la revascularización. la monitoria con un Doppler transcutáneo se usa comúnmente para monitorear la permeabilidad del injerto diariamente. 6 Deben establecerse las metas de presión arterial a mantener por parte del equipo neuro quirúrgico teniendo presente si uno o 2 lados del cerebro han sido re vascularizados.
Complicaciones y desenlaces
La morbilidad y mortalidad quirúrgica por hemisferio tratado se reporta como 3.5% y 0.7% respectivamente, para los procedimientos de revascularización en los pacientes con EM. 6 La complicación más común postoperatoria es la aparición de isquemia o de un nuevo síndrome de hiperperfusión cerebral. 15
Un estudio retrospectivo concluyó que la incidencia de isquemia postoperatoria está más relacionada con el manejo quirúrgico y la severidad de la enfermedad más que otros factores como el manejo anestésico. los factores de riesgo para la isquemia postoperatoria incluyen una historia de AITs frecuentes, pacientes con factores precipitantes de AITs Y cirugía de revascularización indirecta. 13 Estudios más pequeños han encontrado otros factores de riesgo como la hipovolemia perioperatoria, hipercapnia, hipocapnia, hipotensión y hematocrito bajo, 2,15 pero estos no fueron factores independientes de complicaciones si su duración fue controlada.
Un aumento significativo del plus sanguíneo cerebral por encima de la demanda metabólica del cerebro puede causar hiperperfusión cerebral. este este escenario se presenta frecuentemente después de la cirugía de un bypass directo en el período postoperatorio agudo y se manifiesta por un deterioro neurológico transitorio caracterizado por disartria, disfunción mano-motriz, disfasia moto sensorial, o convulsiones. los factores de riesgo para desarrollar hiper perfusión sintomática incluyen una extracción elevada de oxígeno en los estudios preoperatorios de una tomografía de emisión de positrones que indican un flujo sanguíneo cerebral significativamente reducido. la hiper perfusión cerebral frecuentemente es transitorio con el flujo sanguíneo cerebral regresando a niveles normales 3 o 4 meses del postoperatorio. 16 Sin embargo, como el síndrome de hiper perfusión cerebral es un factor de riesgo importante para la hemorragia intracraneana debe hacerse un control estricto de la presión arterial cuando se sospecha con una meta de presión arterial inferior a 120/80 mmHg.
Debe anotarse que el deterioro neurológico postoperatorio puede ocurrir por hipo perfusión cerebral, vaso espasmo del injerto, o hiperperfusión cerebral y puede ser difícil diferenciar estas etiologías clínicamente. el uso de Doppler transcraneal, espectroscopia del infrarrojo e imágenes dinámicas (como escaneo de perfusión o angiografía) son útiles para discriminar la causa.
RESUMEN
La EM es una enfermedad cerebrovascular rara mayormente de etiología desconocida para la que no hay un tratamiento efectivo comúnmente aceptado. Se propone la revascularización quirúrgica sobre el manejo médico para [revenir episodios isquémicos yo hemorrágicos en los pacientes sintomáticos. En estos pacientes, el bypass para aumentar el bajo flujo es la cirugía mas frecuentemente realizada, y para su manejo anestésico, el objetivo es mantener el balance de la oferta vs. demanda de oxígeno cerebral. Es indispensable una comprensión minuciosa de la patología de la EM para proporcionar un acto anestésico seguro y efectivo para mejorar los desenlaces postoperatorios y evitar complicaciones.
REFERENCES
- Scott RM, Smith Moyamoya disease and moyamoya syndrome. N Engl J Med. 2009;(12) 360:1226-1237.
- Parray T, Martin TW, Siddiqui S. Moyamoya disease: a review of the disease and anesthetic management. J Neurosurg Anesthesiol.2011;23(2):100-109.
- Chui J, Manninen P, Sacho RH. Anesthetic management of patients undergoing intracranial bypass procedures. Anesth Analg.2015;120(1):193-203.
- Sato Y, Kazumata K, Nakatani E et Characteristics of moyamoya disease based on national registry data in Japan. Stroke. 2019;50(8):1973-1980.
- Research Committee on the Pathology and Treatment of Spontaneous Occlusion of the Circle of Willis; Health Labour Sciences ResearchGrant for Research on Measures for Intractable Guidelines for diagnosis and treatment of moyamoya disease (spontaneousocclusion of the circle of Willis). Neurol Med Chir (Tokyo). 2012;52(5):245-266.
- Aaron Cohen-Gadol. The neurosurgical atlas, low flow revascularization. Accessed January 7, 2021. https://www.neurocom/volumes/cerebrovascular-surgery/revascularization/low-flow-revascularization?highlight¼low%20flow
- Miyamoto S, Yoshimoto T, Hashimoto N, et Effects of extracranial-intracranial bypass for patients with hemorrhagic moyamoyadisease: results of the Japan Adult Moyamoya Trial (JAM trial) Stroke. 2014;45(5):1415-1421.
- Kuroda S, AMORE Study Asymptomatic moyamoya disease: literature review and ongoing aMORE study. Neurol Med Chir (Tokyo).2015;55(3):194-198.
- Mayeku J, Lopez-Gonzalez Current surgical options for moyamoya disease. Cureus. 2020;12(11):e11332.
- Jeon JP, Kim JE, Cho WS, et al. Meta-analysis of the surgical outcomes of symptomatic moyamoya disease in adults. J Neurosurg.2018;128(3):793-799.
- Giustini AJ, Stone SA, Ramamoorthy Moyamoya disease in children and its anesthetic implications: a review. Pediatr Anesth.2020;30(11):1191-1198.
- Adachi K, Yamamoto Y, Kameyama E, et Early postoperative complications in patients with moyamoya disease—a comparison ofinhaled anesthesia with total intravenous anesthesia (TIVA). Masui. 2005;54(6):653-657.
- Sakamoto T, Kawaguchi M, Kurehera K, et Risk factors for neurologic deterioration after revascularization surgery in patients withmoyamoya disease. Anesth Analg. 1997;85(5):1060-1065.
- Williams GW II, Jones WS, Chaudhry R, et Intraoperative anesthesiology management and patient outcomes for surgicalrevascularization for moyamoya disease: a review and clinical experience. J Neurol Surg A. 2019;80(3):143-148.
- Zhao M, Deng XF, Zhang D, et Risk factors for and outcomes of postoperative complications in adult patients with moyamoyadisease. J Neurosurg. 2019;130(2):531-542.
- Kaku Y, Iihara K, Nakajima N, et Cerebral blood flow and metabolism of hyperperfusion after cerebral revascularization in patients withmoyamoya disease. J Cereb Blood Flow Metab. 2012;32(11):2066-2075.
This work by WFSA is licensed under a Creative Commons Attribution-NonCommercial-NoDerivitives 4.0 International License. To viewthis license, visit https://creativecommons.org/licenses/by-nc-nd/4.0/
WFSA Disclaimer
The material and content provided has been set out in good faith for information and educational purposes only and is not intended as a substitute for theactive involvement and judgement of appropriate professional medical and technical personnel. Neither we, the authors, nor other parties involved in its production make any representations or give any warranties with respect to its accuracy, applicability, or com- pleteness nor is any responsibility accepted forany adverse effects arising as a result of your reading or viewing this material and content. Any and all liability directly or indirectly arising from the use of thismaterial and content is disclaimed without reservation.



