General Topics
PUNTOS CLAVE
- Hipertensión Pulmonar (HP) se define como una presión media de arteria pulmonar ≥ 20 mm Hg en reposo.
- El manejo perioperatorio apunta a minimizar los efectos de anestesia y cirugía sobre la función ventricular derecha en los pacientes a riesgo de tal disfunción como resultado de una HP crónica.
- La función ventricular derecha puede estar comprometida si hay (1) una reducción en la perfusión ventricular derecha si la resistencia vascular sistémica (RVS) cae y/o (2) una reducción en volumen latido ventricular derecho si la resistencia vascular pulmonar (RVP) aumenta.
- Caídas en RVS pueden ser minimizadas con el uso juicioso de vasopresores y fluídos intravenosos.
- Aumentos agudos en RVP pueden ser minimizados evitando precipitantes vasoconstrictores pulmonares directos, es decir, hipoxia, hipercarbia, acidosis e hipotermia.
- Técnicas anestésicas regionales, en lo posible, son a menudo preferibles ya que es menos probable que comprometan RVS y RVP en la manera descrita arriba.
INTRODUCCIÓN
Hipertensión Pulmonar (HP) se define como una presión de cateterización de arteria pulmonar ≥ 20 mm Hg en reposo y resistencia vascular pulmonar > 3 unidades Wood (WU).1 La severidad se clasifica como leve (20-40 mm Hg), moderada (40-55 mm Hg) y severa (>55 mm Hg).
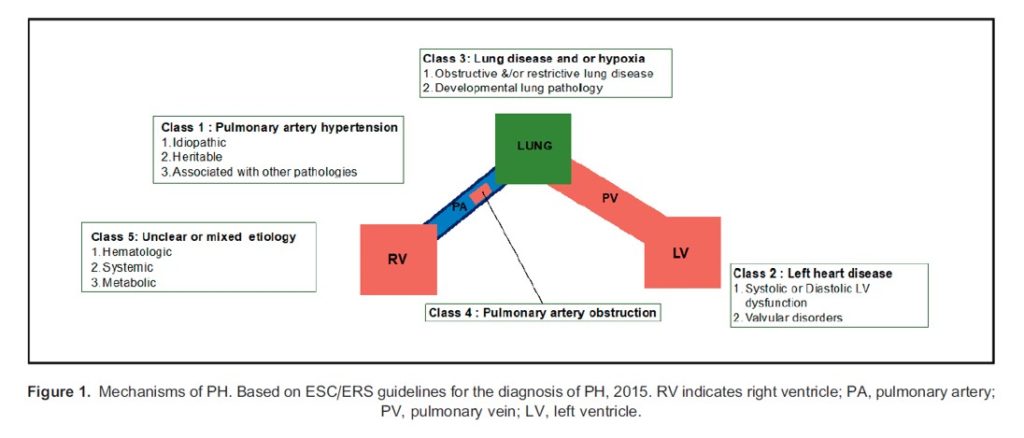
Una Fuerza de Tarea Conjunta de la Sociedad Europea de Cardiología y la Sociedad Respiratoria Europea (ESC/ERS) proveyó una clasificación para la etiología de la HP (Figura 1).
- Clase : enfermedad de la vasculatura arterial pulmonar
- Clase : debido a enfermedad de corazón izquierdo.
- Clase : debido a enfermedad pulmonar o hipoxia
- Clase : debido a obstrucción de arteria pulmonar
Clase 5: etiologías multifactoriales
Figura 1. Mecanismos de HP. Basado en guías de ESC/ERS para el diagnóstico de HP, 2015. RV: Ventrículo derecho, PA: Arteria pulmonar, PV: Vena pulmonar, LV: Ventrículo Izquierdo.
Clase 1: Hipertensión arteria Pulmonar Clase 2: Enfermedad de Corazón Izquierdo
- Idiopática 1. Disfunción Sistólica o Diastólica VI
- Hereditaria 2. Desórdenes valvulares
3. Asociada con otras patologías
Clase 3: Enfermedad Pulmonar y/o Hipoxia Clase 4: Obstrucción Arteria Pulmonar
- Enfermedad Pulmonar Obstructiva
y/o Restrictiva
- Patología Pulmonar del Desarrollo
Clase 5: Etiología no clara o mixta
- Hematológica
- Sistémica
- Metabólica
La epidemia Europea de HP a mitad de los 1960’s, siguiendo al uso generalizado del supresor del apetito anfetamina-like de prescripción Aminorex, resultó en su reconocimiento por la Organización Mundial de la Salud. 2
Las causas subyacentes varían entre los países, con los países de bajos ingresos agobiados por etiologías infecciosas tales como VIH, enfermedad cardíaca reumática y esquistosomiasis, mientras que la etiología en los países de altos ingresos, grandes recursos, es en gran parte secundaria a enfermedad pulmonar obstructiva crónica (EPOC) y falla ventricular izquierda secundaria a enfermedad arterial. La incidencia anual de HP está aumentando en el Reino Unido; las estimaciones actuales predicen 8 casos por millón de personas.
Demográficamente, los pacientes diagnosticados con HP están en la 5a década de la vida (53 ± 14 años) y es más probable que sean mujeres (2- 5:1) con una etiología de enfermedad clase 2 ó 3. La razón de la desigualdad entre sexos permanece sin esclarecer. Datos de registro multicéntricos basados en los EU (Registro REVEAL) destacan una disparidad racial: 73% Caucásicos, 13% Afro- Americanos y 9% Hispánicos.3 El reconocimiento temprano de la enfermedad es a menudo un desafío debido a síntomas no-específicos, lo que lleva a un retraso en el diagnóstico de hasta 2 años, con una clara influencia en el pronóstico de la enfermedad, especialmente en el caso de la esclerosis sistémica.
Fisiología y Patofisiología Ventricular Derecha
Estructura Ventricular Derecha y Suministro Sanguíneo
El ventrículo derecho (VD) bombea sangre desoxigenada en la vasculatura pulmonar, de alto-volumen, baja-presión. Este sistema requiere menor trabajo de latido comparado con el ventrículo izquierdo (VI), con una consecuente reducción 6-x de la masa ventricular derecha.
Usualmente, la arteria coronaria derecha, (ACD) suple el corazón derecho. En ausencia de patología, tal como hipertrofia, la relativamente baja presión intraventricular permite el flujo a través de la ACD durante todo el ciclo cardíaco, aunque el flujo diastólico predomina en los vasos más distales. La presión de perfusión del VD es por lo tanto dependiente de la presión arterial media en vez de solo la presión diastólica; esto difiere con la situación de perfusión de VI.4
Resistencia Vascular Pulmonar
HP puede o no estar asociada a una resistencia vascular pulmonar (RVP) aumentada. Sin embargo el manejo anestésico frecuentemente está basado en evitar aumentos agudos en RVP que pueden exacerbar la disfunción de VD. Comprender los factores que alteran la RVP es por lo tanto crítico en el manejo perioperatorio de estos pacientes.
La vasculatura pulmonar es de paredes delgadas y fácilmente distensible; la resistencia es baja y dependiente de factores físicos pasivos tales como gravedad, postura y la diferencia de presiones entre los alvéolos y los capilares. El diferencial de presión alveolar-capilar está aumentado en momentos de bajo gasto cardíaco (los capilares colapsan fácilmente), subexpansión pulmonar (las fuerzas que mantienen los alveolos abiertos se ven disminuídas), o sobreexpansión pulmonar (los capilares pulmonares están compresionados). Otros factores alteran activamente la RVP afectando el tono muscular vascular pulmonar. (Tabla 1).
Patofisiología
Cambios crónicos en la poscarga de VD, como se observa en HP, pueden perjudicar la perfusión de la coronaria derecha, debido al efecto de cambios adaptativos miocárdicos en los vasos coronarios, similar a lo que ocurre con la hipertensión sistémica perjudicando la perfusión miocárdica del VI. Esto puede hacer al VD de un paciente con HP más susceptible a la isquemia si la presión de perfusión desciende.

En salud, el VD puede dilatarse y acomodar mayores volúmenes más fácilmente que el VI. Sin embargo, la elevación crónica de la presión de la arteria pulmonar puede llevar a cambios hipertróficos con un aumento en el grosor de la pared del VD y una reducción del radio interno. En esta etapa, el VD responde pobremente a elevaciones agudas de la presión de la arteria pulmonar, lo que puede precipitar falla aguda de VD secundaria a sobredistensión, tanto macroscópicamente hacia el VI (via desviación del septo interventricular) y microscópicamente debido al sobreestiramiento de la sarcómera. A la larga, ambos mecanismos conducen a una reducción en el gasto de ambos ventrículos para una precarga determinada, resultando en shock cardiogénico.
EVALUACIÓN PREOPERATORIA Y MANEJO
Historia
Los símtomas de HP crónica son a menudo inespecíficos, lo que conduce a un retraso en el diagnóstico. Los síntomas pueden ser clasificados en 4 categorías:
- Síntomas sistémicos de gasto cardíaco reducido (eg, disnea y fatiga)
- Síntomas cardíacos primarios: falla de VD lleva a dolor precordial al esfuerzo y síncope con ganancia de peso y sobrecarga de líquidos.
- Síntomas mecánicos intratorácicos: Dilatación del tronco de la arteria pulmonar puede llevar a compresión del nervio laríngeo recurrente izquierdo, presentándose como ronquera.
- Síntomas relacionados a la etiología subyacente (Figura 1)
Síntomas sugestivos de enfermedad de vía aérea superior (apnea obstructiva del sueño) enfermedad respiratoria crónica (EPOC, tromboembolismo venoso) enfermedades de tejido conectivo, desórdenes endócrinos y metabólicos.
b. Historia de uso ilícito de drogas, ingesta de alcohol, fumado y factores de riesgo de VIH.5
Exámen
Los signos clínicos pueden reflejar lo siguiente:
- Falla de VD: elevación de la presión venosa yugular y signos asociados de sobrecarga de líquidos, tales como hepatomegalia sensible, ascitis y edema periférico.
- Regurgitación de válvula tricúspide causando un murmullo pansistólico y una onda “v” prominente en la curva de presión venosa central.
- Presión de arteria pulmonar elevada que lleva a una intensidad aumentada del segundo ruido cardíaco (P2 fuerte)
Investigaciones
Las pruebas de laboratorio pueden ser usadas tanto para cribado como para diagnóstico de pacientes con HP. Las pruebas de detección básicas deberían incluir un ecocardiograma; la Sociedad Británica de Ecocardiografía en 2018 describe los criterios para diagnóstico de HP (Tabla 2).6 No hace falta decir, dicho ecocardiograma puede también dar detalles del tamaño y función del VD para ayudar a delinear las consecuencias a órganos blanco de un diagnóstico de HP.

Tabla 2. Criterios Diagnósticos de HP Durante Ecocardiografía. Los criterios ecocardiográficos sugestivos de HP son determinados por parámetros positivos de al menos 2 grupos (ventrículo, arteria pulmonar, vena cava inferior y atrio derecho). Adaptado con permiso de las guías 2018 de la Sociedad Británica de Ecocardiografía.6 VD indica ventrículo derecho; VI, ventrículo izquierdo; AP, arteria Pulmonar; VCI, vena cava inferior
Pruebas adicionales que pueden proveer mayor información incluyen las siguientes:
- Bioquímica de Laboratorio ( la enfermedad cardíaca puede causar disfunción renal, ya sea directamente o como consecuencia de tratamiento farmacológico para falla cardíaca)
- Péptido natriurético cerebral elevado puede ser sugestivo de disfunción VD +/- VI
- Electrocardiografía (desviación del eje a la derecha, bloqueo de rama derecha y finalmente una relación onda R/onda S en V1 >1 son sugestivas de tensión en el VD)
- Radiografía de tórax (puede mostrar evidencia de patología cardiorrespiratoria e HP con agrandamiento de los vasos pulmonares centrales y agrandamiento del atrio y ventrículo derechos)
Pruebas de función pulmonar ( PFP’s) son un método no invasivo de evaluar la función pulmonar. Los pacientes que se presentan con HP deberían tener PFP’s, especialmente aquellos con enfermedad multifactorial (clase 5) o enfermedad pulmonar específica (clase 3). Debe enfocarse la atención en la reversibilidad, patrones de vía aérea común (relación volumen de espiración forzada en 1 segundo/capacidad vital forzada) y tasas de intercambio gaseoso (capacidad de difusión del monóxido de carbono).
El gold standard para el diagnóstico sigue siendo la cateterización de corazón derecho (RHC; Figura 2).7 Parámetros a notar durante la cateterización son los siguientes:
- Pulmonares
a) Presión de arteria pulmonar b) RVP c) Presión capilar pulmonar en cuña (Figura 2) - Cardíacos
a) Presión ventricular derecha b) Presión atrio derecho c) Gasto cardíaco d) Índice Cardíaco
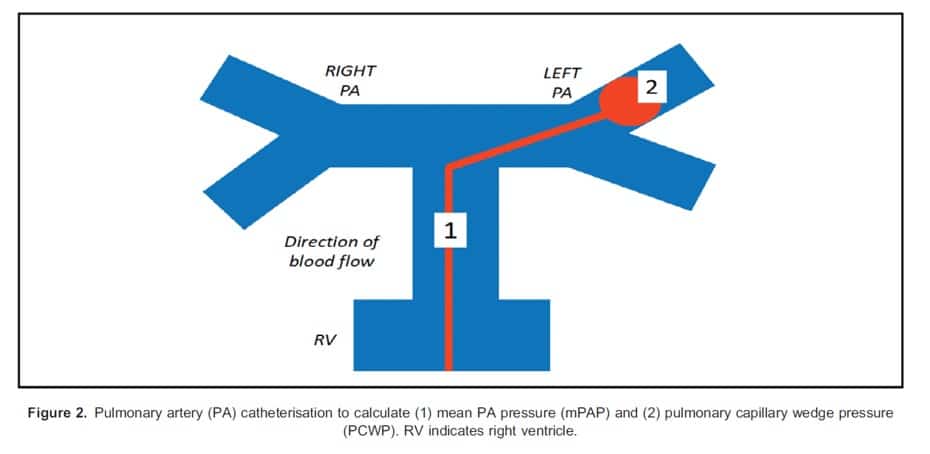
Figura 2. Cateterización de Arteria Pulmonar (PA) para calcular (1) Presión PA media (mPAP) y (2) presión capilar pulmonar en cuña (PCWP). RV indica ventrículo derecho. (Right: derecha; Left: izquierda)
Pruebas cardiopulmonares de esfuerzo (CPET) siguen siendo una herramienta no invasiva y dinámica fundamental para determinar la capacidad funcional y limitación al ejercicio al tiempo que obtiene información acerca de la capacidad metabólica y la función cardiorrespiratoria.8 CPET puede proveer información de apoyo acerca de patrones de enfermedad pero, a diferencia de RHC, no hace diagnóstico de HP.
Los pacientes con HP pueden no ser capaces de alcanzar oxigenación perioperatoria adecuada, debido a un gasto cardíaco deteriorado en presencia de presiones medias de arteria pulmonar elevadas (mPAPs) y posible disfunción de VD. La guía europea más reciente (2015 ESC/ERS) usa VO2 máximo (consumo máximo de oxígeno en mL/kg/min) y VE/V0CO2 (equivalentes ventilatorios para dióxido de carbono) para clasificar pacientes de HP en categorías de bajo, mediano o alto riesgo, aunque el documento reconoce que el protocolo de carga progresiva usado en CPET no está estandarizado para pacientes de HP.
Manejo de la Enfermedad Crónica
En el Reino Unido, el manejo de la enfermedad crónica en HP se inicia por 1 de 8 centros terciarios cuando la mPAP es ≥ 25 mm Hg. Hay disponibles tratamientos farmacológicos efectivos específicos a cada etiología. Las células endoteliales pulmonares liberan óxido nítrico, que estimula las células del músculo liso vascular para producir guanosín monofosfato cíclico (cGMP), una vía intracelular, que luego resulta en relajación de las células de músculo liso vascular pulmonar mediado por adenosina monofosfato cíclico.
Las clases de medicamentos básicas para el tratamiento farmacológico de HP incluyen las siguientes:
- Inhibidores de la Fosfodiesterasa-5 (sildenafil): inhibición de esta enzima previene la ruptura del cGMP intracelular
- Activadores del Guanilato ciclasa (riociguat): estimula la producción de cGMP por la misma via que el óxido nítrico
- Agonistas de receptores de Prostaciclinas (selexipag): estos se unen selectivamente al receptor I de prostaglandinas, un receptor acoplado a proteína G que propicia vasodilatación.
- Antagonista de receptor de Endotelinas (ERA; ambrisentan, bosentan): ERAs inhibe la acción de endotelina-1, un amino ácido producido por células endoteliales que promueve la constricción vascular.
Agentes activos respiratorios deben ser continuados a través del período perioperatorio, con conversión a rutas inhaladas o intravenosas cuando la vía enteral no está dsiponible.
Otras terapias pueden incluir diuréticos y oxígeno suplementario. Una sospecha de un estado protrombótico en HP o una etiología tromboembólica puede significar que los pacientes también sean tratados con anticoagulantes, pero la naturaleza heterogénea de la HP significa que esto es a menudo específico para cada paciente.
CUIDADO INTRAOPERATORIO
Toma de Decisiones Preoperatorias
Es importante que los pacientes sean evaluados y optimizados por un especialista en HP antes de cirugía electiva; la presencia de HP eleva la mortalidad perioperatoria, por lo que los riesgos y beneficios de la cirugía deben ser valorados entre sí.
Esto puede significar una discusión multidisciplinaria para identificar si la cirugía es en el mejor interés del paciente o no. Una condición que puede normalmente ser tratada quirúrgicamente puede ser tratada de manera conservadora si esa es la decisión correcta para ese paciente. Este balance de riesgos necesita considerar la opinión del especialista, el deseo del paciente, la patología quirúrgica y el sitio y magnitud de la cirugía; esta toma de decisión es probablemente tan importante como el manejo intraoperatorio de la fisiología del paciente.
Requerimientos Cardiovasculares
Las dos principales metas intraoperatorias al administrar anestesia para pacientes con HP apuntan a mantener el gasto cardíaco.
Primero, para evitar comprometer la perfusión de VD que se lleva a cabo en forma más o menos continua durante el ciclo cardíaco, es esencial mantener la presión arterial sistólica. Esto significa mantener la resistencia vascular sistémica (RVS) contrarrestando la reducción que a menudo ocurre en la presencia de agentes anestésicos vasodilatadores. Esto puede lograrse con vasopresores administrados periféricamente (metaraminol o fenilefrina) o centralmente (eg, noradrenalina o vasopresina).
Noradrenalina teóricamente ayuda a mantener la función de VD vía agonismo de adrenoceptores β1 y reducción de RVP mediada por β2, mientras que vasopresina ofrece un beneficio potencial similar al aparentar no causar constricción vascular pulmonar. Sin embargo, estos beneficios no se han demostrado que causen resultados en ensayos clínicos, y todos los agentes han sido usados con seguridad y efectividad en la práctica clínica.9
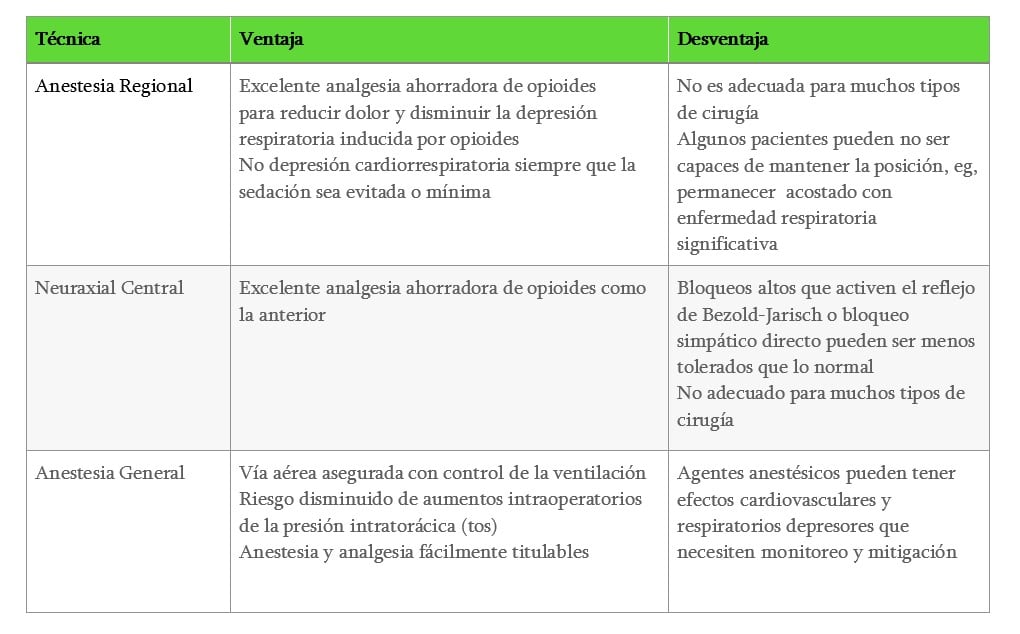
Tabla 3. Técnica Anestésica, Ventajas y Desventajas Explicadas. PONV indica náusea y vómito postoperatorio
Segundo, es importante evitar elevaciones agudas de RVP que comprometerían la eyección de VD. Esto puede ocurrir con función de VD preservada pero será más severa en un ventrículo deteriorado. Como se mencionó arriba, si el VD se dilata en respuesta a una postcarga aumentada, puede también llevar a distorsión del septo interventricular, comprometiendo la eyección del VI.10 RVP pueden ser influenciadas tanto farmacológicamente como no farmacológicamente.
Las medidas no farmacológicas incluyen evitar precipitantes fisiológicos de vasoconstricción pulmonar como la hipoxia, hypercapnia (meta PaCO2 4-4.5 kpa), sobre- y sub- inflación de los pulmones (6-8 mL/kg de peso corporal ideal), acidosis, dolor e hipotermia.
Las medidas farmacológicas incluyen la implementación de agentes vasodilatadores pulmonares que pueden ser administrados tanto por vía inhalada como endovenosa. Los agentes incluyen análogos sintéticos de la prostaciclina (iloprost y epoprostenol) y gases (óxido nítrico); estos agente y, más importante, la experiencia en su uso pueden estar disponibles solo en ciertos centros.
También puede ser necesario apoyar directamente el gasto cardíaco con un agente inotrópico. Los sensibilizadores del calcio (eg, levosimendan) y los inhibitors de la fosfodiesterasa (eg, milrinone) pueden ser útiles ya que pueden reducir la RVP y por lo tanto ser más beneficiosos en falla de corazón derecho. Sin embargo, no existe un inotrópico de corazón derecho selectivo. Nótese que el uso de inotrópicos puede requerir administración concomitante de vasopresores para atenuar la vasodilatación que ocurre con algunos agentes inotrópicos.
TÉCNICAS DE ANESTESIA
La técnica anestésica más apropiada para cada paciente va a depender de factores del paciente, de la anestesia y de la cirugía.
Los factores del paciente obviamente incluyen condiciones médicas adicionales relevantes y el escoge del paciente pero también necesitará considerar la severidad de la HP y la disfunción cardíaca asociada.
Los factores anestésicos y quirúrgicos incluyen el posicionamiento del paciente, la duración de la cirugía, el sitio operatorio y el riesgo de inestabilidad cardiovascular (eg, pérdida sanguínea); estos son claramente aplicables con o sin HP.
Anestesia General y regional —ya sea neuroaxial central, regional periférica o anestesia local— son todas opciones potenciales, y las ventajas y desventajas claras están enumeradas en la Tabla 3. Mientras que muchas de estas ventajas y desventajas son genéricas, es la prevención de cualquier depresión cardíaca y respiratoria innecesarias que es de beneficio específico en pacientes con HP, más aún que en un paciente sano y en forma, de ahí el rol de una analgesia ahorradora de opioides, evitar la sedación excesiva o un buen control del intercambio gaseoso.
La anticoagulación puede ser común y necesita ser considerada al optar por ciertos tipos de técnicas anestésicas regionales.
Anestesia Regional y Local
La anestesia regional se mantiene como una opción simple y segura para proveer estas condiciones cardiovasculares intraoperatorias con la ventaja agregada de una buena analgesia intra y postoperatoria libre de opioides. Evidentemente, algunos tipos de cirugía, tales como cirugía ortopédica u oftálmica, se prestan a anestesia regional.
Estas ventajas pueden ser anuladas si la anestesia regional se acompaña por cualquier efecto adverso de una sedación concomitante. El uso de sedación debe por lo tanto ser considerado muy cuidadosamente.
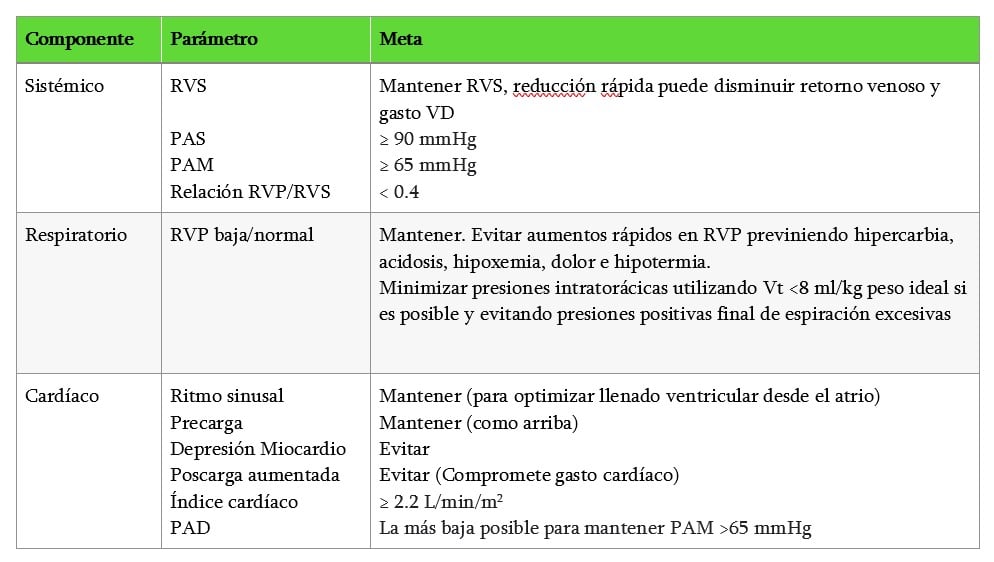
Tabla 4. Metas y Parámetros Hemodinámicos Perioperatorios. Adaptado con permiso de Pilkington et al.12 RVS indica resistencia vascular sistémica; PAS, presión arteria sistólica; PAM, presión arterial media; RVP, resistencia vascular pulmonar; Vt, volumen tidal; PAD, presión atrio derecho
Anestesia Central Neuroaxial
La anestesia neuroaxial puede ser administrada con seguridad a los pacientes de HP si se presta atención a alcanzar las metas cardiovasculares descritas arriba. Puede ocurrir vasodilatación sistémica relativamente rápido, lo que puede comprometer el llenado cardíaco derecho así como la perfusión coronaria de VD. Si se combina con la inhibición de fibras nerviosas autonómicas cardioaceleradoras de tórax alto, puede resultar en una respuesta cronotrópica e inotrópica negativa profunda. En ambas instancias, el deterioro cardiovascular en presencia de mPAPs elevadas puede llevar a perfusión respiratoria disminuida, crisis hipertensiva pulmonar aguda y colapso cardiovascular, por lo que debe tomarse cuidado con las metas cardiovasculares ya descritas.
Anestesia General
La anestesia regional o local a menudo es una opción preferida. Sin embargo, hay circunstancias en las que la anestesia general es el único escoge, y es aún así una opción segura en pacientes de HP si se presta atención a las metas ya descritas.
El control diligente del CO2 y por tanto del pH es importante y es a menudo alcanzado más fácilmente a través de una ventilación controlada. Esto usualmente necesita intubación endotraqueal, pero para cirugías más cortas en pacientes apropiados (eg, no obeso, bajo riesgo de aspiración, etc), un dispositivo supraglótico de segunda generación apropiado (SAD) puede ser utilizado.
En cambio, técnicas de ventilación espontánea, usualmente pero no exclusivamente involucrando un SAD, son usualmente evitados en pacientes con HP a menos que la enfermedad sea leve y el procedimiento corto.
Tanto agentes anestésicos volátiles como intravenosos tienen efectos depresores cardiorrespiratorios, pero la inducción y mantenimiento de la anestesia puede ser logrado con seguridad con ambos. Todos los agentes intravenosos y todos los agentes inhalatorios administrados hasta una concentración de 1 Concentración Alveolar Mínima tienen efectos despreciables en la resistencia vascular pulmonar.11
Todos los agentes reducen el impulso ventilatorio y la ventilación minuto, pero esto se evita con el control de la ventilación. Hay una disminución de la vasoconstricción pulmonar hipóxica pero poco efecto directo en RVP, aparte del óxido nitroso, que puede aumentar directamente RVP y por lo tanto es mejor evitar en pacientes con HP.
Los efectos cardiovasculares varían dependiendo del agente utilizado, pero todos en general disminuyen la contractilidad miocárdica, RVS, volumen latido y presión sanguínea. Pueden haber efectos diferentes en la frecuencia cardíaca dependiendo del agente y la tasa de administración. Todos estos efectos son predecibles, el uso apropiado de monitoreo y soporte cardiovascular farmacológico pueden ayudar a mejorarlos y mantener la meta de una de una RVS sostenida (para perfusión y llenado de VD desde el retorno venoso).
Los pacientes deben ser monitoreados según las técnicas de monitoreo standard recomendadas descritas por la Asociación de Anestesiólogos de Gran Bretaña e Irlanda. Monitoreo adicional dependerá del paciente y la cirugía, y pueden incluir monitoreo invasivo de presión arterial y/o venosa central, cateterización de arteria pulmonar u otras técnicas de monitoreo de gasto cardíaco. Los parámetros hemodinámicos perioperatorioss sugeridos — cuando están disponibles a partir de monitoreo invasivo — se encuentran en la tabla 4.
CUIDADOS POSTOPERATORIOS
HP conlleva mortalidad y morbilidad perioperatoria significativa. Los pacientes deben ser monitoreados postoperatoriamente en una unidad de alta dependencia. Las metas postoperatorias reflejan los parámetros cardiorrespiratorios dirigidos a prevenir las elevaciones en RVP y mantener la RVS, como se describió (Tabla 4).
Una buena analgesia, que idealmente utilice abordajes ahorradores de opioides incluyendo analgésicos no sedantes (paracetamol, anti-inflamatorios no esteroideos), y analgesia local o regional deben ser aplicados en lo posible, ya que esto asiste en minimizar los aumentos de RVP asociados a hipoventilación así como mejorar la recuperación en general.
También debe haber una interrupción mínima de la terapia de HP ya instalada.
Las taquiarritmias son un problema común en los pacientes de HP. A diferencia de las enfermedades de corazón izquierdo, las arritmias son usualmente supraventriculares, los ritmos ventriculares son raros. Las arritmias supraventriculares pueden comprometer tanto el pronóstico de corto como de largo plazo, con un potencial de deterioro hacia falla cardíaca derecha. La restauración y mantenimiento del ritmo sinusal es altamente deseable, con antiarrítmicos profilácticos siendo usados con frecuencia. Faltan datos acerca de fármacos individuales, pero usar un agente con inotropismo negativo mínimo debe ser considerado.
Los ritmos asociados con inestabilidad hemodinámica deben ser tratados según algoritmos de resucitación, usando cardioversión eléctrica según sea apropiado.
CRISIS PULMONAR HIPERTENSIVA
Una crisis pulmonar hipertensiva (CPH) se caracteriza por elevación aguda de RVP que sobrepasa la habilidad del VD para mantener el gasto en contra de una postcarga elevada y está asociada a una mortalidad significativa (>50%).13 Esto puede avanzar a afectar negativamente la precarga de VI, gasto cardíaco de VI y presión de perfusión coronaria diastólica, llevando a colapso miocárdico y shock cardiogénico.
Bajo condiciones fisiológicas normales, la adaptación y remodelamiento de VD ayudan a mantener el gasto de VD. Sin embargo, los cambios fisiológicos intraoperatorios secundarios a factores físicos (e.g, posicionamiento de paciente y neumoperitoneo) o farmacológicos (anestésicos u otros fármacos) pueden llevar a descompensación. El rápido reconocimiento de CPH es esencial; mientras que los signos de shock cardiogénico son observados característicamente, la confirmación generalmente requiere mediciones invasivas de presiones y/o ecocardiografía junto a la cama (presiones pulmonar y de atrio derecho elevadas con gasto cardíaco decreciente).
Las opciones de tratamiento son de apoyo o farmacológicas y reflejan las previamente discutidas para controlar las RVP:
- De soporte
Tratamiento de una causa precipitante específica si es posible (e.g, dolor, hipotermia)
b. Oxígeno suplementario
c. Administración de fluídos apropiada (si se sospecha hipovolemia)
d. Apoyo Ventilatorio para mantener el CO2 y controlar el pH si es necesario; la depresión respiratoria postoperatoria puede ser multifactorial - Farmacológicos
- El gasto cardíaco puede ser aumentado con agentes inotrópicos y cronotrópicos
b. Las resistencias vasculares sistémicas pueden ser aumentadas con vasopresores
c. Pueden darse vasodilatadores vasculares pulmonares por vía inhalada o intravenosa.
RESUMEN
Los pacientes con HP se presentan tanto para cirugía cardíaca y no cardíaca como electiva y de urgencia. No todos los pacientes podrían tener un diagnóstico preoperatorio confirmado, por lo que la evaluación clínica puede ser necesaria para ayudar en el diagnóstico y determinar el grado de compromiso cardiorrespiratorio.
El manejo intraoperatorio debería involucrar aporte de un clínico experimentado en el manejo de pacientes con HP. El cuidado postoperatorio debería realizarse en un área de alta agudeza, con técnicas regionales bajas en opioides conformando el pilar principal del tratamiento.
REFERENCIAS
- Condon DF, Nickel NP, Anderson R, et al. The 6th World Symposium on Pulmonary Hypertension: what’s old is new. F1000Research. 2019;8(F1000 Faculty Rev-888).
- Montani D, Seferian A, Savale L et al. Drug-induced pulmonary arterial hypertension: a recent outbreak. Eur Respir Rev. 2013;22(129):244-250.
- Frost AE, Badesch DB, Barst RJ, et al. The changing picture of patients with pulmonary arterial hypertension in the United States: how REVEAL differs from historic and non-US contemporary registries. Chest. 2011;139(1):128-137.
- Crystal GJ, Pagel PS. Right ventricular perfusion: physiology and clinical implications. Anesthesiology. 2018;128(1):202- 218.
- Elliot CA, Kiely DG. Pulmonary hypertension. Contin Educ Anaesth Crit Care Pain. 2006;6(1):17-22.
- Augustine DX, Coates-Bradshaw LD, Willis J, et al. Echocardiographic assessment of pulmonary hypertension: a guideline protocol from the British Society of Echocardiography. Echo Res Pract. 2018;5(3):G11-G24.
- Rosenkranz S, Preston IR. Right heart catheterisation: best practice and pitfalls in pulmonary hypertension. Eur Respir 2015;24(138):642-652.
- Farina S, Correale M, Bruno N, et al. The role of cardiopulmonary exercise tests in pulmonary arterial hypertension. Eur Respir Rev. 2018;27(148):170134.
- Currigan DA, Hughes RJA, Wright CE, et al. Vasoconstrictor responses to vasopressor agents in human pulmonary and radial arteries: an in vitro study. Anesthesiology. 2014;121:930-936.
- Condliffe R, Kiely DG. Critical care management of pulmonary hypertension. BJA Educ. 2017;7(17):228-234.
- Sarkar MS, Desai PM. Pulmonary hypertension and cardiac anaesthesia: anesthesiologist’s perspective. Ann Card 2018;21(2):116-122.
- Pilkington SA, Taboada D, Martinez G. Pulmonary hypertension and its management in patients undergoing non-cardiac Anaesthesia. 2015;7(1):56-70.
- Simon M. Perioperative management of pulmonary hypertensive crisis. Adv Pulm Hypertens. 2013;12(1):38-39.