Obstetric Anaesthesia
PREGUNTAS
Antes de continuar, trate de responder las siguientes preguntas. Las respuestas se pueden encontrar al final del artículo, acompañadas de una explicación. Por favor, responda Verdadero o Falso:
- En cuanto a la miocardiopatía periparto (PPCM) (MCPP en español):
a. La etiología está bien establecida
b. La disfunción diastólica es una característica común
c. El 80% de las mujeres se recuperan ad integrum
d. La incidencia es alta
e. Por lo general es un diagnóstico de exclusión - Los siguientes hallazgos ECG se asocian con el embarazo:
a. Desviación del eje a la derecha
b. La depresión del segmento ST en derivaciones de los miembros (Bipolares I-II-III)
c. Ondas Q en la derivación III
d. Inversión de la onda T en derivaciones inferiores (II-III-AVF)
e. Latidos prematuros - En cuanto a la miocardiopatía periparto:
a. Comúnmente se presenta en el primer trimestre del embarazo
b. Se puede presentar hasta cinco meses después del parto
c. Las afectadas tienen una fracción de eyección ventricular izquierda > 45%
d. Se asocia con trombo mural
e. La tasa de mortalidad puede ser hasta un 50% - Los siguientes son factores de riesgo para el desarrollo de la miocardiopatía periparto:
a. La edad materna avanzada (> 35 años)
b. El embarazo múltiple
c. El uso de tocolíticos
d. Primiparidad
e. Etnia - Con respecto al manejo de la miocardiopatía periparto:
a. Los betabloqueantes pueden mejorar el resultado
b. El manejo debe ser multidisciplinario
c. Es poco probable que la MCPP ocurra en embarazos ulteriores
d. La terapia anticoagulante está contraindicada
e. Se deben evitar las arritmias
EJEMPLO DE UN CASO
Una señora de 37 años de edad se presenta a las 36 semanas de gestación en su cuarto embarazo con una historia de 6 días de deterioro con falta de aire, disnea paroxística nocturna, ortopnea y edema periférico. Sus tres embarazos anteriores fueron por vía vaginal y sin complicaciones.
Su historia clínica incluye hipotiroidismo y obesidad mórbida (IMC 40). Ella no ha tenido antecedentes de patología cardíaca. No hay antecedentes familiares, ni de consumo de drogas o alcohol significativos.
En el examen la paciente está taquipnéica y taquicárdica en reposo, con presión sanguínea normal. La saturación de oxígeno es de 92% con aire ambiente. En la auscultación son audibles estertores bibasales. La gasometría arterial revela una alcalosis respiratoria con hipoxemia leve, el electrocardiograma (ECG) muestra taquicardia sinusal con bloqueo de rama izquierda, la radiografía de tórax muestra cardiomegalia con líquido en la cisura horizontal y vasos prominentes en el lóbulo superior.
INTRODUCCIÓN
La miocardiopatía periparto (MCPP) es una enfermedad rara que afecta a las mujeres al final del embarazo y en el período post-parto. Se caracteriza por insuficiencia cardiaca que se presenta en ausencia de cualquier otra causa identificable. Se asocia con morbilidad y mortalidad significativas. El reconocimiento temprano y el manejo agresivo de la enfermedad son fundamentales para mejorar los resultados.
INCIDENCIA
La verdadera incidencia de MCPP es desconocida. La incidencia reportada varía entre 1 en 3000 a 1 de cada 10.000 embarazos.
ETIOLOGÍA Y FISIOPATOLOGÍA
La etiología de la miocardiopatía periparto es desconocida. Se postula que la MCPP podría estar mediada a través de muchos mecanismos que incluyen: factores inmunológicos, respuesta hormonal anormal, cambios inflamatorios anormales, miocarditis, o predisposición genética.
La MCPP se manifiesta predominantemente con disfunción sistólica ventricular originada en una reducción global en la contracción del miocardio y consecuentemente de la fracción de eyección del ventrículo izquierdo. La compensación por el agrandamiento del ventrículo izquierdo produce el aumento de los volúmenes telesistólico y telediastólico. Cuando falla la compensación, el gasto cardíaco disminuye y sobreviene insuficiencia cardiaca.
FACTORES DE RIESGO
Los factores de riesgo para MCPP incluyen:
- Edad materna > 30 años
- Multiparidad
- Grupo étnico – por ejemplo, afrodescendientes
- Obesidad
- Embarazo múltiple
- Embarazo asociado con trastornos hipertensivos
- Hipertensión esencial
- Tratamiento tocolítico con β-agonistas
- Consumo de cocaína
CARACTERISTICAS CLÍNICAS Y DIAGNÓSTICO
Los síntomas de falta de aire al hacer esfuerzos y ortopnea son comunes en el tercer trimestre. El diagnóstico de MCPP puede retrasarse si estos síntomas son erróneamente atribuidos a los cambios fisiológicos normales del embarazo.
Los síntomas de la MCPP incluyen: disnea, fatiga, ortopnea, disnea paroxística nocturna, palpitaciones, hemoptisis y edema periférico. Éstos pueden presentarse como episodios agudos o subagudos de insuficiencia ventricular izquierda.
Las taquiarritmias que pueden acontecer en la MCPP incluyen taquicardia supraventricular (TSV), fibrilación auricular (FA) y raramente taquicardia ventricular (VT). Existe un mayor riesgo de tromboembolia debido al desarrollo potencial de trombos murales.
La MCPP es un diagnóstico de exclusión. Las parturientas con cardiopatía congénita o adquirida reconocidas se pueden presentar con síntomas similares al final del embarazo o durante el parto. Del mismo modo, las mujeres embarazadas con cardiopatía isquémica o estructural no diagnosticada, tienen disminuida su reserva funcional y son menos capaces de tolerar los cambios hemodinámicos fisiológicos del embarazo normal.
El diagnóstico de MCPP debe cumplir cuatro criterios que: 1
- Insuficiencia cardíaca hacia el final del embarazo o hasta cinco meses después del parto
- Ausencia de otra causa identificable de la insuficiencia cardíaca
- Ausencia de síntomas cardiacos o enfermedad antes de final del embarazo
- Disfunción ventricular izquierda – definido como una fracción de eyección menor de 45% o reducción de la fracción de acortamiento de menos del 30%
La miocardiopatía con los criterios del 2-4 que se presenta antes del tercer trimestre se conoce como cardiomiopatía asociada al embarazo (PACM) (MP en español). La fisiopatología subyacente es probablemente similar a la MCPP.2
DIAGNÓSTICO DIFERENCIAL
El diagnóstico diferencial de la MCPP incluye:
- Embolia pulmonar
- Sepsis grave
- Embolia de líquido amniótico
- Preeclampsia / inducida por enfermedad hipertensiva del embarazo
- Arritmias
- Anemia grave
- Infarto de miocardio
- Miocardiopatía dilatada de otras etiologías (Tabla 1)
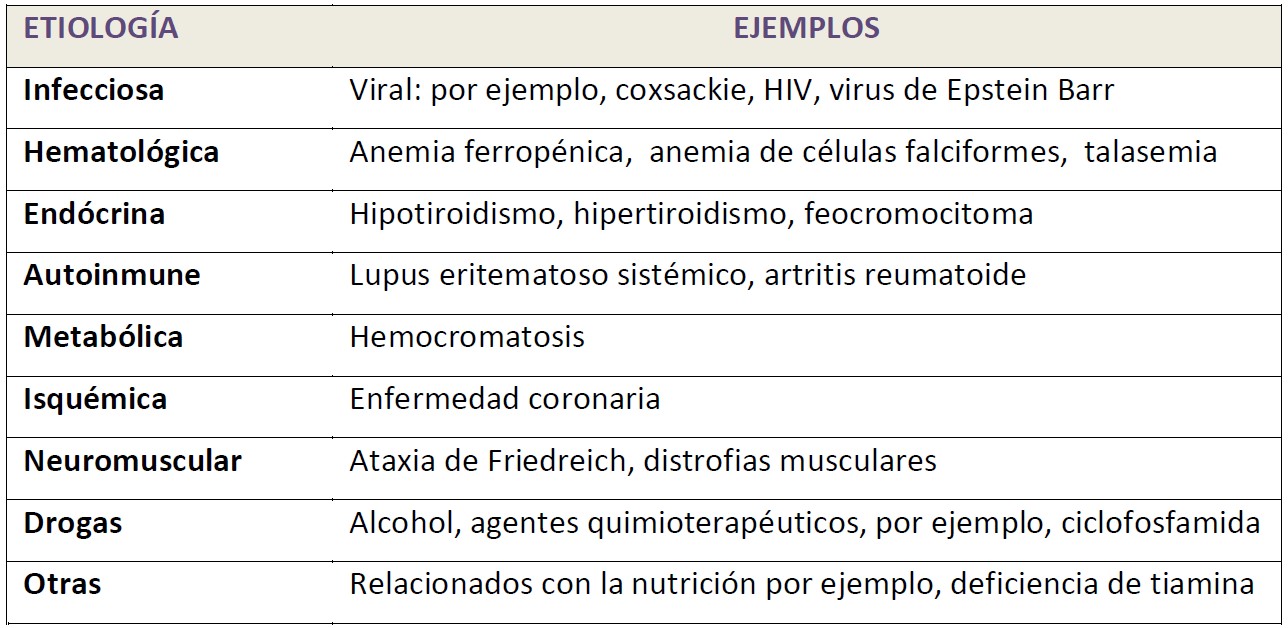
Tabla 1. Causas de la miocardiopatía dilatada
ESTUDIOS
Los estudios incluyen:
- Electrocardiograma (ECG)
- Ecocardiograma transtorácico incluyendo estudios Doppler
- Resonancia magnética cardíaca
- Angiografía coronaria
- Estudios virales
- Péptido natriurético tipo B (BNP): es un marcador de selección, pero carece de especificidad
PRONÓSTICO
El pronóstico es malo y la MCPP es una de las principales causas de muerte materna.3 Un indicador pronóstico es el grado de disfunción en la presentación, ya sea definido por la clasificación funcional de New York Heart Association (NYHA) o por ecocardiografía transtorácica.
La tasa de mortalidad es entre 15 y 50%. Entre el 30-50% mejora y recupera la fracción de eyección ventricular izquierda al 50% o más. La mortalidad resulta por insuficiencia cardíaca intratable, arritmias y tromboembolismo.
MANEJO
La identificación temprana de la MCPP periparto permite un manejo óptimo.
Es fundamental un manejo multidisciplinario de personal de alto nivel, y debe incluir la participación de un obstetra, un cardiólogo con especial interés en los trastornos obstétricos y un anestesiólogo. En caso de que la MCPP se presente durante el embarazo, la optimización de la madre es la clave y puede requerir un parto urgente. Un neonatólogo debería participar en las discusiones sobre la fecha del parto y hacer frente a los posibles efectos de la enfermedad de la madre en el neonato. Si es posible la admisión en Cuidados Críticos, la participación temprana de un especialista en cuidados intensivos es importante.
En dónde deben ser atendidas las mujeres con MCPP dependerá del momento y la presentación de la enfermedad. En todos los casos se debe considerar, remitir a un centro de atención obstétrica especializado con la experiencia y los recursos para el manejo de este tipo de pacientes.
TERAPIAS FARMACOLÓGICAS
El manejo de la MCPP es similar a la de otras causas de insuficiencia cardiaca e incluye el mantenimiento adecuado de la oxigenación, la restricción de líquido y sal y el acompañar la descarga ventricular con vasodilatación y diuresis.
Los inhibidores de la enzima convertidora de la angiotensina (IECA) han demostrado mejorar la mortalidad en la insuficiencia cardiaca y se recomienda como tratamiento de primera línea para el tratamiento de la MCPP.
Los bloqueadores de los receptores de angiotensina (BRA) son una alternativa para pacientes que no toleran los efectos secundarios de los IECA. Los IECA y los BRA están contraindicados durante el embarazo debido al riesgo teratogénico.
La administración de IECA, especialmente en el segundo y el tercer trimestre se asocia con aumento de la pérdida fetal, oligohidramnios, disfunción renal fetal y otras anomalías congénitas. No se recomienda el uso de IECA y BRA II en las madres que amamantan debido al riesgo de hipotensión neonatal. 4
La terapia con IECA en el post-parto se indica, mientras el ventrículo izquierdo continúe en fallo. Con la de IECA a largo plazo, puede mejorar el remodelado cardíaco.
La terapia de hidralazina y nitratos, tales como dinitrato de isosorbide, se puede utilizar de forma segura durante el embarazo. Estos medicamentos reducen la poscarga, la precarga y las presiones intracavitarias.
Los betabloqueantes han demostrado mejorar la supervivencia y pueden tener un efecto protector contra las taquiarritmias.
La digoxina se considera segura en el embarazo y puede ser utilizada por su efecto inotrópico positivo y para el tratamiento de la fibrilación auricular en caso de producirse. Los niveles plasmáticos de digoxina deben ser monitoreados cuidadosamente.
Los diuréticos de asa, por ejemplo furosemida, pueden reducir la congestión pulmonar y el edema periférico, se pueden utilizar de forma segura en el embarazo y la lactancia.
Los bloqueadores de los canales de calcio, se evitan generalmente, debido a sus propiedades inotrópicas negativas. No se recomiendan antagonistas de la aldosterona tales como espironolactona durante el embarazo.
La biopsia endomiocárdica se puede realizar para evaluar si la inmunoglobulina intravenosa puede ser beneficiosa. Existe alguna evidencia de pequeños ensayos para sugerir esta terapia dirigida y otros tales como la bromocriptina y la pentoxifilina, si la biopsia muestra un componente inflamatorio.5,6,7
No todas las MCPP se asocian con un estado de miocarditis inflamatoria y la terapia de inmunoglobulina no se recomienda empíricamente.
Debido al riesgo de tromboembolismo venoso y trombo mural asociados con MCPP, se indica terapia profiláctica con heparina de bajo peso molecular (HBPM). Si se han identificado secuelas tromboembólicas o trombo mural, está indicada la anticoagulación completa.
TERAPIAS NO FARMACOLÓGICAS
Las pacientes en la fase aguda pueden requerir terapia de apoyo con ventilación mecánica no invasiva o intubación, ventilación asistida y soporte inotrópico.
En los casos graves balón de contrapulsación intra-aórtico, dispositivo de asistencia ventricular izquierda (DAVI) o puede requerirse oxigenación por membrana extracorpórea (ECMO). El trasplante cardíaco puede estar indicado para pacientes con enfermedad grave que no responden a los tratamientos farmacológicos. Los implantes de cardiodesfibrilador o resincronizador son intervenciones posibles en aquellas mujeres que sobreviven a la fase aguda, pero los datos actuales sugieres que tendrán un deterioro funcional significativo.
RECOMENDACIÓN PRE- CONCEPTUAL
Se debe advertir a todas las mujeres con antecedentes de MCPP: hay un riesgo significativo de readquirir MCPP en embarazos posteriores. Las mujeres con deterioro cardíaco tras la MCPP, es decir clase 3 o 4 de la NYHA, o aquellas con una fracción de eyección ventricular izquierda inferior al 30% se encuentran en mayor riesgo con embarazos futuros. Las mujeres con mayor riesgo deberían recibir información sobre los riesgos de un futuro embarazo, orientación sobre anticoncepción y conocer la potencial necesidad de considerar la terminación del embarazo.
CONSIDERACIONES ANESTÉSICAS
LA MCPP plantea muchos retos para el anestesiólogo. La elección de la técnica anestésica se verá influenciada por la urgencia del parto y la condición fisiológica de la parturienta. Las mujeres con antecedente o sospecha de MCPP deben ser evaluados por un anestesiólogo en el momento oportuno y se debe acordar un plan para el parto y la atención del post-parto.
Las consideraciones respecto a la modalidad de parto deben incluir los antecedentes obstétricos del paciente, estado hemodinámico actual y su respuesta al tratamiento médico. El parto vaginal es una opción para las pacientes con MCPP compensada. Se recomiendan las técnicas para limitar el aumento de las catecolaminas plasmáticas, la resistencia vascular sistémica y la carga de trabajo del miocardio asociados con el trabajo de parto.
Se debe impedir la compresión aorto-cava en todo momento, evitando la posición supina sin desplazamiento uterino adecuado. Debe iniciarse temprano el control regular con ECG, saturación de oxígeno y mediciones de la presión arterial (hay escasa necesidad del control de la presión arterial invasiva). Con el fin de limitar el estrés cardiovascular del parto, se recomienda la analgesia epidural temprana. Esto no sólo reducirá la respuesta simpática causada por el dolor de las contracciones, sino que también disminuye la poscarga y proporciona la posibilidad de contar con la anestesia adecuada en caso de necesitarse la intervención quirúrgica.
La segunda fase del parto se puede controlar con ayuda instrumental para reducir la carga de trabajo del miocardio y los efectos cardiovasculares perjudiciales de la maniobra de Valsalva prolongada durante los pujos.
Se han descrito tanto la anestesia general y regional para el parto por cesárea.8 El monitoreo debe incluir la presión arterial invasiva. El monitoreo del gasto cardíaco proporcionará información adicional que el manejo perioperatorio.
Los objetivos de manejo anestésico son:
- Mantener la perfusión miocárdica, evitando:
- arritmias
- episodios de hipotensión o taquicardia
- Optimizar el gasto cardíaco
- mantener la precarga, pero evitar la sobrecarga de líquidos
- mantener / aumentar la contractilidad miocárdica
- evitar el aumento de la poscarga
La anestesia neuroaxial titulada incremental, epidural o epidural combinada y bajas dosis en la anestésica espinal, pueden alcanzar estos objetivos. La anestesia neuroaxial reduce la poscarga, promueve el flujo anterógrado y evita el uso de agentes anestésicos generales que reducen la contractilidad miocárdica. Los opioides neuroaxiales proporcionan analgesia efectiva postoperatoria reduciendo así la respuesta simpática mediada por el aumento de la poscarga después del parto. Se deben evitar caídas significativas en la resistencia vascular sistémica para que se mantenga la perfusión coronaria. Si se utiliza una técnica de anestesia neuroaxial, se debe prestar atención para sincronizar el tiempo de la terapia anticoagulante.
Si se lleva a cabo la anestesia general, la inducción debe ser tan suave como sea posible para minimizar tanto la hipotensión como la hipertensión. La respuesta presora a la laringoscopia y a la intubación debe ser atenuada con la administración de una dosis apropiada de un opioide de acción rápida, por ejemplo, alfentanilo o remifentanilo. Puede ser necesaria la administración de inotrópicos, como dobutamina, sensibilizadores de calcio (por ejemplo, levosimendán) o inhibidores de la fosfodiesterasa (por ejemplo milrinona) para compensar la depresión miocárdica causada por los agentes anestésicos intravenosos y volátiles. También puede ser necesario utilizar vasopresores para contrarrestar la vasodilatación y mantener la perfusión coronaria. La precarga debe mantenerse y el monitoreo del gasto cardíaco mínimamente invasivo o invasivo puede proporcionar información útil para orientar estas terapias.
Los fármacos uterotónicos deben utilizarse con precaución debido a sus efectos secundarios asociados:
- La oxitocina puede causar una marcada disminución en la resistencia vascular sistémica y en dosis más altas tiene un efecto antidiurético
- La ergometrina puede causar aumentos significativos en la poscarga
Después del parto, la paciente debe ser recuperada en un entorno de cuidados críticos con monitoreo hemodinámico invasivo continuo, manejo cuidadoso de líquidos y una analgesia adecuada.
RESUMEN
- La miocardiopatía periparto (MCPP) es una enfermedad rara con una mortalidad significativa
- La MCPP tiene criterios diagnósticos estrictos
- La identificación temprana de la miocardiopatía periparto mejora el resultado
- El manejo es multidisciplinario
- Se debe ofrecer asesoramiento a las mujeres que han padecido MCPP
RESPUESTAS
- a. F, b. F, c. F, d. F, e. V
La etiología es desconocida. Podría haber factores inmunológicos, cambios inflamatorios, miocarditis, o una predisposición genética.
La MCPP afecta predominantemente a la función sistólica.
La verdadera incidencia es desconocida.
La morbilidad y la mortalidad son altas (30-50%), mejorarán y recuperarán la fracción de eyección del ventrículo izquierdo el ≥50% de las pacientes.
Deben excluirse otras causas antes de diagnosticar MCPP. - a. F, b. V, c. F, d. V, e. V
La desviación del eje a la izquierda puede estar presente en el embarazo, debido al desplazamiento del ápex cardíaco.
La onda Q en la derivación III es una variante normal de toda la población, no es específica para el embarazo. - a. F, b. V, c. F, d. V, e. V
La MCPP se define como el desarrollo de insuficiencia cardíaca hacia el final del embarazo o dentro de los primeros cinco meses del puerperio. La disfunción ventricular izquierda en la MCPP se define como una fracción de eyección menor de 45% o por una reducción de la fracción de acortamiento de menos de 30%. - a. V, b. V, c. V, d. F, e. V
- a. V, b. V, c. F, d. F, e. V
La anticoagulación reduce el riesgo de tromboembolismo.
Las arritmias se deben evitar para optimizar la perfusión coronaria, la contracción auricular y ventricular, el volumen sistólico y el gasto cardíaco.
REFERENCIAS Y LECTURA ADICIONAL
- Sliwa K, Hilfiker-Kleiner D, Petrie MC, et al. Current state of knowledge on aetiology, diagnosis, management, and therapy of peripartum cardiomyopathy: a position statement from the Heart Failure Association of the European Society of Cardiology Working Group on peripartum cardiomyopathy. Eur J Heart Fail 2010; 12:767-78.
- Elkayam U, Akhter MW, Singh H, et al. Pregnancy-associated cardiomyopathy: clinical characteristics and a comparison between early and late presentation. Circulation 2005; 111:2050-5.
- Steer P, Gatzoulis M and Baker P. Heart Disease and Pregnancy. London: RCOG Press 2006.
- Drug and safety undate May 2009, vol 2 issue 10:3.
http://www.mhra.gov.uk/safetyinformation/drugsafetyupdate/CPN088003 - Mason JW, O’Connell JB, Herskowitz A, et al. A clinical trial of immunosuppressive therapy for myocarditis. The Myocarditis Treatment Trial Investigators. N Engl J Med 1995; 333:269-75.
- Sliwa K, Blauwet L, Tibazarwa K, et al. Evaluation of bromocriptine in the treatment of acute severe peripartum cardiomyopathy: a proof-of-concept pilot study. Circulation 2010; 121: 1465–73.
- Sliwa K, Skudicky D, Candy G, Bergemann A, Hopley M, Sareli P. The addition of pentoxifylline to conventional therapy improves outcome in patients with peripartum cardiomyopathy. Eur J Heart Fail 2002; 4:305–9.
- Soni B, Gautam P L, Grewal A, Kaur H. Anaesthetic management of two cases of peripartum cardiomyopathy. J Obstet Anaesth Crit Care 2011; 1:41-5.
Para leer el artículo en inglés:
http://resources.wfsahq.org/images/wfsa-documents/Tutorials_-_English/312_Peripartum_Cardiomyopathy.pdf



