Basic Sciences
QUESTIONS
Avant de continuer, essayez de répondre aux questions suivantes. Les réponses se retrouvent à la fin de l’article, accompagnées d’une explication. Prière de répondre par vrai ou faux:
- Au sujet de la pharmacologie du rémifentanil:
- La pharmacodynamie est plus étroitement liée au poids maigre qu’au poids réel
- La dose de rémifentanil doit être ajustée chez les patients dont la clairance de la créatinine est faible
- On retrouve moins de frissonnement postopératoire avec le rémifentanil qu’avec les autres opioïdes
- La demi-vie du rémifentanil est d’environ 3 minutes
- Le rémifentanil ne doit pas être donné aux patients qui ont un bloc prolongé suite à la succinylcholine, car il est lui aussi dégradé par les estérases plasmatiques
- Au sujet de l’anesthésie intraveineuse à objectif de concentration (AIVOC):
- Le modèle de Marsh est utilisé pour prédire les concentrations de rémifentanil au niveau des organes-cibles
- Les seules caractéristiques spécifiques au patient dont la pompe AIVOC a besoin sont la taille, le poids et le sexe
- Le rémifentanil diminue les besoins en propofol pour l’anesthésie intraveineuse totale
- La concentration de rémifentanil au site effecteur doit être maintenue entre 2 et12 microgrammes par ml (mcg.ml-1) pour obtenir une analgésie intraopératoire
- La dose de bolus de rémifentanil est de trois à quatre fois plus élevée avec la concentration plasmatique comme cible (Cpt) qu’avec le site effecteur (Cet) comme cible
- Parmi les applications cliniques du rémifentanil, on retrouve:
- L’intubation sans curare
- L’analgésie postopératoire contrôlée par le patient (ACP) à l’unité de soins
- Les changements de pansements chez les brûlés
- L’analgésie et la sédation aux soins intensifs
- L’ACP pendant le travail
INTRODUCTION
Le rémifentanil est un agoniste pur des récepteurs opioïdes μ mis en marché au début des années 1990. Grâce à son début d’action rapide, son effet pharmacologique court et une synergie avec les autres produits anesthésiants, le rémifentanil est idéal pour l’anesthésie et pour la sédation consciente. Ses indications s’élargissent alors que partout à travers le monde, on repousse continuellement les limites de son utilisation en anesthésie et aux soins intensifs. Cet article traite de la pharmacologie de base du rémifentanil, de son utilisation habituelle, des nouveaux créneaux et des considérations essentielles de sécurité.
Points essentiels
- Le rémifentanil est un médicament d’utilisation flexible dans un contexte d’anesthésie et de soins intensifs
- Sa durée d’action et sa demi-vie contextuelle sont brèves, ce qui le rend idéal pour l’analgésie et la sédation aux soins intensifs
- Il peut être utilisé de façon efficace pour l’intubation à fibre optique vigile et pour la sédation consciente
- Lorsque la péridurale ne peut se faire, une analgésie au rémifentanil contrôlée par la patiente peut être administrée dans les milieux qui adoptent une telle pratique
- L’utilisation de perfusions à objectif de concentration sans bolus permet d’éviter les effets secondaires cardiovasculaires et respiratoires significatifs du rémifentanil
PHARMACOLOGIE
La structure du rémifentanil, comme celle de l’alfentanil ou du sufentanil, est semblable à celle du prototype de sa classe, le fentanyl (Figure 1). La différence essentielle est la présence d’un groupe ester (partie ombrée), permettant un métabolisme rapide par les estérases plasmatiques et tissulaires non spécifiques. Ainsi, la molécule se démarque par une durée ultra-brève et des ajustements rapides de posologie sont possibles.
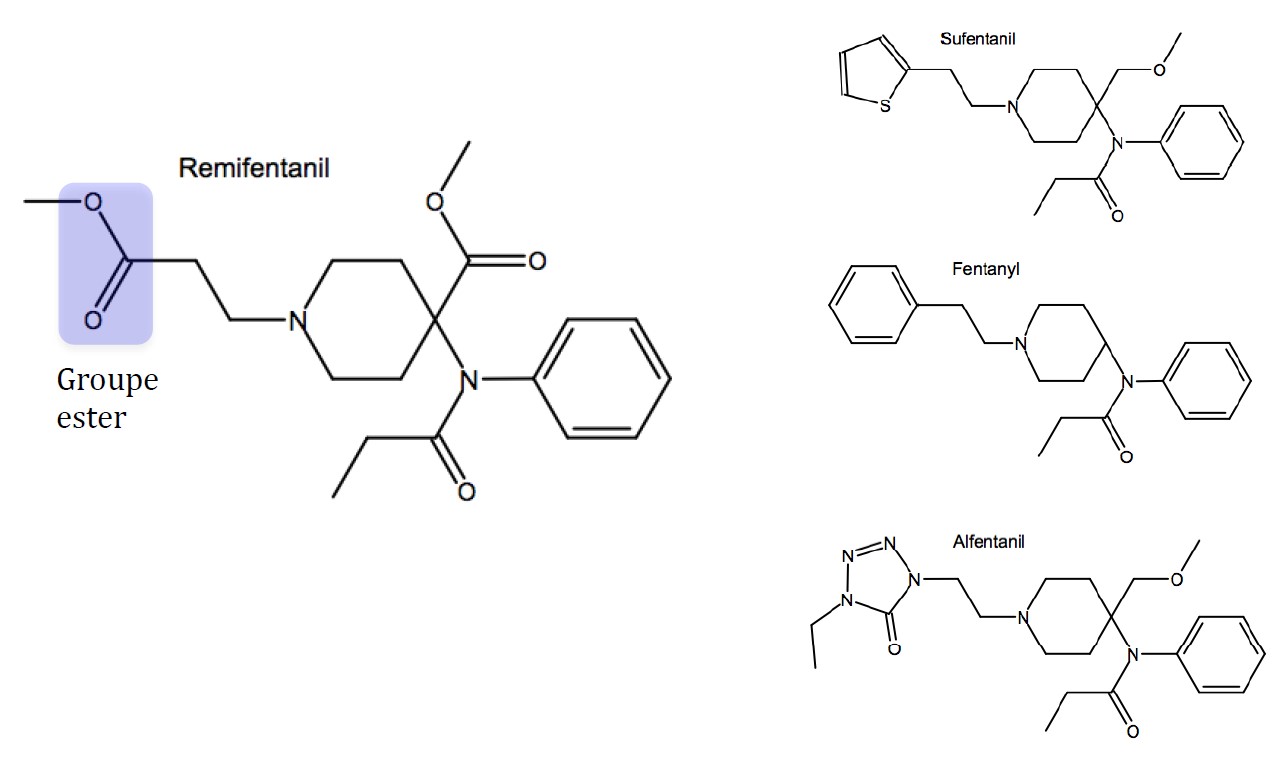
Figure 1. Structure du rémifentanil en comparaison avec d’autres opioïdes
Le rémifentanil est dégradé par des estérases, mais il peut être quand même utilisé chez les patients porteurs d’un déficit en pseudocholinestérase1. Son métabolite principal, l’acide de rémifentanil, est excrété par le rein et s’accumule chez les patients avec atteinte rénale1,2. Toutefois, la posologie du remifentanil reste la même quelle que soit la fonction rénale, parce que l’acide de rémifentanil est à peu près inactif1,2.
Les effets secondaires du rémifentanil ressemblent à ceux des autres opioïdes (Figure 2).
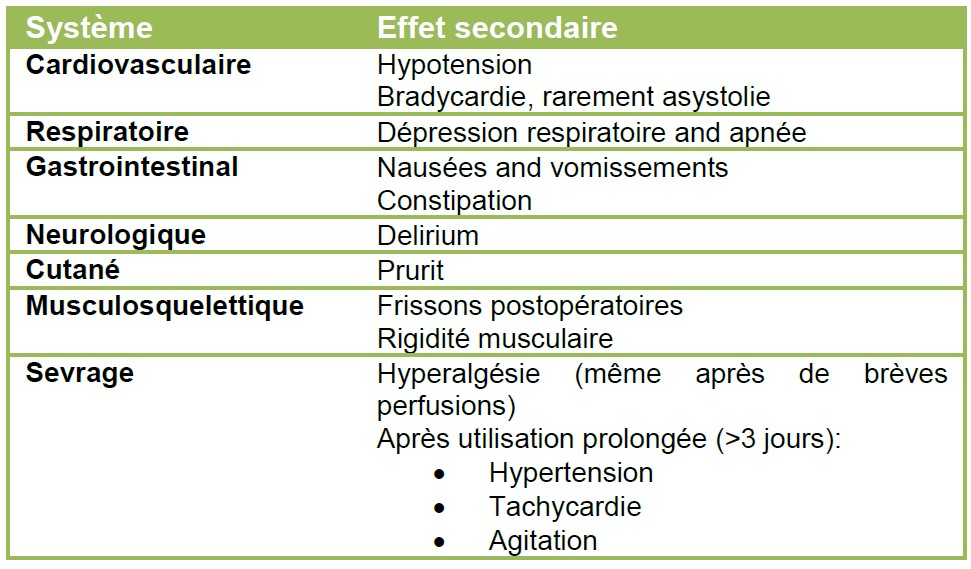
Figure 2. Effets secondaires du rémifentanil
Le rémifentanil procure une anesthésie et une analgésie intraopératoires plus profondes que les autres opoïdes à courte action (fentanyl, alfentanil and sufentanil)3, avec une tension artérielle et un pouls moindres3. Les doses élevées de rémifentanil sont associées à un risque accru d’hypotension, de bradycardie et d’apnée3. Il est prudent d’avoir des vasopresseurs et des anticholinergiques à disposition lorsqu’on utilise le rémifentanil.
On observe de l’hyperalgésie postopératoire en association avec des doses élevées de rémifentanil4. Ce phénomène pourrait être expliqué en partie par une analgésie postopératoire insuffisante. Il est suggéré d’administrer de la morphine (0,15–0,3mg.kg-1) ou un équivalent, au moins 30 minutes avant de cesser le rémifentanil pour permettre l’atteinte de l’effet maximum. En dépit d’un recours occasionnel à une analgésie de secours, on a rarement besoin de naloxone suite à une utilisation intraopératoire de rémifentanil3. Les nausées et vomissements se produisent à la même fréquence qu’avec les autres opioïdes à courte action, mais ils semblent se produire moins souvent dans le cadre d’une anesthésie intraveineuse totale. Les frissons postopératoires surviennent deux fois plus souvent avec le rémifentanil3.
La pharmacocinétique du rémifentanil suit plus étroitement le poids maigre que le poids réel1. Certes, les patients obèses ont besoin d’une dose plus élevée que ce que laisserait croire leur poids maigre, mais bien moindre que celle que l’on obtiendrait en se basant sur le poids réel. Une telle dose entraînerait un risque de dépression cardiovasculaire1.
Le modèle de Minto
Les pompes à perfusion à objectif de concentration ajustent la vitesse de perfusion pour atteindre une concentration stable au site effecteur, en prenant en compte la pharmacocinétique connue du médicament et certaines caractéristiques physiques du patient. Le modèle de Minto, du nom de l’un de ces concepteurs, le Dr Charles Minto, prédit la concentration de rémifentanil dans le plasma et au site effecteur. Il existe des modèles plus précis (le modèle de Minto prédit des valeurs jusqu’à 15% supérieures à la réalité5), mais le modèle de Minto est le plus populaire à cause de sa flexibilité et de la vaste expérience acquise avec ce modèle.
Le modèle de Minto est à trois compartiments et cible soit le site effecteur (Cet) ou le site plasmatique (Cpt). La constante de diffusion pour le Cet (keo) et pour la perte de conscience a été obtenue par des mesures de l’électroencéphalogramme (EEG). La dose bolus initiale injectée selon le mode Cet est 3-4 fois plus grande que celle donnée selon le mode Cpt. Cette dose plus élevée pourrait donner lieu à plus d’effets secondaires (rigidité thoracique, bradycardie, apnée). On peut souvent atténuer ces effets en administrant la dose initiale par paliers jusqu’à l’atteinte du Cet voulu et la bradycardie peut être contrôlée en donnant du glycopyrrolate en prophylaxie. On recommande aux cliniciens peu familiers avec l’administration de rémifentanil en mode AIVOC d’utiliser le Cpt plutôt que le Cet.
Les pompes AIVOC basées sur un modèle comme celui de Minto ont un avantage sur celles qui utilisent le “mcg.kg-1.min-1”, parce qu’ils tiennent compte de plusieurs caractéristiques du patient, et pas seulement le poids réel, pour prédire la pharmacocinétique du rémifentanil chez un individu donné. Pour le modèle de Minto, on doit spécifier le sexe du patient, son âge, son poids (kg) et sa taille (cm), pour calculer le poids maigre. Ce modèle n’est pas adapté à la plupart des enfants, puisqu’il fonctionne que pour les patients de plus de 12 ans et pesant plus de 30 kg; malheureusement, il n’y a pas de modèles couramment disponibles pour les enfants, mais cette situation pourrait changer dans l’avenir. L’influence de l’âge est déterminante, parce la pharmacocinétique du rémifentanil varie grandement avec l’âge; par exemple, à 85 ans, le volume de distribution est diminué de 25% et la clairance du tiers par rapport aux valeurs à 20 ans6. Une attention spéciale doit être portée aux patients âgés et fragiles pour réduire les complications cardiovasculaires et respiratoires. On y arrive plus facilement avec l’AIVOC qu’avec la technique plus simple du mcg.kg-1.min-1.
Le graphique et le tableau ci-dessous (figure 3) illustrent les concentrations de rémifentanil dans le sang, prédites par le modèle de Minto, en fonction des vitesses de perfusion chez un homme de 70 kg, mesurant 170 cm et âgé de 40 ans.
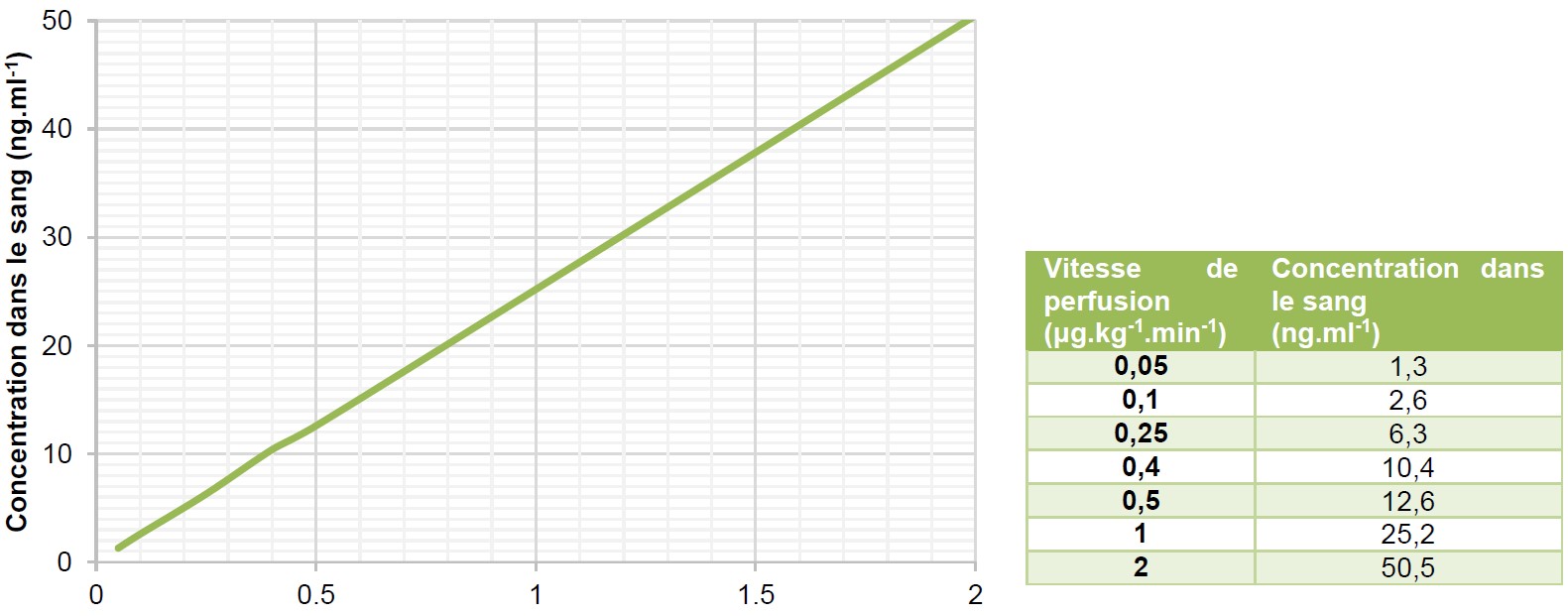
Figure 3 Vitesse de perfusion (μg.kg-1.min-1)
APPLICATIONS CLINIQUES
Anesthésie générale
Pour l’anesthésie générale, on a besoin d’une Cet de 3 à 10 ng.ml-1, soit environ 0,1 à 0,3 μg.kg-1.min-1. Le monitorage de l’index bispectral (BIS) fournit une autre façon d’ajuster la dose: si le BIS s’éloigne de la plage de valeurs acceptables (par exemple <40 or >55), la perfusion de rémifentanil est augmentée ou diminuée de 0,05 ng.ml-1.
À cause de ses puissants effets dépresseurs sur la respiration, il peut être difficile d’atteindre une respiration spontanée avec une AIVOC au rémifentanil, particulièrement à des vitesses de perfusion élevées. Sous anesthésie générale intraveineuse avec une technique associant le rémifentanil et le propofol, il est recommandé, pour maintenir une respiration spontanée, de choisir une vitesse de perfusion plutôt élevée pour le propofol (Cet 4-6 μg.ml-1) et une vitesse de perfusion assez basse pour le rémifentanil (Cet 2,5ng.ml-1). Lorsque l’on a obtenu une respiration spontanée, on peut augmenter la dose de rémifentanil par petits paliers (par ex. 0,05 ng.ml-1) jusqu’à l’atteinte d’une analgésie suffisante. Dans ce cas, la fréquence respiratoire peut être un reflet de l’analgésie, une fréquence de 10 à 15 respirations par minute indiquant une analgésie suffisante.
Le rémifentanil est particulièrement indiqué pour l’anesthésie intraveineuse totale; il est sécuritaire pour l’hyperthermie maligne et diminue le recours à de fortes doses de propofol à cause d’une synergie entre les deux médicaments7. La posologie du rémifentanil dépend de l’expérience clinique, de la préférence de l’utilisateur, du patient et de l’intervention. Grosso modo, le Cet du propofol est maintenu entre 2 et 4 μg.ml-1 pour assurer l’anesthésie et celle du rémifentanil entre 6 et 12 ng.ml-1 (peu de propofol, beaucoup de rémifentanil); ou encore on choisit 5-6 μg.ml-1 pour le propofol et 0,5-3 ng.ml-1 pour le rémifentanil (beaucoup de propofol, peu de rémifentanil) pour les interventions nécessitant peu d’analgésie ou pour les patients chez qui on veut garder une respiration spontanée7. Habituellement l’éveil est plus rapide avec une technique combinant peu de propofol et beaucoup de rémifentanil8. Les patients jeunes, musclés et en santé ont besoin de plus de rémifentanil, tout comme ceux qui subissent des chirurgies douloureuses, qui ont une histoire de douleur chronique ou qui abusent de drogues intraveineuses. Avec des concentrations élevées de rémifentanil, il faut garder à l’esprit la possibilité d’effets secondaires cardiovasculaires et respiratoires.
Attention : il est important que le poids idéal utilisé par le modèle de Minto au début de l’intervention se rapproche de celui du patient et soit exact, surtout si le sujet est obèse morbide. Le poids idéal calculé par la pompe AIVOC selon l’équation de James est précis jusqu’à un IMC de 42 chez les hommes et de 37 chez les femmes; au-delà de ces valeurs, une diminution paradoxale du poids idéal se produit. Si le poids idéal estimé est trop bas, une confusion survient : le patient semble avoir besoin de beaucoup plus de rémifentanil que prévu pour la valeur du BIS et le stade de la chirurgie. Si cette erreur se produit, le poids ne peut être changé en cours d’intervention sans effacer le modèle en entier; ainsi, il est important d’estimer le poids idéal dès le début. L’équation de Janmahasatian est plus compliquée, mais pourrait donner un estimé du poids idéal plus précis chez les obèses morbides, quoique cette méthode ne fait pas l’unanimité8. Certains préconisent la formule de Servin ou la méthode de Lemmens, obtenant ainsi un compromis acceptable pour le poids idéal ajusté, entre le poids réel (qui peut être trop) et le poids idéal (insuffisant)9,10. Ces formules sont souvent utilisées pour les modèles d’AIVOC au propofol, mais peuvent aussi convenir au rémifentanil9,10. Il est important, dans la mesure du possible, de s’assurer que le patient a été bien pesé peu avant la chirurgie et de ne pas se fier à des poids estimés, lesquels peuvent être remarquablement imprécis.
Résumé des différentes formules utilisées pour calculer le poids idéal (IBW) ou le poids maigre (LBW) (pour référence) (tous les poids en kg) 8,9,10:
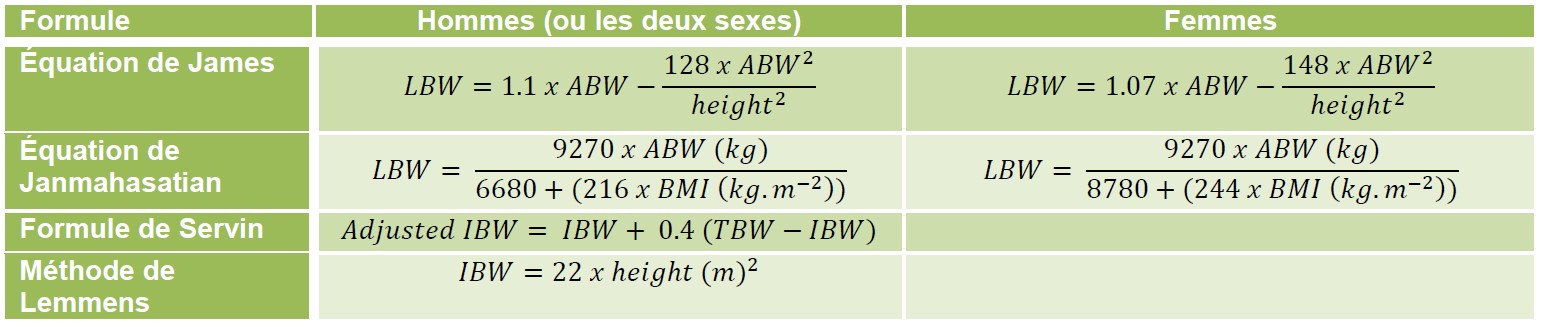
ABW: poids réel; height: taille; adjusted: ajusté
Le rémifentanil a une demi-vie contextuelle relativement courte de seulement 3 à 4 minutes11. En pratique, on doit compter environ 6-12 minutes avant qu’un patient revienne en respiration spontanée après avoir cessé le rémifentanil ou après avoir ciblé un Cet bas (environ 2,5 ng.ml-1). Ce délai est influencé par plusieurs facteurs, comme le Cet au moment où la perfusion est cessée et la présence d’autres médicaments qui dépriment la respiration. Il est important de prendre ces facteurs en compte pour estimer le moment de l’éveil, afin de s’assurer que les patients respirent et émergent de l’anesthésie au bon moment et correctement à la fin de la chirurgie. Cette prévisibilité du rémifentanil le rend utile pour des interventions prolongées lorsqu’on veut un éveil rapide, par exemple en neurochirurgie, chez des patients obèses ou quand on essaie d’éviter une dépression respiratoire postopératoire, notamment chez les patients souffrant d’apnée du sommeil.
On a décrit une technique d’induction en séquence rapide modifiée avec du rémifentanil (Cet 4-6ng.ml-1) en le combinant avec un hypnotique (kétamine, thiopental ou propofol) et de la succinylcholine ou du rocuronium.
Intubation sans curare
Le rémifentanil diminue considérablement les réflexes des voies aériennes supérieures et permet la plupart du temps une intubation trachéale sans curare, tant chez les adultes que chez les enfants. D’après notre expérience, cette technique fonctionne mieux avec une anesthésie intraveineuse qu’avec des agents volatils. Même s’il existe une controverse à ce sujet, il pourrait y avoir des avantages à omettre les curares dans certaines situations, par exemple :
- Dans le cas de sensibilité accrue aux curares (allergie, myasthénie grave, hyperthermie maligne, etc)
- Si un neurostimulateur est utile pour la chirurgie, par exemple pour vérifier l’intégrité du nerf facial dans les opérations de la mastoïde ou de la parotide ou pour réaliser un bloc locorégional après l’induction
- Pour éviter la curarisation résiduelle ou la recurarisation
- Pour diminuer le risque d’éveil peropératoire.
Voici notre recette pout l’intubation utilisant le rémifentanil:
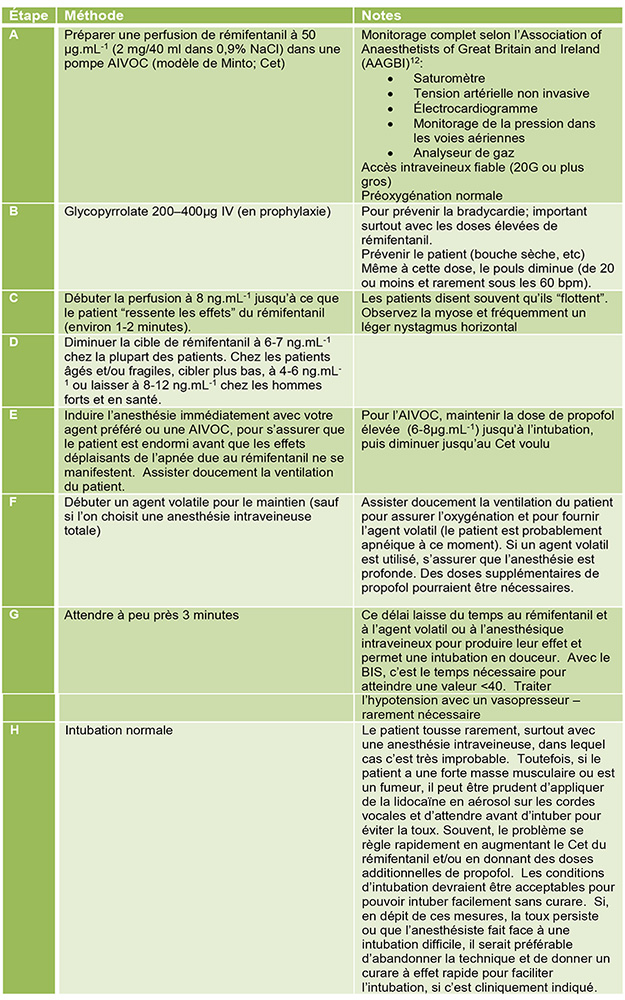
Figure 4. Protocole d’intubation suggéré avec le rémifentanil sans curare
Obstétrique
Bien que l’analgésie par voie péridurale demeure la technique utilisée en première intention pour le travail, l’analgésie au rémifentanil contrôlée par la patiente (ACP) est prudemment acceptée quand la péridurale est contrindiquée (Figure 5). On a montré que le rémifentanil est associé à des scores de satisfaction équivalents ou meilleurs que la péridurale chez les parturientes13, peut-être à cause d’une facilité apparente d’administration et d’une efficacité rapide pour le rémifentanil.
Le rémifentanil traverse la barrière placentaire, mais il est métabolisé et redistribué rapidement chez le foetus, même prématuré13. Chez la mère, le rémifentanil possède un effet dépresseur sur la respiration et sur l’état de conscience plus prononcé que les autres opioïdes; ceci doit être expliqué aux parturientes et une surveillance constante doit être exercée par les cliniciens et les sages-femmes sur un mode 1:1. Le monitorage de la saturométrie est obligatoire; de l’oxygène et du matériel de réanimation doivent être disponibles immédiatement, tout comme du personnel formé à son utilisation4. Il n’y a pas de différence de mortalité ou de morbidité maternelle ou néonatale quand on compare la péridurale à l’ACP au remifentanil; toutefois, il est prudent d’aviser l’équipe de néonatologie que du rémifentanil a été utilisé pendant le travail, au cas où le nouveau-né aurait besoin de réanimation13.

Figure 5
Aussi, le rémifentanil peut être utile dans le cadre d’une césarienne urgente pour éviter l’hypertension produite par la laryngoscopie chez les patientes éclamptiques15. Pour cet aspect de technique à séquence rapide, une Cet cible à 4-6 ng.ml-1 devrait suffire. On a aussi préconisé des doses uniques de rémifentanil (0,6-1,3 μg.kg-1), mais il faut être prudent, car le rémifentanil est injecté beaucoup plus rapidement avec un bolus qu’avec l’AIVOC, ce qui peut produire des effets secondaires cardiovasculaires, une rigidité thoracique et une apnée.
Intubation vigile à fibre optique (IVFO)
L’IVFO est une technique utile pour l’intubation difficile. Les objectifs de l’IVFO sont d’obtenir des conditions optimales d’intubation, de maintenir une respiration spontanée chez un patient calme et confortable, tout en gardant la possibilité de revoir la technique et de faire marche arrière. Le rémifentanil est un outil utile pour l’IFVO, rendant le processus plus facile et plus acceptable pour les patients.
La figure 6 illustre notre recette pour l’IFVO avec le rémifentanil. À noter que dans cet article, on se limite à l’aspect sédation, la technique de l’IFVO et ses complexités étant décrites dans un autre article (ATOTW 201).
Sédation consciente
Le rémifentanil peut être utilisé dans de nombreux cas où une sédation consciente est nécessaire, tels que:
- Extractions dentaires simples
- Réduction de fracture ou de luxation
- Changement de pansements chez les brûlés
- Trachéostomie vigile
- Bronchoscopie
- Technique locorégionale partiellement efficace ou dont l’effet se dissipe
L’utilisation sécuritaire du rémifentanil commence avec le choix judicieux du patient. Le rémifentanil ne convient pas à tous les patients qui pourraient avoir une intubation difficile, qui sont obèses morbides, qui ne sont pas à jeun ou qui pourraient subir une longue intervention. La technique doit aussi être entreprise dans un lieu où se trouve du matériel pour traiter les complications, en conformité complète avec les exigences de monitorage et de réanimation de l’AAGBI9. Il existe deux écoles de pensée concernant la pertinence de donner de l’oxygène pendant la sédation consciente. D’un côté, la présence d’un réservoir d’oxygène dans les poumons est utile en cas de difficultés respiratoires. En revanche, une chute précoce de la saturation en oxygène aide au diagnostic de sédation exagérée, menant plus rapidement à un ajustement à la baisse de la perfusion de rémifentanil et à des appels au patient à respirer.
Notre recette de sédation consciente est fondamentalement la même que pour les étapes A-D de l’IVFO plus haut (Figure 6). Toutefois, répétons-le, il ne faut pas se presser – laissez au moins 2-3 minutes au patient pour répondre à toute augmentation de dose. Évitez les bolus non contrôlés parce qu’ils peuvent produire des bradycardies sévères et des apnées, surtout chez les adultes. N’oubliez pas le glycopyrrolate en prophylaxie. Assurez-vous de l’exactitude du poids idéal du patient selon le modèle de Minto.
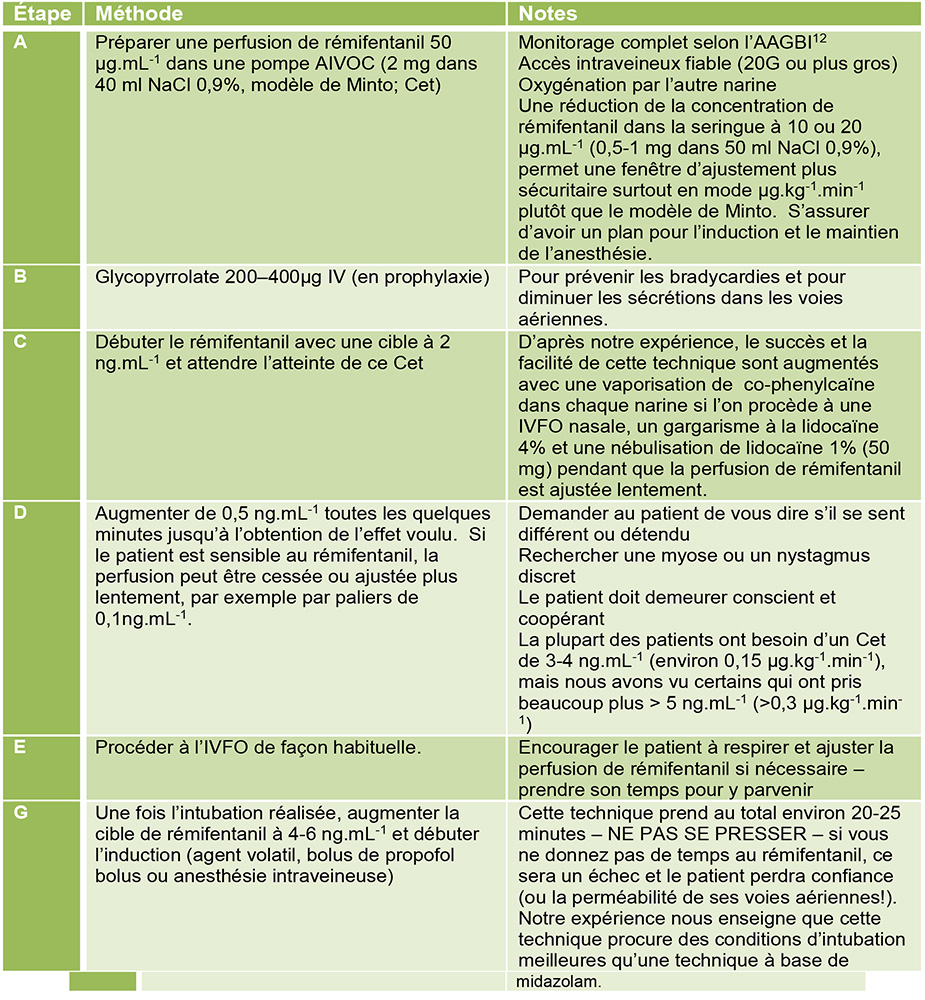
Figure 6. Protocole suggéré pour le rémifentanil dans le cadre d’une intubation vigile à fibre optique
Soins intensifs
Une analgésie et une sédation optimales jouent un rôle important dans la prise en charge des patients aux soins intensifs. Pour y arriver, on donne habituellement du propofol et un opioïde (souvent l’alfentanil au RU). Les données probantes penchent de plus en plus vers la notion que des pauses de sédation et des essais de respiration spontanée mènent à des séjours plus courts aux soins intensifs et à un meilleur pronostic16,17,18. Le rémifentanil possède de nombreux avantages comparativement aux autres opioïdes à courte action. Ainsi, plusieurs unités de soins intensifs le choisissent en première intention. Parmi ces avantages, on retrouve:
- Une durée d’action brève permettant un examen neurologique pendant les pauses de sédation.
- Une dépression respiratoire profonde, évitant ainsi une asynchronie ventilatoire – un problème moins important avec les nouveaux modes de ventilation.
- Une demi-vie contextuelle très brève et peu d’accumulation (contrairement à l’alfentaniil et à la morphine) – idéal pour la reprise rapide de la respiration spontanée2.
- Aucun ajustement nécessaire dans les cas d’atteinte rénale aiguë ou chronique – l’effet se dissipe à peu près deux fois plus lentement en cas d’atteinte rénale modérée à sévère, mais la différence n’est que de 16,5 min, ce qui normalement n’est pas significatif2.
- Un effet qui se dissipe de façon plus prévisible en cas d’atteinte multi-organe.
Avec la disponibilité accrue du rémifentanil, les coûts ont baissé de sorte qu’il y a peu de différence entre le coût du rémifentanil et celui de l’alfentanil pour une perfusion de 24 h. (Prix au RU; rémifentanil = £5.72 pour 2 mg, alfentanil = £3.20 for 5 mg19). Nous utilisons le rémifentanil avec le propofol en première intention pour l’analgésie et la sédation aux soins intensifs.
Les inconvénients du rémifentanil aux soins intensifs peuvent être gérés de façon sécuritaire et ne devraient pas être un frein à son utilisation. Ces inconvénients sont notamment:
- Une possibilité d’hyperalgésie et de syndrome de sevrage après l’arrêt de la perfusion de rémifentanil, nécessitant le recours à une analgésie de relais avant une diminution de posologie.
- Un risque potentiel d’apnée et/ou de rigidité thoracique (à forte dose), rendant la ventilation plus difficile. Le risque d’apnée doit être pris au sérieux, surtout chez les patients non intubés. Ainsi, le personnel doit demeurer vigilant et avoir un plan d’action au cas où des apnées surviendraient.
- Une instabilité cardiovasculaire (hypotension et bradycardie) peut justifier un recours accru aux vasopresseurs ou aux inotropes.
Le rémifentanil convient moins aux patients non intubés. Toutefois, chez des patients choisis avec soin et avec un personnel expérimenté, l’utilisation du rémifentanil aux soins intensifs chez des patients non intubés devrait augmenter, par exemple pour faciliter l’acceptation de la ventilation non invasive, pour procurer une l’analgésie optimale pour un bref changement ou rotation de pansement et pour améliorer l’analgésie pendant des interventions invasives.
Les vitesses de perfusion recommandées chez les patients ventilés pour une perfusion continue de rémifentanil aux soins intensifs seraient de 0,1 – 0,15 μg.kg-1.min-1 (6 – 9 ng.mL-1), en plus d’une perfusion de propofol. Chez les patients non ventilés, une perfusion de 0,05-0,1μg.kg-1.min-1 serait plus adaptée, dépendant du patient. Un protocole d’utilisation de rémifentanil aux soins intensifs peut permettre aux infirmières de choisir les doses et de procéder au sevrage.
CONSEILS DE SÉCURITÉ POUR LE RÉMIFENTANIL
- Ne pas donner de bolus – utiliser le modèle de Minto et changer les vitesses de perfusion au besoin.
- Une prémédication avec un anticholinergique (glycopyrolate 200 – 400 μg) ou un sympathomimétique (éphédrine 3 – 6 mg) aide à contrecarrer la bradycardie.
- S’assurer de la fiabilité de l’accès intraveineux et des pompes à perfusion; changer les seringues rapidement – l’effet du rémifentanil s’estompe rapidement, ce qui peut devenir un problème si la perfusion s’arrête inopinément.
- Enveler ou changer les solutés et purger les canules à la fin de l’opération pour éviter une injection par erreur à la salle de réveil ou encore pire, à l’unité de soins.
- Être patient et ajuster lentement les doses de rémifentanil pour la sédation consciente et pour l’IVFO. L’impatience est souvent source d’effets secondaires.
RÉSUMÉ
Le rémifentanil est un excellent médicament, qui possède la flexibilité voulue pour des applications en anesthésie et aux soins intensifs. Avec une formation du personnel et un usage adapté, le rémifentanil peut améliorer le déroulement des cas et au final la qualité des soins fournis à nos patients.
RÉPONSES AUX QUESTIONS
- Au sujet de la pharmacologie du rémifentanil:
- Vrai: La pharmacocinétique est plus étroitement liée au poids maigre qu’au poids réel
- Faux: Pas d’ajustement de dose nécessaire en cas de défaillance rénale
- Faux: Les frissons en postopératoire surviennent deux fois plus souvent avec le rémifentanil
- Vrai: La demi-vie du remifentanil est d’environ 3 minutes.
- Faux: Le rémifentanil est dégradé par les estérases plasmatiques et tissulaires non spécifiques. Ses effets ne sont pas prolongés en cas de déficit en pseudocholinestérase
- Au sujet de l’anesthésie intraveineuse à objectif de concentration (AIVOC):
- Faux: Le modèle de Minto est utilisé pour le rémifentanil en AIVOC alors que le modèle de Marsh est utilisé pour le propofol
- Faux: Il faut aussi spécifier l’âge dans le modèle de Minto
- Vrai: Le rémifentanil possède une action synergique avec le propofol, ce qui permet d’administrer une concentration plus faible de ce dernier pour une anesthésie intraveineuse
- Faux: Il faut 2 – 8 nanogrammes par ml (ng. ml-1) pas des microgrammes par ml (μg.ml-1)
- Faux: La dose de bolus est de trois à quatre fois plus élevée avec le site effecteur comme cible (Cet) qu’avec la concentration plasmatique (Cpt) comme cible
- Parmi les applications cliniques du rémifentanil, on retrouve:
- Vrai
- Faux: Surtout, à NE PAS essayer!
- Vrai
- Vrai
- Vrai: Toutefois, la sécurité des patientes exige une vigilance constante auprès des parturientes utilisant l’ACP au rémifentanil
RÉFÉRENCES ET BIOBLIOGRAPHIE
- Egan TD. Pharmacokinetics and pharmacodynamics of remifentanil: an update in the year 2000. Current Opinion in Anaesthesiology. 2000, 13:449-455.
- Breen D, Wilmer A, Bodenham A, Bach V, Bonde J, Kessler P, Albrecht S, Shaikh S. Offset of pharmacodynamic effects and safety of remifentanil in intensive care unit patients with various degrees of renal impairment. Critical Care. 2004, 8:R21-R30.
- Komatsu R, Turan AM, Orhan-Sungur M, McGuire J, Radke OC, Apfel CC. Remifentanil for general anaesthesia: a systematic review. Anaesthesia 2007; 62: 1266-1280.
- Fletcher D, Martinez V. Opioid-induced hyperalgesia in patients after surgery: a systematic review and a meta-analysis. British Journal of Anaesthesia 2014; 112(6): 991 – 1004.
- Mertens MJ, Engbers FHM, Burm AGL, Vuyk J. Predictive performance of computer-controlled infusion of remifentanil during propofol/remifentanil anaesthesia. British Journal or Anaesthesia 2003; 90(2): 132-141.
- Minto CF, Schnider TW, Egan TD et. al. Influence of age and gender on the pharmacokinetics and pharmacodynamics of remifentanil. Model development. Anesthesiology. 1997; 86(1): 10-23.
- Mertens MJ, Olofsen E, Engbers FH, Burm AG, Bovill JG, Vuyk J. Propofol reduces perioperative remifentanil requirements in a synergistic manner: response surface modeling of perioperative remifentanil-propofol interactions. Anesthesiology. 2003; 99(2): 347-59.
- Tahari AK, Chien D, Azadi JR, et al. Optimum Lean Body Formulation for Correction of Standardised Uptake Value in PET Imaging. Journal of Nuclear Medicine. 2014; 55: 1-4
- Albertin A, Poli D, La Colla L, et al. Predictive performance of ‘Servin’s formula’ during BIS-guided propofol-remifentanil target-controlled infusion in morbidly obese patients. British Journal of Anaesthesia. 2007; 98(1): 66-75
- Lemmens HJ, Brodsky JB, Bernstein DP. Estimating ideal body weight – a new formula. Obesity Surgery. 2005; 15(7): 1082-3
- Milne SE, Kenny GNC, Schraag S. Propofol sparing effect of remifentanil using closed-loop anaesthesia. British Journal of Anaesthesia. 2003; 90(5): 623-9
- Checketts MR, Alladi R, Furguson K et al. Recommendations for standards of monitoring during anaesthesia and recovery 2015: Association of Anaesthetists of Great Britain and Ireland. Published: December 2015.
- Freeman LM, Bloemenkamp KW, Franssen MT et al. Patient controlled analgesia with remifentanil versus epidural analgesia in labour: randomized multicenter equivalence trial. British Medical Journal. 2015;350:h846
- Douma MR, Verwey RA, Kam-Endtz CE, van der Linden PD, Stienstra R. Obstetric analgesia: a comparison of patient-controlled meperidine, remifentanil, and fentanyl in labour. British Journal of Anaesthesia. 2009; doi: 10.1093/bja/aep359
- Yoo KY, Kang DH, Jeong H, Jeong CW, Choi YY, Lee J. A dose-response study of remifentanil for attenuation of the hypertensive response to laryngoscopy and tracheal intubation in severely preeclamptic women undergoing caesarean delivery under general anaesthesia. International journal of obstetric anaesthesia. 2013; 22: 10-18.
- Girard T, Kress J, Fuchs B, Thomason J, Schweickert W, Pun B et al, Efficacy and safety of a paired sedation and ventilator weaning protocol for mechanically ventilated patients in intensive care (Awakening and Breathing Controlled trial): A randomised controlled trial. Lancet. 2008; 371: 126-134.
- Reade MC, Finfer S. Sedation and delirium in the Intensive Care Unit. New England Journal of Medicine. 2014; 370: 444-54.
- Barr J, Fraser GL, Puntillo K, et al. Clinical practice guidelines for the management of pain, agitation, and delirium in adult patients in the intensive care unit. Critical Care Medicine. 2013; 41: 263-306.
- Paediatric Formulary Committee. BNF for Children September 2016. London: BMJ Group, Pharmaceutical Press, and RCPCH Publications; 2016



