Intensive Care Medicine
Pontos-chave
- A cetamina é um agente anestésico que, dependendo da dosagem, serve como analgésico, sedativo, anestésico de indução ou anestésico de manutenção.
- A cetamina tem vantagens específicas sobre alguns outros agentes anestésicos. Os reflexos e o tônus das vias aéreas são geralmente preservados durante a sedação com cetamina e o perfil hemodinâmico possui característica única.
- A cetamina tem indicação em cuidados pré-hospitalares, emergenciais e críticos e é amplamente usada por anestesistas no mundo inteiro.
- As pesquisas mostram que o uso de isômeros ópticos da cetamina ajuda a reduzir efeitos adversos.
- A cetamina parece possuir propriedades anti-inflamatórias, broncodilatadores e neuroprotetoras.
Introdução
A cetamina é um potente analgésico e agente anestésico do tipo dissociativo usado desde a sua descoberta e sintetização em 1962. A sua popularidade deve-se à sua extraordinária capacidade de produzir efeitos sedativos, analgésicos e amnésicos rápidos e às suas qualidades secundárias benéficas. Estas incluem broncodilatação e manutenção dos reflexos das vias aéreas e do tônus do sistema nervoso simpático.1 Estudos recentes apontam para a existência de propriedades neuroprotetoras2 e anti-inflamatórias3 previamente desconhecidas.
Devido às suas propriedades e versatilidade, a cetamina é uma opção cada vez mais popular em cuidados pré-hospitalares e emergenciais e é amplamente usada por anestesistas e seus assistentes no mundo todo. Os usos mais recentes incluem protocolos de baixas doses de analgésicos, terapia adjuvante em bloqueios anestésicos de nervos locais, tratamento de doença reativa das vias aéreas, e sedação em centros cirúrgicos, serviços de emergência e unidades de cuidados críticos.
Apesar de todas essas vantagens, a sua popularidade não é hegemônica devido a preocupações com reações adversas ao final do procedimento, ao seu potencial para abuso e à disponibilidade de outras drogas sedativas e analgésicas.
Pesquisas com isômeros da cetamina, tais como S(+) cetamina possibilitaram o uso de doses mais baixas, sem prejuízo do efeito.4 Segundo relatos ocorre redução daa incidência dos efeitos colaterais psicoativos convencionais sem abrir mão dos efeitos desejados.5
O presente tutorial aborda a farmacologia e diversos usos da cetamina, com referência à literatura atual.
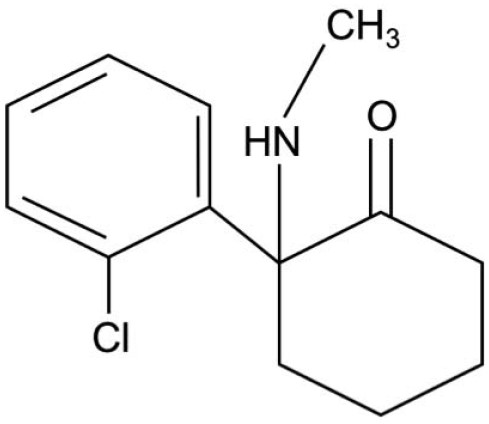
Figura 1: Estrutura química da cetamina. O centro quiral no anel de ciclo-hexanona permite a existência dos isômeros S e R.
Farmacologia
A cetamina é derivada de agentes anestésicos da ciclo-hexamina (fenciclidina), comumente usados nos anos 50. É um antagonista do receptor NMDA do tipo não competitivo; bloqueia o sítio de ligação de fenciclidina no receptor NMDA o que por sua vez impede a despolarização do neurônio. Os receptores do NMDA são localizados nos níveis espinhal, talâmico, límbico e cortical. Por isso, a cetamina interfere com o input sensorial nos centros superiores do SNC, afetando as respostas de dor, emotivas e da memória (daí a definição como “anestésico dissociativo”).6 A cetamina também apresenta efeitos secundários sobre os receptores de opióides, os quais ajudam a propagar seu efeito analgésico, bem como sobre os receptores alfa, beta e de catecolamina.
Fórmula estrutural
A cetamina (Figura 1) tem um centro quiral no carbono C-2 do anel de ciclo-hexanona; logo, existem dois isômeros ópticos: S (+) e R (-), o primeiro dos quais é o mais ativo, farmacologicamente.
No Reino Unido, a cetamina está geralmente disponível na forma de solução racêmica, i.e. uma mistura dos isômeros R (-) e S (+) em quantidades iguais. Está disponível em várias concentrações (10, 50 e 100 mg mL-1). O isômero óptico cetamina S (+) (5 e 25 mg mL-1) não é atualmente comercializado no Reino Unido, mas pode ser encontrado em vários países europeus e no Brasil.
Farmacocinética
Distribuição
A cetamina é altamente lipossolúvel, mas tem pouca capacidade de ligação protéica. Essa característica permite uma rápida passagem pela barreira hematoencefálica, levando a concentrações de 4 a 5 vezes maiores que no plasma. A meia-vida de distribuição é de 7 a 11 minutos, aproximadamente.
Metabolismo e eliminação
A maior parte da cetamina (80%) é metabolizada no fígado, produzindo norcetamina. Esta última também possui propriedades analgésicas, porém fracas (20 a 30% da potência da cetamina). O pico da concentração sanguínea da norcetamina é atingido cerca de 30 minutos após a administração intravenosa. Em seguida, a norcetamina é primariamente hidrolisada por meio de glucurono-conjugação e excretada pela urina e pela bilis.5
Farmacodinâmica
Sistema nervoso central
A cetamina produz um estado de transe cataléptico, com sedação e analgesia potentes. De 30 a 50% dos pacientes apresentam sinais e sintomas ao despertar, especialmente quando a dose é alta. Os sintomas incluem desconforto, alucinações, sonhos vívidos, sensação de estar flutuando e delírio.
Sistema cardiovascular
A cetamina parece estimular o sistema nervoso simpático, causando taquicardia e aumentando o débito cardíaco e a pressão arterial. Portanto, deve ser usado com cautela em pacientes com doença cardíaca isquêmica. O mecanismo responsável não é bem conhecido, mas alguns acreditam que a cetamina possa inibir a reabsorção das catecolaminas circulantes. Em pacientes com depleção crônica de catecolaminas (p.ex. pacientes criticamente doentes) foi observado que a cetamina, isoladamente, na verdade causa um efeito inotrópico negativo. Em pacientes com controle autonômico normal, o efeito inotrópico negativo direto é frequentemente suplantado pela resposta simpática central,1 levando a um aumento global ou manutenção da pressão arterial.6
Sistema respiratório
Diferentemente de outros agentes sedativos e anestésicos, o uso da cetamina geralmente preserva o tônus das vias aéreas e os reflexos laríngeos e faríngeos, porém em crianças com menos de 12 meses de idade, os reflexos das vias aéreas são mais variáveis e imprevisíveis.7 A cetamina pode apresentar leve efeito respiratório depressivo através da redução da resposta ao aumento dos níveis de PaCO2. Isso é particularmente perceptível após a administração de grandes bolus i.v., situação em que foi observada apneia transitória.8 A cetamina também pode causar broncodilatação, de modo que é o agente indutor de escolha em pacientes asmáticos graves necessitados de ventilação mecânica.
Outros efeitos
A cetamina aumenta o tônus muscular, os níveis sanguíneos de glicose e os níveis plasmáticos de cortisol e prolactina.6 Um efeito colateral potencialmente preocupante é aumento da salivação. Alguns autores recomendam a co-administração de anti sialogogos (geralmente atropina).9
Usos e evidências atuais
Sedação
A cetamina é cada vez mais usada para fazer analgesia e sedação em procedimentos pré-hospitalares e emergenciais. É ideal para o manejo de eventos traumáticos (p.ex. na redução de fraturas e tratamento de queimaduras). O estado dissociativo característico da cetamina pode ser alcançado com doses entre 0,25 e 1,5 mg·kg-1 i.v.
Para sedação de emergência, recomenda-se uma dose de ataque administrada durante 30 a 60 segundos. Isso produz sedação dentro de 1 minuto, com duração de 5 a 10 minutos. A dose de ataque recomendada varia muito: de 0,25 a 1,0 mg kg-1 i.v. em adultos e de 0,25 a 2,0 mg kg-1 i.v. em crianças.4 As doses maiores são comumente usadas para a indução de anestesia geral. Uma dose única é adequada em procedimentos curtos, mas em procedimentos mais demorados, o estado dissociativo pode ser mantido com bolus intermitentes de 0,5 mg kg-1. Existem diretrizes clínicas detalhadas sobre o uso de cetamina em serviços de emergência,10 mas, como no uso de qualquer medicação anestésica são necessárias observação e monitorização adequada. A monitorização mínima (quando disponível) deve ser contínua e incluir eletrocardiografia, pressão arterial não-invasiva, oxigênio saturado e CO2 expirado.
A cetamina pode ser usada com segurança em combinações com outras drogas de indução ou sedação, p.ex. propofol. A combinação cetamina e propofol reduz em cerca de 50% a dose necessária de cada droga,4 e reduz a incidência e a gravidade dos efeitos colaterais de ambas. Acredita-se que, através de sua ação simpaticomimética, a cetamina reduz a hipotensão induzida por propofol, ao passo que o propofol reduz a incidência de agitação pós-cirúrgica observada com cetamina isoladamente. Recentes ensaios randomizados controlados mostram sedação melhor quando as drogas são combinadas do que quando o propofol é usado isoladamente.11
Se o acesso intravenoso for difícil, a cetamina pode ser administrada por via intramuscular, oral ou intranasal, com bom esultado. Nesse caso, o tempo para o início do efeito é usualmente mais longo do que na aplicação i.v., e há maior variabilidade na dose exigida devido a variações de vascularidade e absorção gastrointestinal (Tabela 1). O uso oral de cetamina, sozinha ou em combinação com paracetamol e diazepam, é uma opção em casos de trocas de curativos (especialmente queimaduras), minimizando o uso da sala cirúrgica. Com o uso repetido, é observada um certo grau de taquifilaxia.
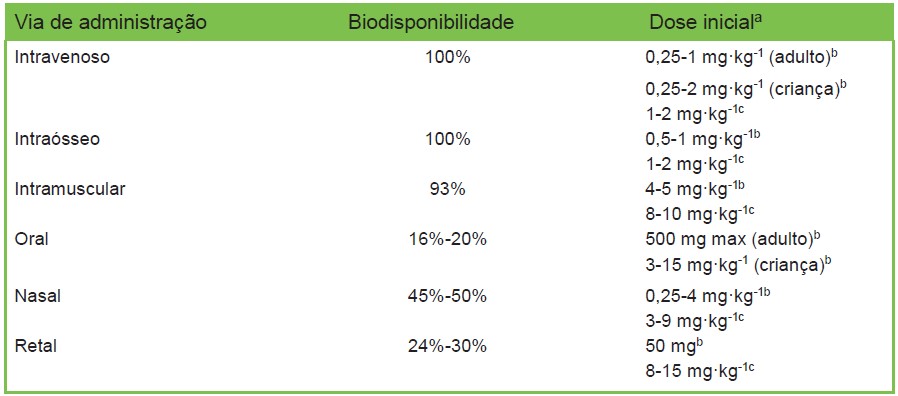
Tabela 1: Vias de administração de cetamina e faixas de dosagem em crianças e adultos (fonte: Marland & Ellerton).4 A doses acima produzem uma variedade de efeitos, de sedação leve a indução anestésica plena. Em crianças, as dosagens propostas para as vias intranasal, intraóssea e intramuscular variam muito e não há um consenso na literatura sobre dosagens específicas. Alguns dos artigos referenciados propõem regimes de dosagens pediátricas.29 a = A cetamina deve ser titulada até alcançar o efeito clínico necessário. b = Dose analgésica e sedativa. c = Dose anestésica. Há uma certa sobreposição entre as doses de sedação e de anestesia.
Os principais efeitos colaterais que limitam o uso da cetamina em procedimentos curtos são agitação e sintomas indesejáveis ao despertar. Ambos são mais comuns com doses altas. Os benzodiazepínicos reduzem eficazmente a incidência dos sintomas ao despertar. Há relatos do uso de midazolam (0,07-0,1 mg kg-1), diazepam (0,15-0,3 mg kg-1) e lorazepam (2-4 mg).8 A recuperação do paciente em um ambiente silencioso, com sensação de plena segurança, pode reduzir a incidência e gravidade dos sintomas ao despertar após sedação com cetamina.
Estudo de caso 1: Cuidados pré-hospitalares
Uma menina de 6 anos, com saudável, foi vista caindo de um muro de 1,80 m sobre uma superfície de concreto. Queixa-se de dor aguda no tornozelo direito. Está a 45 minutos do hospital mais próximo e foi atendida por uma ambulância. Não perdeu a consciência e não há evidência de traumatismo craniano. Achados primários:
A: sem hemorragia grave.
B: via aérea patente, ventilando sozinha, saturação de oxigênio 99% em ar ambiente.
C: hemodinamicamente estável, todos os pulsos periféricos presentes, porém com tempo de perfusão capilar aumentado no pé direito (5 segundos vs. 2 segundos nas outras periferias).
D: Escala de Glasgow 15, pupilas isocóricas e fotorreagentes, glicemia normal.
E: Fratura com deslocamento no tornozelo direito, nenhuma outra lesão perceptível.
Devido à perfusão reduzida no pé e à distância até o hospital, o médico decide reduzir a fratura no local. Considere as opções disponíveis de sedação e analgesia para permitir a manipulação.
Neste caso, foi usada uma combinação de fentanil e cetamina para induzir um estado dissociativo. Após iniciar a monitorização plena (eletrocardiograma, oximetria de pulso, pressão arterial não-invasiva e CO2 expirado) foram administradas doses iniciais de 0,5 mcg·kg-1 de fentanil e 0,2 mg·kg-1 de cetamina. Tração delicada foi aplicada, mas não foi tolerada devido à dor. Assim, foram administrados mais 0,25 mcg·kg-1 de fentanil e 0,2 mg·kg-1 de cetamina. O efeito foi bom, permitindo a redução com sucesso e a colocação de curativo e de uma tala. O transporte seguiu sem intercorrências.
Indução e manutenção de anestesia
A cetamina é também cada vez mais usada em ambientes hospitalares e pré-hospitalares como agente anestésico e de manutenção em emergências. Em indução de sequência rápida, uma dose de 1 a 2 mg·kg-1 i.v. produz anestesia dissociativa dentro de 1 a 2 minutos. Isso é geralmente mais lento que o tempo circulatório de ‘braço-a-cérebro’ para inconsciência observada com os usuais agentes de indução i.v. (p.ex. propofol e tiopental). Porém, em circunstâncias onde o controle hemodinâmico é importante (p.ex. trauma e sepse), a cetamina tem suas vantagens. Ela oferece outros benefícios importantes, como p.ex. permitir uma melhor pré-oxigenação em pacientes agitados, podendo-se administrar doses reduzidas (0,25-0,5 mg·kg-1 i.v.) antes da indução da anestesia plena.12 Uma dose reduzida de cetamina para indução deve ser considerada em pacientes com choque devido à possibilidade de efeitos simpaticomiméticos inadequados nessa população.
Descrições do uso de cetamina para anestesia intravenosa total (TIVA) em combinação com relaxantes musculares não são frequentes na literatura, mas já foi relatado o uso de cetamina como agente único e combinada com outros hipnóticos (p.ex. propofol e benzodiazepinas). As indicações potenciais para TIVA com cetamina incluem choque cardiogênico, hipovolemia e tamponamento pericárdico, especialmente em regiões com acesso limitado a drogas vasoativas. TIVA com cetamina também já foi usada em crianças, com bom resultado.8
A anestesia pode ser mantida com bolus intermitentes de cetamina i.v. (0.5 mg kg—1) ou por infusão contínua a 10-30 mcg kg-1 min-1, titulado de acordo com o efeito. A interrupção da infusão 20 a 30 minutos antes do fim da cirurgia permite uma eliminação adequada. Deve ser lembrado que a eletroencefalografia e o índice bispectral não devem ser utilizados para monitorar a profundidade anestésica em anestesia induzida com cetamina.
Analgesia
A cetamina é um analgésico potente. Age como antagonista dos receptores NMDA, produzindo analgesia dissociativa. Porém, a baixas doses, a cetamina dessensibiliza as vias de dor central e modula os receptores de opióides.13 Há estudos mostrando que a administração perioperatória de pequenas doses de cetamina pode reduzir em até 50% a necessidade de opióides.14
Exemplos de regimes de analgesia perioperatória incluem infusões intra-operatórias de cetamina, infusões pós-operatórias, bolus de doses baixas, e analgesia controlada pelo paciente. Todos foram descritos em detalhes em revisão Cochrane de 2006.14 Esta última fornece evidências da eficácia analgésica da administração perioperatória de cetamina, sem concluir sobre dosagens ideais ou métodos de administração. Em um ensaio randomizado controlado de pacientes monitorados em UTIs após grandes cirurgias abdominais, cetamina foi administrada na forma de um bolus i.v. inicial de 0,5 mg kg-1 seguido por uma infusão de 2 mcg kg-1 min-1 nas primeiras 24 horas, e 1 mcg kg-1 min-1 nas próximas 24 horas.15, com redução significativa do uso pós-operatório de morfina.
Em serviços de emergência e ambientes pré-hospitalares também se utiliza regimes de baixas doses de cetamina para manejo de dor. Tipicamente, as doses recomendadas são entre 0,1 e 0,2 mg kg-1 i.v. Em um estudo, um bolus de 0,1 mg kg-1 cetamina i.v. foi combinado com opióides em pacientes com diversas queixas (p.ex. dor abdominal, lacerações e fraturas).16 Isso produziu analgesia eficaz por mais de 120 minutos e reduziu a necessidade de opióides. Houve alguns efeitos colaterais no grupo de cetamina, mas a maioria era insignificante e tolerável.
Há evidências de que, através da dessensibilização das vias centrais de dor, a cetamina pode ser útil em pacientes cirúrgicos com uso crônico de opióides. Vários estudos em populações com esse perfil mostram uma redução no uso de opióides nas primeiras 48 horas e melhores escores de dor 6 semanas após a administração intraoperatória de cetamina i.v.17 Recentemente, foi também proposta a administração intraoperatória de cetamina para a prevenção de dor pós-cirúrgica crônica. Uma metanálise recente examinou estudos comparando cetamina intraoperatória de baixa dose com placebo, com acompanhamento de 3, 6 e 12 meses.18 Os resultados mostram que a dor pós cirúrgica foi reduzida aos 3 e 6 meses, embora não houvesse diferença significativa entre os grupos aos 12 meses. Os primeiros estudos são promissores, mas serão necessárias novos trabalhos para avaliar o papel potencial da cetamina na dor pós cirúrgica persistente.
Doença reativa das vias aéreas
A cetamina tem efeitos broncodilatadores e é eficaz em pacientes com broncoespasmo agudo. Acredita-se que o efeito da cetamina sobre as vias aéreas seja através da modulação da cascata inflamatória. Uma revisão recente mostrou que a cetamina pode ter utilidade em casos de asma refratária ao tratamento convencional.19 Os autores perceberam que os pacientes tratados com cetamina apresentaram melhora clínica, demandaram menos oxigênio e, em alguns casos, evitaram o uso de ventilação mecânica. Pacientes mecanicamente ventilados que receberam cetamina para broncoespasmo grave mostraram uma melhor troca gasosa, menor pressão inspiratória e maior ventilação minuto, e com frequência o desmame foi bem sucedido. Nenhum efeito adverso importante foi relatado nesta revisão de cetamina com 244 pacientes. A revisão incluiu um mix de relatos de caso, séries de casos, estudos observacionais e ensaios randomizados controlados. Doses de carga altamente variáveis (de 0,1 a 2,0 mg kg-1) foram usadas nos estudos e, dependendo da resposta inicial, a dosagem usada para infusão contínua foi de 0,15 a 2,5 mg kg-1 hr-1. Considerando o tamanho pequeno da amostra e a grande variação na dosagem de carga e infusão, mais pesquisas são necessárias nessa área.
Usos clínicos
A cetamina possui várias aplicações potenciais em cuidados críticos, tais como sedação, analgesia e o tratamento de broncoespasmo persistente. A combinação de cetamina e propofol (“cetofol”) é eficaz em sedação de curta duração em cuidados críticos.20 Deve-se lembrar que, em pacientes críticos, o efeito inotrópico negativo direto da cetamina pode se sobrepor à resposta cardiovascular usualmente favorável. Há relatos de reduções inesperadas de pressão arterial e débito cardíaco após a administração de cetamina em alguns pacientes críticos. Porém, um grande estudo multicêntrico de pacientes críticos sépticos não encontrou nenhum efeito adverso da cetamina.21 Outros sugeriram que a cetamina pode ter vantagens potenciais sobre outros agentes em pacientes com sepse grave (veja o segundo estudo de caso, abaixo). Há evidências de que a cetamina pode exercer um efeito anti-inflamatório protetor, reduzindo os efeitos sistêmicos da sepse (p.ex. hipotensão e acidose metabólica).22
No passado, a cetamina era contraindicada em pacientes com lesão cerebral traumática ou pressão intracraniana aumentada, mas estudos posteriores vêm mostrando que a cetamina pode ser útil como sedativo nessas populações. O seu uso já foi associado com a manutenção da pressão de perfusão cerebral durante intervenções estimulantes em uma população de pacientes críticos com lesão cerebral.23 O seu uso em casos de lesão cefálica traumática ainda é objeto de discussão, mas as atuais evidências (Oxford nível 2b, grau C) sugerem que a cetamina não aumenta a pressão intracraniana em pacientes sedados e ventilados com lesão cerebral traumática grave; na verdade, pode até reduzi-la.24 Mais pesquisas são necessárias nessa área antes que o seu uso possa ser amplamente recomendado.
Estudo de caso 2: Sepse
Um homem de 67 anos compareceu à emergência com uma queixa de 2 dias de tosse produtiva, confusão e febre. Estava hemodinamicamente instável, com hipotensão e taquicardia. Recebeu diagnóstico de septicemia secundária a uma suposta pneumonia grave. O tratamento inicial consistiu de soro i.v. e antibióticos apropriados. Apesar disso, piorou o quadro de hipóxia, hipotensão e acidose metabólica. O paciente foi transferido para cuidados críticos, iniciando ventilação mecânica e suporte cardiovascular.
Considere os agentes de indução disponíveis e os riscos e benefícios de cada.
Neste caso, a cetamina foi escolhida como agente anestésico (1,5 mg•kg-1), isso devido à sua estabilidade cardiovascular quando comparada com agentes de indução alternativos. Há também evidências de que a cetamina tem propriedades anti-inflamatórias.
Precauções e limitações
A cetamina tem um ótimo perfil de segurança. Overdose de cetamina é descrita como sedação prolongada em estudos de caso com crianças que inadvertidamente receberam de 5 a 100 vezes a dose recomendada.6 Existem alguns poucos estudos de caso com depressão respiratória grave após administração de rotina de cetamina combinada com outras medicações, mas geralmente só ocorreram episódios apnéicos transitórios após grandes doses em bolus i.v.
Conforme a British National Formulary,25 as contraindicações absolutas de cetamina i.v. são hipertensão arterial, pré-eclâmpsia ou eclâmpsia, doença cardíaca grave, AVC, pressão intracraniana aumentada, e porfiria aguda. A cetamina também não é recomendada em crianças de até 3 meses e em esquizofrênicos.
Países em desenvolvimento
A cetamina é hoje muito usado no mundo devido à sua versatilidade, disponibilidade e perfil de poucos efeitos colaterais. Há um debate sobre seu potencial para abuso e a necessidade de um maior controle. Em 2015, a OMS concluiu que, devido à importância da cetamina em alguns países, o controle internacional limitaria o acesso a cirurgias essenciais e de emergência, levando a uma crise na saúde pública de países onde não há alternativas de custo acessível.
A cetamina é um dos anestésicos mais disponíveis em países de baixa e média renda (PBMR).26 Um relatório recente constatou que em 12 PBMRs, somente 53% dos hospitais possuiam um equipmento funcional de anestesia e somente 52% tinham acesso permanente a oximetria de pulso. Em média, de 21 a 45% não possuiam equipamento básico de manejo das vias aéreas. No relatório em questão, anestesia geral inalatória estava disponível em somente 58% das instituições. Contudo, de 70 a 90% relataram ter acesso permanente a cetamina.
Um estudo visando quantificar o uso de cetamina em PBMRs encontrou uma taxa de complicações graves (p.ex. morte, parada cardíaca, apnéia, laringoespasmo e broncoaspiração) de somente 0,15% em um total de mais de 12.000 aplicações de cetamina durante cirurgias de rotina e emergência.27 As complicações estavam muitas vezes relacionadas à experiência dos profissionais e monitorização disponível, indicando que a margem de segurança do uso de cetamina é elevada nessas situações.
O tutorial nº 27 (de Craven e Alkhafaji) traz mais exemplos dos diversos usos da cetamina, inclusive em PBMRs.28
Resumo
A cetamina é uma droga versátil com um perfil extraordinário que permite o seu uso bem sucedido em uma grande variedade de situações. Por ter uma dosagem variável, pode ser usada como agente de indução, com bom perfil hemodinâmico, ou em doses baixas como sedativo ou analgésico confiável. Tem uma aplicação útil em cuidados pré-hospitalares e procedimentos de emergência. Como adjunto durante a anestesia de rotina, ajuda a reduzir a necessidade pós-operatória de opióides. Seu uso em cuidados críticos inclui sedação e manejo de asma refratária. Contudo, há necessidade de mais estudos para esclarecer o seu papel em pacientes com traumatismo craniano. Nos países em desenvolvimento, é uma droga vital e muito valorizada que permite fazer intervenções e cirurgias, especialmente onde os recursos são escassos.
A cetamina ainda é estigmatizada por médicos e outras pessoas e é frequentemente preterida por causa de preocupações com efeitos colaterais psicológicos. Uma maior disponibilidade de preparações de cetamina de isômero S (+) poderá aumentar a sua popularidade.
Referências
- Kurdi MS, Theerth KA, Deva RS. Ketamine: current applications in anesthesia, pain and critical care. Anesth Essays Res. 2014;8(3):283-290.
- Ori C, Freo U, Merico A, et al. Effects of ketamine-enantiomers anesthesia on local glucose utilization in the rat. Anesthesiology. 1999;91(3A)A772.
- Kawasaki T, Ogata M, Kawasaki C, et al. Ketamine suppresses pro-inflammatory cytokine production in human whole blood in vitro. Anesth Analg. 1999;89(3):665-669.
- Marland S, Ellerton J. Ketamine: use in anesthesia. Review. CNS Neurosci Ther. 2013;19(6):381-389.
- Luft AN, Mendes FF. Low S(þ) ketamine doses: a review. Rev. Bras. Anestesiol. 2005;55 (4):460-469.
- Best W, Bodenschatz C, Beran D. World Health Organisation Critical Review of Ketamine. 36th WHO Expert Committee on Drug Dependence report, 6.2. Geneva, Switzerland: World Health Organisation. 2014.
- Dolansky G, Shah A, Mosdossy G, Rieder M. What is the evidence for the safety and efficacy of using ketamine in children? Paediatr Child Health. 2008;13(4):307-308.
- Pai A, Heining M. Ketamine. Cont Educ Anesth Crit Care Pain: CEACCP 2007;7(2):59-63.
- Heinz P, Geelhoed GC, Wee C, Pascoe EM. Is atropine needed with ketamine sedation? A prospective, randomised, double blind study. Emerg Med J: EMJ. 2006;23(3):206-209.
- Green SM, Roback MG, Kennedy RM et al. Clinical practice guideline for emergency department ketamine dissociative sedation: 2011 update. Ann Emerg Med. 2011;57(5):449-461.
- Andolfatto G, Abu-Laban RB, Zed PJ, et al. Ketamine propofol combination (ketofol) versus propofol alone for emergency department procedural sedation and analgesia: a randomized double-blind trial. Ann Emerg Med. 2012;59(6):504-512.
- Mosier JM, Joshi R, Hypes C, Pacheco G, Valenzuela T, Sakles JC. The physiologically difficult airway. West J Emerg Med. 2015;16(7):1109-1117.
- Sleigh J, Harvey M, Voss L, Denny B. Ketamine—more mechanisms of action than just NMDA blockade. Trends Anaesth Crit Care. 2014;4(2):76-81.
- Bell RF, Dahl JB, Moore RA, Kalso EA. Perioperative ketamine for acute postoperative pain. Cochrane Database Syst Rev. 2006;Jan 25(1):CD004603.
- Guillou N, Tanguy M, Seguin P, et al. The effects of small-dose ketamine on morphine consumption in surgical intensive care unit patients after major abdominal surgery. Anesth Analg. 2003;97(3):843-847.
- Bowers KJ, McAllister KB, Ray M, Heitz C. Ketamine as an adjunct to opioids for acute pain in the emergency department: a randomized controlled trial. Acad Emerg Med. 2017;24(6):676-685.
- Gorlin AW, Rosenfeld DM, Ramakrishna H. Intravenous sub-anesthetic ketamine for perioperative analgesia. J Anaesthesiol Clin Pharmacol. 2016;32(2):160-167.
- McNicol ED, Schumann R, Haroutounian S. A systematic review and meta-analysis of ketamine for the prevention of persistent post-surgical pain. Acta Anaesthesiol Scand. 2014;58(10):1199-213.
- Goyal S, Agrawal A. Ketamine in status asthmaticus: a review. Ind J Critl Care Med. 2013;17(3):154-161.
- Hamimy W, Abdelaal A. The application of a new regimen for short term sedation in ICU (ketofol)—case series. Egypt J Anaesth. 2012;28(3):179-182.
- Jabre P, Combes X, Lapostolle F, et al. Etomidate versus ketamine for rapid sequence intubation in acutely ill patients: a multicentre randomised controlled trial. Lancet. 2009;374(9686):293-300.
- Yoon SH. Concerns of the anesthesiologist: anesthetic induction in severe sepsis or septic shock patients. Korean J Anesthesiol. 2012;63(1):3-10.
- Bar JG, Guilburd Y, Guilburd J. Ketamine effectively prevents intracranial pressure elevation during endotracheal suctioning and other distressing interventions in patients with severe traumatic brain injury. Crit Care Med. 2009;37(12):A402.
- Zeiler FA, Teitelbaum J, West M, et al. The ketamine effect on ICP in traumatic brain injury. Neurocrit Care. 2014;21(1):163-173.
- Joint Formulary Committee. British National Formulary. http://www.medicinescomplete.com. Accessed October 26, 2017.
- Dong TT, Mellin-Olsen J, Gelb AW. Ketamine: a growing global health-care need. Br J Anaesth. 2015;115(4):491-493.
- Green SM, Clem, KJ, Rothrock SG. Ketamine safety profile in the developing world. Acad Emerg Med. 1996;3(6):598- 604.
- Craven R, Alkhafaji R. Ketamine in Anaesthetic Practice, ATOTW 27. World Anaesthesia Tutorial of the week. 2006.
- Poonai N, Canton K, Ali S, et al. Intranasal ketamine for procedural sedation and analgesia in children: A systematic review. Ma Z-L, ed. PLoS ONE. 2017;12(3)



