Intensive Care Medicine
PONTOS-CHAVE
- A anestesia em emergência pré-hospitalar (AEPH) é uma intervenção de alto risco que pode ter um impacto positivo significativo no desfecho do paciente.
- A seleção cuidadosa do paciente é de suma importância. Indicações adequadas incluem pacientes com comprometimento de via aérea, comprometimento da ventilação, aqueles que requerem neuroproteção específica, e pacientes cujo desfecho clínico previsto sugere a necessidade de indução emergencial de anestesia antes do transporte ao hospital ou logo após a sua chegada ao hospital.
- As condições climáticas, a disponibilidade de equipamento, posição do paciente, dinâmica do local e as competências da equipe podem todas contribuir para aumentar as dificuldades na indução anestésica no ambiente pré-hospitalar.
- A escolha das drogas para indução e manutenção deve ser adaptada de acordo com o estado hemodinâmico e a condição associada de cada paciente.
- O uso de imobilização da coluna cervical, pressão da cricóide, e cetamina como um agente de indução representam areas de controvérsia. Contudo, uma base de evidências em evolução informa a prática nessas áreas.
INTRODUÇÃO
A anestesia em emergência pré-hospitalar (AEPH) se refere à indução de anestesia e estabelecimento da via aérea no ambiente pré-hospitalar. É uma forma modificada da indução de sequência rápida (ISR) e intubação. A AEPH é inerentemente de alto risco por causa tanto de fatores relacionados ao paciente quanto ao ambiente pré-hospitalar. Muitos fatores precisam ser considerados e abordados a fim de minimizar os riscos. A anestesia pré-hospitalar foi descrita como uma “intervenção desejável em relativamente poucos pacientes que podem resultar em morbidade e mortalidade desnecessárias se for mal executada.”1 O relatório “Trauma: Quem se Preocupa?”, do Inquérito Confidencial Nacional sobre Resultados e Óbitos de Pacientes (NCEPOD, em inglês), de 2007, investigou áreas que potencialmente contribuem com óbitos preveníveis em traumas significativos. Esse relatório identificou que uma via aérea inadequada foi estabelecida em 42 de 438 casos, e que 72,9% dos pacientes com lesão grave na cabeça e um escore menor que 9 na Escala de Coma de Glasgow (ECG) não foram submetidos a AEPH.2
POR QUÊ? PARA QUEM?
Os riscos associados à realização de AEPH precisam ser ponderados em relação aos benefícios propostos para cada paciente. Há variações regionais e internacionais na prática acerca da realização de intervenções pré-hospitalares. Os 2 extremos desta variação têm sido chamados de “stay and play” (“fique e jogue”) X transferência rápida “scoop and run” (“remova e corra”). Há poucas evidências de que um sistema tenha vantagens sobre o outro.22 Múltiplos fatores devem ser considerados para cada caso em que a AEPH for considerada. Isso inclui considerações geográficas, modo de transporte e competência clínica do time de resposta, e distribuições das lesões/doenças. Esses fatores são determinantes importantes na seleção de pacientes nos quais os benefícios da AEPH superam seus riscos.
Fatores Relacionados ao Paciente a Serem Considerados na Seleção dos Pacientes
- A necessidade de proteção da via aérea em pacientes com comprometimento real ou iminente da via aérea.
- A necessidade de suporte respiratório. A insuficiência ventilatória às vezes pode ser melhorada de maneira mais efetiva pela intubação e instituição de ventilação mecânica.
- A necessidade de neuroproteção para evitar lesão cerebral secundária.
- O percurso clínico previsto (p.ex.: um paciente com ECG reduzido que está combativo e que se prevê que vá exigir anestesia quando der entrada no hospital para facilitar exames de imagem e tratamento) O NCEPOD relatou no documento “Trauma: Quem se Preocupa?” que 31,7% de pacientes com lesões graves com um Escore de Gravidade de Lesão >16 exigiram intubação até 30 minutos após a chegada. Concluiu-se que isso levou a resultados clínicos piores.1 Portanto, em casos em que o curso clínico previsto seja a deterioração ao ponto em que a anestesia provavelmente será exigida imediatamente na chegada à atenção secundária, então a AEPH deve ser normalmente realizada no local.
- Por razões humanitárias (p.ex.: na presença de várias lesões graves como fraturas que exijam talas, ou queimaduras significativas).
- O modo de transporte, a equipe para o transporte e o tempo necessário para a transferência do paciente à atenção definitiva também devem ser considerados ao se ponderar sobre os benefícios da AEPH. Em ambientes com tempos de transferência curtos (como os ambientes urbanos britânicos), o benefício de uma rápida transferência a um ambiente hospitalar pode superar o benefício de intervenções pré-hospitalares.3 A posição do paciente e dos diferentes membros da equipe dentro do veículo de transporte também deve ser prevista, já que o acesso ao paciente durante a transferência geralmente é limitado. Por exemplo, uma lesão no tórax que pode exigir uma toracostomia no trajeto precisa ser cuidadosamente considerada se o lado lesionado estiver imediatamente ao lado da parede da ambulância ou aeronave, e, portanto, não imediatamente acessível.
RISCOS AUMENTADOS E SUA MITIGAÇÃO
Os riscos de se realizar a AEPH podem ser divididos em fatores ambientais, fatores do operador/humanos, e fatores do paciente. Esses fatores geralmente estão interligados.
Fatores Ambientais
Uma variedade de fatores ambientais influencia os riscos de AEPH.
1. Condições ambientais. Comparada ao trabalho no ambiente hospitalar geralmente controlado, aquecido e iluminado, uma tentativa de AEPH tem estressores adicionais. Ruídos que distraem, excesso ou falta de luz, vento, chuva, membros do público, veículos em movimento, solo íngreme, vazamentos de combustível, etc., todos aumentam a carga cognitiva do operador. Isso pode resultar em uma habilidade técnica reduzida para completar a tarefa, e em uma perda de atenção situacional, incluindo uma menor habilidade para reconhecer quando ocorreram erros.
As condições ambientais também terão impacto na temperatura do paciente, pois eles podem ficar expostos ao clima e ficar imóveis devido à lesão ou doença e, eventualmente, fisicamente presos. Qualquer redução na temperatura central será exacerbada após a anestesia. Uma temperatura central reduzida contribuirá para a coagulopatia e resultados ruins do trauma.4 Medidas para manter ativamente a temperatura corporal reduzindo a perda de calor, buscando o aquecimento ativo, e reduzindo o tempo de permanência no local são urgentes nessa população. Uma escola de local às vezes pode mitigar alguns desses problemas.
A alterações na luz natural também podem levar a problemas. O brilho da luz solar contrairá a pupila do intubador, reduzindo assim a visualização das cordas vocais na orofaringe relativamente escura. O posicionamento do paciente com a cabeça virada para a direção contrária à luz do sol e adaptações criativas no ambiente podem criar sombra.
2. Acesso ao paciente. Pacientes que requerem intubação no ambiente pré-hospitalar raramente são encontrados em locais convenientes. Os exemplos incluem porões, quartos pequenos, dentro de veículos, margens íngremes, encostas rochosas e becos estreitos. Vários riscos são inerentes à tentativa de anestesia em locais com acesso restrito ao paciente. Onde for possível, o paciente deve ser movido para um local onde se possa ter um “acesso de 360°” antes de se tentar a AEPH. Para otimizar a tentativa de intubação tanto quanto possível e assim reduzir o risco de fracasso na intubação, o paciente é melhor posicionado em uma altura na qual o intubador possa se ajoelhar ou ficar de pé. Isso pode ser em uma maca hospitalar, que pode ser adaptada à altura apropriada.
3. Acessibilidade do kit. Em um ambiente hospitalar organizado, o equipamento e as medicações estão prontamente disponíveis e rapidamente acessíveis. No ambiente pré-hospitalar, todo o equipamento necessário deve ser carregado até o local. A padronização de kits em mochila/sacos e o treinamento frequente para familiarizar os membros da equipe com o conteúdo e arranjo dos kits em mochila/sacos (“kit dump”) são essenciais; isso vai permitir que qualquer membro da equipe pré- hospitalar os prepare. O “kit dump” deve incluir dispositivos de via aérea e adjuvantes, guia introdutor do tipo “bougie” para intubação, aspiração, oxigênio, sistema de respiração/ventilação, monitorização e drogas (preparadas ou colocadas em seringas rotuladas; v. Tabela 2). A capnografia quantitativa com forma de onda é recomendada no Reino Unidos e deve ser considerada como um requisito obrigatório antes de se iniciar a AEPH.
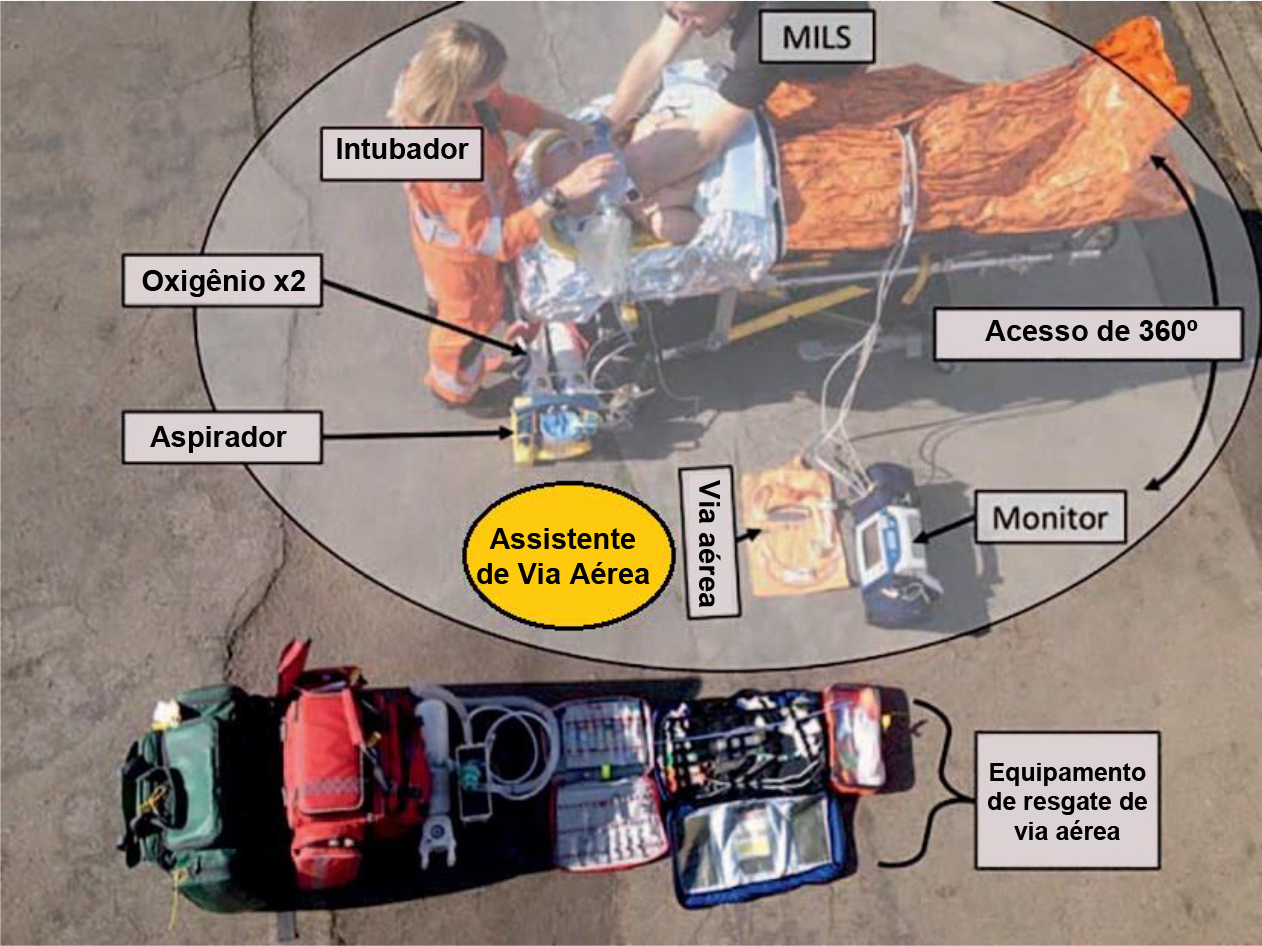
Figura. Esquema do kit com destaque mostrando a localização do equipamento e da equipe. A posição do assistente de via aérea está marcada em laranja. A estabilização manual em linha (“MILS”) deve ser considerada quando houver risco de lesão à coluna cervical para prevenir movimento excessivo durante a intubação.
Em um estudo de Li et al., 5 até 3% das intubações de emergência resultaram em intubação esofágica. Em um estudo baseado nos EUA, o uso do traçado de CO2 pelo do capnógrafo reduziu a taxa de má colocação não reconhecida de tubos traqueais de 9% para 0%.6 Outros fatores que podem ajudar na detecção de intubação esofágica é o uso de videolaringoscopia (pois isso permite que o tubo seja observado passando pelas cordas), auscultação do tórax com um estetoscópio, e familiaridade com “como deve ser” quando se está ventilando manualmente um paciente por meio de um tubo endotraqueal corretamente colocado (Figura).7
Fatores do Operador/Humanos
- Conforto e segurança. Como discutido acima, o conforto e segurança do intubador e do restante da equipe são importantes para a redução do risco. Equipamento de proteção individual, incluindo vestimentas apropriadas para o clima e a temperatura, é importante, bem como uma localização e posicionamento apropriados do paciente.
- Conjunto de habilidades da equipe. A anestesia pré-hospitalar é uma intervenção de alto risco que não deve ser tentada por quem não tem treinamento ou experiência suficientes. É essencial que haja um rigoroso programa de treinamento, que as habilidades sejam mantidas, e que haja uma revisão regular da prática.1 Todos os envolvidos na AEPH devem trabalhar de acordo com um conjunto de procedimentos operacionais padrão (POPs) e devem estar bem treinados, de forma que toda a equipe saiba tanto o seu papel quando a maneira padronizada como os procedimentos são feitos na sua organização.
- Sobrecarga cognitiva. O ambiente pré-hospitalar geralmente tem muitos socorristas no local, incluindo profissionais de saúde, outros profissionais de emergência, e o público. Frequentemente, há atividades concomitantes, e, às vezes, há mais de um incidente. A redução de erros é conseguida por meio do uso de uma lista de verificação verbal de pré-indução do tipo “desafio-resposta”. Os POPs e as listas de verificação simplificam os processos e limita a escolha para reduzir ainda mais a carga cognitiva.8 A carga cognitiva é reduzida ao se confirmar a disponibilidade de equipamentos, drogas (incluindo cálculos de doses), e planos de ação de emergência para falha de intubação e outros problemas potenciais.1 Usar listas de verificação também garante que quem estiver executando a AEPH permaneça apropriadamente focado na tarefa. Um exemplo de uma lista de verificação é fornecido na Tabela 1.
Fatores do Paciente
Pacientes que requeiram AEPH não terão sido submetidos a uma avaliação pré-operatória padrão. Em contraste com pacientes de cirurgia eletiva, eles não terão sido otimizados para anestesia, e informações prévias sobre avaliação das vias aéreas estarão indisponíveis. Eles são um grupo de alto risco, frequentemente com desarranjo fisiológico significativo, como hipovolemia, hipóxia, hipotermia e acidose metabólica. Mitigar esses fatores pode ser extremamente difícil, e nem sempre é possível.
1. Hipovolemia. A indução de anestesia em pacientes hipovolêmicos é perigosa; A AEPH em pacientes com trauma, hipovolêmicos e sub ressuscitados está associada a um aumento na mortalidade. Esses pacientes devem idealmente serem submetidos a ressuscitação com produtos sanguíneos balanceados antes da indução da anestesia. A ressuscitação com controle de danos enfatiza a importância de uma ressuscitação apropriada com produtos sanguíneos balanceados para diminuir os efeitos prejudiciais de sangramento importante, incluindo acidemia e coagulopatia, neste grupo de pacientes.9
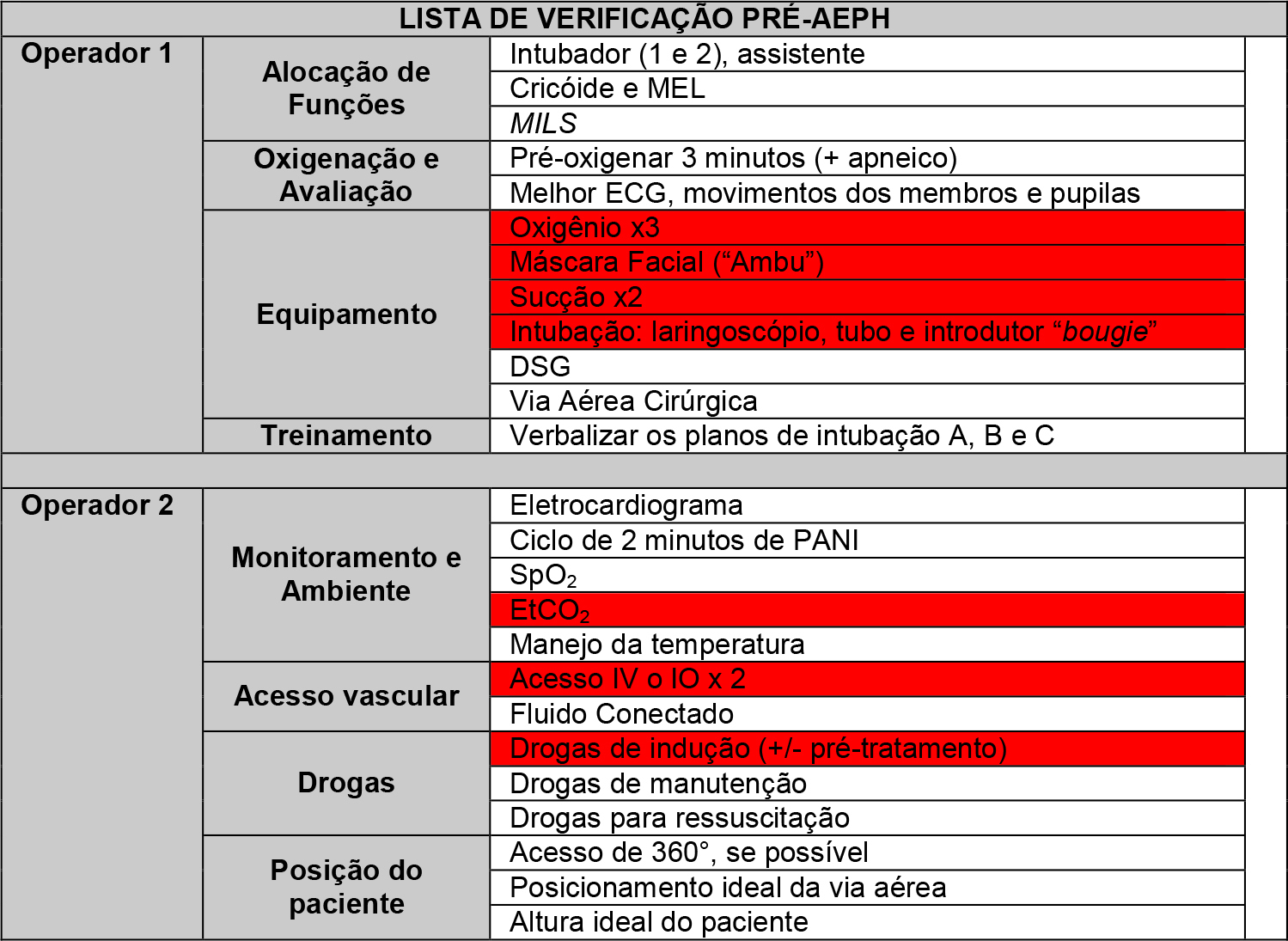
Tabela 1. Exemplo de Lista de Verificação de AEPH com Elementos Centrais para “Indução Imediata” Destacados em Vermelho. MEL, Manipulação Externa da Laringe; MILS, estabilização manual em linha; DSG, dispositivo supraglótico de via aérea. Retirado do Serviço de Ambulância do Sudoeste, NHS Foundation Trust, Diretriz Crítica ID CCG02, “Anestesia em Emergência Pré Hospitalar (AEPH)”, emitido em 1o de setembro de 2015
Antes de se atingir o controle definitivo da hemorragia, os valores fisiológicos adequados a serem buscados incluem uma pressão arterial média de 50 mmHg, pressão arterial sistólica de mais de 80 mmHg, ou retorno de um pulso periférico palpável.10 A acidose, monitorada “poit-of-care” pelo “base excess”, pode ser corrigida por uma boa ressuscitação.
Drogas anestésicas podem piorar ainda mais o perfil hemodinâmico do paciente por meio de uma vasodilatação induzida por medicamento, depressão do miocárdio, e perda de tônus simpático compensatório. Além disso, a ventilação com pressão positiva neste cenário vai reduzir ainda mais a pré-carga.
Um acesso intravenoso adequado é vital. Recomenda-se idealmente ter dois locais de acesso venoso confiável, de largo calibre, e algum tipo de fluido instalado para todas as induções anestésicas. Isso permitirá tanto uma rápida administração de um bolus de 250ml de fluido, se requerido, quanto uma fácil infusão de drogas que tenham disso administrada. A necessidade de doses adaptadas de agente de indução deve ser considerada. Como discutido mais adiante, os vasopressores devem ser evitados na hipovolemia, se possível.
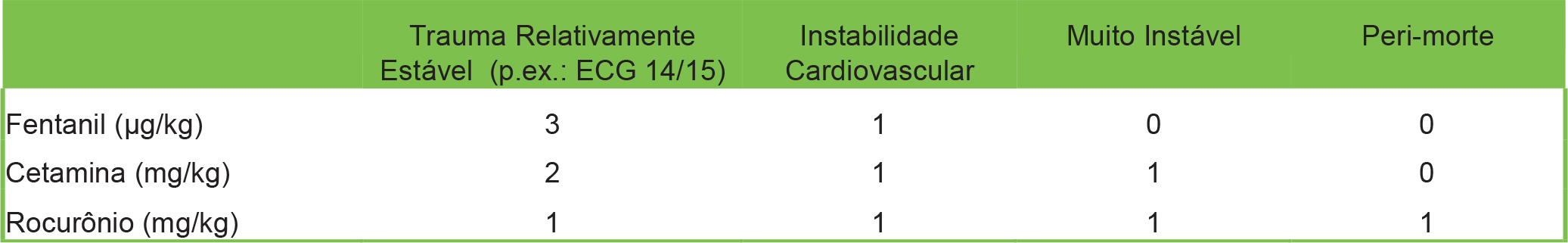
Tabela 2. Doses de Agentes Anestésicos Ajustadas para a Condição do Paciente (Adaptado de Ref. 14)
2. Hipóxia. Deve-se fazer um esforço para maximizar a efetividade da pré-oxigenação. Uma pré-oxigenação efetiva no ambiente pré-hospitalar pode ser difícil, mas é melhor atingida por uma combinação de alto fluxo de oxigênio nasal e um circuito de Water. Este último pode ser continuado na fase apneica, e isso pode aumentar o tempo apneico seguro em até 10 minutos.11 Para aqueles em quem a pré-oxigenação é difícil por causa de agitação, uma sedação criteriosa pode ser usada para permitir uma pré-oxigenação efetiva antes de se tentar a AEPH. A cetamina 0,5 a 1 mg/kg por via intravenosa (ou 4-5 mg/kg por via intramuscular) é o agente mais comumente usado para este fim. Enquanto o midazolam também pode ser efetivo, ele é usado menos comumente neste cenário por causa de preocupações sobre a perda de permeabilidade das vias aéreas.
Embora, de maneira clássica, uma ISR não inclua ventilação manual, no paciente crítico, a ventilação assistida é comumente usada durante e após a indução da anestesia. O risco de inflação gástrica e consequente aspiração pode ser mitigado mantendo- se uma pressão inspiratória de menos de 25 cmH2O.12
3. Hipotermia. Os pacientes devem ser mantidos aquecidos com proteção adequada contra o clima. Em muitos casos, o aquecimento ativo para garantir a manutenção da temperatura também será necessário.
4. Via aérea. Deve-se supor que todas as vias aéreas pré-hospitalares serão difíceis. Muitas equipes de atenção crítica do Reino Unido usam um videolaringoscópio e um guia introdutor do tipo “bougie” em todas as intubações. Isso não apenas reduz a carga cognitiva para a equipe ao se ter uma abordagem padrão, mas também remove uma camada de processo se a via aérea for difícil, permitindo assim uma rápida progressão através de um algoritmo de via difícil.
Para pacientes com trauma e suspeita de lesão da coluna cervical, o equipamento usado para imobilização, como colares cervicais e apoios laterais, diminuirão significativamente o melhor grau alcançável da laringoscopia, e deve ser trocado por estabilização manual em linha antes da indução da anestesia.2
DROGAS PARA INDUÇÃO
O objetivo sempre deve ser entregar uma anestesia segura e balanceada, adaptada ao paciente e a conjunto de habilidades do operador. Muitas fórmulas diferentes foram sugeridas, como oferecer a combinação e doses ideais de drogas.13–15 Algumas são discutidas abaixo. É amplamente aceito que o bloqueio neuromuscular deve ser usado. Um estudo de intubações por paramédicos mostrou uma taxa geral de sucesso de 67,5%, que aumentou para 81% quando se usou um sedativo, e para 96,7% quando se usou um bloqueador neuromuscular.1 Também foi demonstrado que um bloqueio neuromuscular adequado aumenta significativamente a probabilidade de sucesso de procedimentos na parte frontal do pescoço, em situações em que é “impossível intubar, impossível ventilar”.1 Isso é particularmente importante, pois seria muito improvável que um paciente esteja apto a ser acordado neste cenário se a AEPH fosse indicada.
Fórmula “3, 2, 1”
A fórmula 3,2,1, referindo-se às doses de fentanil, cetamina e rocurônio, respectivamente, foi sugerida como a base da anestesia pré-hospitalar em trauma.1212 Isso deve ser adaptado para se adequar a diferentes situações. Um regime de 1:1:1 foi sugerido para pacientes com instabilidade cardiovascular. A remoção do fentanil para pacientes muito instáveis também foi sugerida, assim como a administração de apenas rocurônio no paciente em coma na iminência de parada cardíaca (Tabela 2).
Uma fórmula de fentanil, cetamina e rocurônio mostrou produzir condições de intubação superiores com melhor estabilidade hemodinâmica quando comparada ao etomidato e suxametônio. Além disso, há evidencias que sugerem que pode ocorrer supressão adrenal mesmo após uma única dose de etomidato.16 Em um teste de etomidato X cetamina, 232 pacientes que foram randomizados tiveram insuficiência adrenal avaliada. A insuficiência adrenal foi mais provável no grupo do etomidato, com uma razão de possibilidades de 6,7 (intervalo de confiança de 95%, 3,5-12,7).17
Surgiram preocupações quanto à longa duração do rocurônio quando comparado ao suxametônio usado em ISRs tradicionais. Contudo, na maioria dos pacientes de trauma graves, acordar o paciente em caso de uma intubação fracassada não é uma opção segura nem viável. Além disso, sabe-se que uma via aérea se torna consideravelmente mais desafiadora em um paciente parcialmente anestesiado no qual o suxametônio já perdeu o efeito.12
A cetamina tem uma ampla margem de erro e mantem certo tônus simpático. Isso a torna uma droga muito útil em casos de trauma, mas deve-se ter cautela com idosos, pois comorbidades cardiovasculares subjacentes podem significar que o impulso simpático fornecido pela cetamina é muito mal tolerado.18 Além disso, em pacientes profundamente hipovolêmicos que estão com esgotamento de catecolamina, a administração de cetamina pode resultar em hipotensão apesar de seus efeitos simpatomiméticos.
Parada cardíaca
Em pacientes com retorno de circulação espontânea após parada cardíaca, é importante manter a estabilidade cardiovascular. Neste cenário, alguns autores sugeriram o uso de midazolam 0,1 mg/kg, fentanil 2mcg/kg, e rocurônio1 mg/kg13 para indução, pois isso pode evitar taquicardia e, desse modo, melhorar a perfusão miocárdica, bem como reduzir os efeitos hipertensivos da intubação ao prevenir um aumento da pós-carga.
Lesão Isolada de Cabeça
Em pacientes com lesão grave na cabeça, a manutenção da pressão arterial sistólica de mais de 90 mmHg mostrou reduzir a mortalidade.16 Para prevenir uma lesão cerebral secundária, uma anestesia balanceada é necessária. Pode-se conseguir isso com o fentanil, propofol, e rocurônio, embora a cetamina associada ao fentanil também seja adequada (v. seção “Controvérsias Atuais”).14 Comumente, uma infusão ou bolus repetidos de vasopressor serão necessários para se manter uma pressão arterial sistólica adequada após a indução.
DROGAS PARA MANUTENÇÃO
Os profissionais da saúde deverão estar cientes de que a indução é meramente o início da anestesia. No período imediatamente após a AEPH, é essencial reavaliar o paciente, otimizar sua condição, e se preparar para o transporte. Este último inclui o planejamento e manutenção da anestesia. É muito fácil perder “tempo“ depois que a intubação ocorre. A orientação do Instituto Nacional de Excelência em Saúde e Cuidado (“NICE”, em inglês) recomenda que o tempo desde a chamada para os serviços de emergência até a indução de AEPH deva ser de menos de 45 minutos. A mesma orientação também sugere que o tempo desde a AEPH até o momento de deixar o local deva ser de menos de 15 minutos. Para se conseguir isso, deve se evitar a “inércia pós-tubo”!20
Várias combinações de drogas podem ser usadas para a manutenção da anestesia, incluindo bolus de cetamina, midazolam e bolus de opiáceos ou infusões de propofol ± opiáceos. A escolha final das drogas de manutenção deve ser individual para cada situação e na experiência do operador. Requer-se cuidado adicional para garantir que as linhas venosas das infusões de manutenção não estejam obstruídas (p.ex.: por um curativo ou um medidor de pressão não-invasivo de ciclo frequente). Devem-se usar doses repetidas de um relaxante muscular não-despolarizante de longa duração.
CONTROVÉRSIAS ATUAIS
Imobilização da Coluna Cervical
A imobilização da coluna cervical é uma questão controversa há vários anos, e o NICE emitiu múltiplas recomendações sobre o assunto, conforme novas evidencias surgem.14 A imobilização da coluna cervical se baseia no princípio de que, após o trauma, pode haver dano à coluna cervical, com potencial de maiores danos caso a coluna cervical seja mobilizada. Alguns autores argumentam que a força inicial significativa aplicada à coluna causa lesão na coluna e dano na medula, não os movimentos subsequentes de baixa força.21 Além disso, eles reconhecem que colares rígidos podem aumentar a pressão intracerebral ao reduzir o fluxo venoso. Como muitas vítimas de trauma com risco de lesão na coluna cervical também estão mais propensas a ter lesões concomitantes na cabeça, este é um fator significativo a ser considerado.19 No contexto de AEPH, a imobilização da coluna cervical com colar geralmente causa uma deterioração significativa no grau de laringoscopia ideal. A orientação mais recente do NICE sugere que, em todas as fases da avaliação, deva-se usar a imobilização manual em linha da coluna, particularmente durante qualquer intervenção em via aérea.20 Deve-se permitir que pacientes que não quiserem cooperar ou que estiverem agitados, bem como crianças, encontrem uma posição confortável. Nesses grupos, os colares não são recomendados, e, ao invés disso, deve-se empregar a estabilização manual em linha quando possível. Os colares são contraindicados em pacientes com vias aéreas comprometidas e deformidades da coluna, como espondilite anquilosante.22 Em suma, o manejo das vias aéreas sempre deve ter prioridade sobre a imobilização da coluna cervical.
Uso Rotineiro de Pressão Cricóide
Em 1961, Sellick23 descreveu, pela primeira vez, a aplicação de pressão sobre a cartilagem cricóide para obstruir o esôfago superior, prevenindo, assim, a regurgitação de conteúdo gástrico na faringe. Desde então, o valor da pressão cricóide tem estado sob escrutínio por causa da falta de evidências confiáveis do benefício e algumas evidências de dano potencial.
Evidências contra seu uso rotineiro incluem relatos de casos de aspiração fatal apesar da pressão cricoide,24,25 impacto negativo na permeabilidade da via aérea e na ventilação,26 piora na visão da laringe, e trauma da via aérea.27 Em uma recente análise baseada em propensão de 1195 pacientes, Caruana et al.27 não descobriram qualquer relação significativa entre pressão cricóide para intubação pré-hospitalar e laringoscopia difícil. Entretanto, os mesmos autores descreveram uma incidência aumentada e estatisticamente significativa de trauma da via aérea relacionado à laringoscopia com a aplicação da pressão cricóide. Ellis e muitos outros, portanto, sugeriram que os profissionais de saúde tenham tanto uma consciência dos problemas potenciais associados à aplicação de pressão cricóide quanto um limiar baixo para remover ou reduzir a pressão durante a AEPH.30,31
Cetamina e Lesão de Cabeça
A cetamina é frequentemente usada em pacientes de trauma por causa de seu conhecido efeito na preservação do tônus simpático. É historicamente sugerido que seu uso está associado a um maior fluxo sanguíneo cerebral, que, por sua vez, leva a uma maior pressão intracerebral, com a última sendo claramente prejudicial em lesões graves na cabeça. Todavia, uma investigação mais recente sobre o uso da cetamina em lesões de cabeça refutou isso, sugerindo, ao invés disso, que seu uso leva a uma redução no consumo de oxigênio cerebral,30 que não aumenta a pressão intracerebral no contexto de ventilação controlada, e que pode, de fato, melhorar a perfusão cerebral. Deve ser, portanto, considerada segura e potencialmente benéfica para uso em pacientes com lesões de cabeça.31
RESUMO
A AEPH é uma intervenção de alto risco que pode ter um impacto positivo significativo no desfecho do paciente, se conduzida apropriadamente. Este tutorial fornece uma visão geral de fatores a serem considerados para a AEPH, incluindo a seleção do paciente, as condições ambientais, as competências da equipe, e a escolha de drogas pra indução e manutenção da anestesia. Leituras adicionais sugeridas incluem a transferência e transporte de pacientes (ATOTW 319 e 330) e o uso de cetamina (ATOTW 381).
REFERÊNCIAS
- Association of Anaesthetists of Great Britain and Ireland. AAGBI: Safer prehospital anaesthesia 2017. Anaesthesia. 2017;72:379-390. https://www.aagbi.org/sites/default/files/Safer%20pre_hospital%20anaesthesia2017_0.pdf. Accessed May 20, 2018.
- National Enquiry Into Patient Outcome and Death. Trauma: who cares? http://www.ncepod.org.uk/2007report2/ Downloads/SIP_summary.pdf. Published 2007. Accessed May 20, 2018.
- Smith RM, Conn AK. Prehospital care—scoop and run or stay and play? Injury. 2009;40(suppl 4):S23-S26.
- Kauver DS, Wade CE. The epidemiology and modern management of traumatic hemorrhage: US and international perspectives. Crit Care.2009;5:S1.
- Royal College of Anesthetists and Difficult Airway Society. 4th National Audit Project (NAP4): major complications of airway management in the United Kingdom report and findings. https://www.rcoa.ac.uk/node/4211. Published March 2011. Accessed May 5, 2018.
- Silvestri S, Ralls GA, Krauss B, et al. The effectiveness of out-of-hospital use of continuous end-tidal carbon dioxide monitoring on the rate of unrecognized misplaced intubation within a regional emergency medical services system. Ann Emerg Med. 2005;45;497-503.
- Li J, Murphy-Lavoie H, Bugas C, et al. Complications of emergency intubation with and without paralysis. Am J Emerg Med. 1999;17:141-143.
- Lockey DJ, Crewdson K, Lossius HM. Pre-hospital anaesthesia: the same but different. Br J Anaesth. 2014;113(2):211-219. https://doi.org/10.1093/bja/aeu205. Accessed May 20, 2018.
- Cantle PM, Cotton BA. Balanced resuscitation in trauma management. Surg Clin North Am 2017;97:999-1014.
- Gerhardt RT, Strandenes G, Cap AP, et al. Remote damage control resuscitation and the Solstrand Conference: defining the need, the language, and a way forward. Transfusion. 2013;53:9S-16S.
- Chrimes N, Fritz P. The vortex approach. Safe Apnoea time website. http://vortexapproach.org/safeapnoeatime/#apox. Published 2016. Accessed May 20, 2018.
- Awes EG, Campbell I, Mercer D. Inflation pressure, gastric insufflation and rapid sequence induction. Br J Anaesth. 1987;59:315-318.
- Lyon RM, Perkins AB, Chatterjee D, et al. Significant modification of traditional rapid sequence induction improves safety and effectiveness of pre-hospital trauma anaesthesia. Crit Care. 2015;19:134.
- Miller M, Groombridge CJ, Lyon R. Haemodynamic changes to a midazolam–fentanyl–rocuronium protocol for pre- hospital anaesthesia following return of spontaneous circulation after cardiac arrest. Anaesthesia. 2017;72:585-591.
- Hossfeld B, Bein B, Boettiger BW, et al. Recommended practice for out-of-hospital emergency anaesthesia in adults: statement from the Out-of Hospital Emergency Anaesthesia Working Group of the Emergency Medicine Research Group of the German Society of Anaesthesiology and Intensive Care. Eur J Anaesthesiol. 2016;33(12):881-897.
- Oglesby A. Should etomidate be the induction agent of choice for rapid sequence intubation in the emergency department? Emerg Med J. 2004;21:655-659.
- Jabre P, Combes X, Lapostolle F, et al. Etomidate versus ketamine for rapid sequence intubation in acutely ill patients: a multicentre randomised controlled trial. Lancet. 374:9686:293-300.
- Joint Formulary Committee, ed. BNF (British National Formulary) 74. Chapter 15 “Anaesthesia”, London, UK: Pharmaceutical Press; 2017 2018:1234.
- Miller M, Kruit N, Heldreich C, et al. Response after rapid sequence induction with ketamine in out-of-hospital patients at risk of shock as defined by the shock index. Ann Emerg Med. 2016;68(2):181-188.e2.
- NICE guidance [NG39]. Major trauma: assessment and initial management. https://www.nice.org.uk/guidance/ng39/ chapter/Recommendations. Published February 2016. Accessed August 16, 2018.
- Benger J, Blackham J. Why do we put cervical collars on conscious trauma patients? Scand J Trauma Resusc Emerg Med. 2009;17:44
- NICE guideline [NG41]. Spinal injury: assessment and initial management. https://www.nice.org.uk/guidance/ng41/ chapter/Recommendations. Published February 2016. Accessed May 20, 2018.
- Sellick BA. Cricoid pressure to control regurgitation of stomach contents during induction of anaesthesia. Lancet. 1961;2:404-406.
- Robinson JS, Thompson JM. Fatal aspiration (Mendelson’s) syndrome despite antacids and cricoid pressure. Lancet. 1979;2:228-230.
- Williamson R. Cricoid pressure. Can J Anaesth. 1989;36:601.
- Hartsilver EL, Vanner RG. Airway obstruction with cricoid pressure. Anaesthesia. 2000;55:208-211.
- Caruana E, Chevret S, Pirracchio R. Effect of cricoid pressure on laryngeal view during prehospital tracheal intubation: a propensity-based analysis. Emerg Med J. 2017;34:132-137.
- Ellis DY, Harris T, Zideman D. Cricoid pressure in emergency department rapid sequence tracheal intubations: a risk- benefit analysis. Ann Emerg Med. 2009;50(6):653-665.
- Harris T, Ellis, D, Foster L, et al. Cricoid pressure and laryngeal manipulation in 402 pre-hospital emergency anaesthetics: essential safety measure or a hindrance to rapid safe intubation? Resuscitation. 2010;81(7):810-816.
- Morris C, Perris A, Klein J, et al. Anaesthesia in haemodynamically compromised emergency patients: does ketamine represent the best choice of induction agent? Anaesthesia. 2009;64:532-539.
- Himmelseher S, Durieux ME. Revising a dogma: ketamine for patients with neurological injury? Anesth Analg. 2005;101:524-534.



