Paediatric Anaesthesia
PUNTOS CLAVES
- La anestesia para niños con cardiopatía compleja en el ambiente remoto de un lab cat puede ser desafiante.
- La ketamina es un fármaco clave para pacientes con función cardíaca deteriorada.
- Las infecciones torácicas recurrentes son frecuentes en niños con cardiopatía, especialmente en aquellos con exceso de flujo sanguíneo pulmonar. Las infecciones respiratorias deben ser tratadas antes de proceder con casos electivos.
- El ayuno debe mantenerse al mínimo y evitarse la deshidratación.
- Es muy fácil que el niño se enfríe. Mantener la normotermia.
INTRODUCCIÓN
Las intervenciones diagnósticas y mínimamente invasivas en el laboratorio de cateterismo cardíaco (lab cat) son ahora de rutina en el manejo de niños con cardiopatía congénita (CC). Los niños pueden presentarse a cualquier edad, incluso neonatos, para procedimientos electivos o de emergencia. La mayoría de los procedimientos requieren que el niño sea anestesiado. Es importante comprender la anatomía y fisiología cardíaca de cada niño y los riesgos potenciales, los beneficios y las complicaciones de las intervenciones que se están llevando a cabo. La comunicación efectiva con el equipo, y la constante vigilancia son esenciales cuando se manejan estos casos complejos. Con un buen cuidado clínico, la mayoría de los pacientes pueden ser dados de alta a una sala de cuidados cardíacos al final del procedimiento, haciendo que el tratamiento de los niños en el lab cat sea una opción realista para todos los pacientes, incluso en países con recursos limitados.
PRINCIPIOS GENERALES
Equipo
Los lab cat cardíacos tienden a situarse en áreas remotas del hospital. En adultos, los procedimientos a menudo se realizan bajo anestesia local o sedación y, como tal, los recursos o equipos de anestesia disponibles pueden no ser siempre óptimos. Es más común que los niños requieran de anestesia general y por lo tanto es esencial que el mismo estándar de cuidado anestésico se proporcione como en cualquier otro lugar del hospital. El anestesista debe estar familiarizado con el equipo anestésico y debe chequearlo previo a la operación.1
La monitorización básica es fundamental y debe incluir, como mínimo, oximetría de pulso, electrocardiografía (EKG) y monitorización de la presión arterial (PA). Debe estar disponible un desfibrilador con paletas pediátricas o almohadillas atenuadas. El operador debe estar entrenado para usar este dispositivo.1
El lab cat es a menudo frío y el paciente puede estar expuesto al preparar el caso. Es fácil para los niños hacer hipotermia. Esto puede promover arritmias y retrasar la recuperación de la anestesia. El calentamiento activo con una manta de aire es ideal, y como mínimo, el paciente debe mantenerse cubierto y la temperatura del cuarto controlada para satisfacer las necesidades del paciente.1
La ecocardiografía (ECG) es esencial en el lab cat. Se utiliza para diagnosticar o confirmar lesión cardíaca, medir los gradientes de presión, verificar el posicionamiento de los dispositivos desplegados y evaluar las lesiones cardíacas después de una intervención (p.e. taponamiento o nueva regurgitación valvular).
Investigaciones Preoperatorias
Todos los pacientes deben tener una hematología completa preoperatoria. Para los procedimientos intervencionistas debe estar disponible un concentrado globular guardado, y para procedimientos de mayor riesgo, p.e. dilatación de válvulas con balón, la sangre debe tener pruebas cruzadas y estar disponible al momento. Debe chequearse el azúcar en sangre, electrolitos, función renal y función hepática según lo indicado localmente, pero particularmente en pacientes con función cardíaca significativamente deteriorada o aquellos con enfermedades coexistentes complejas. La trombocitopenia puede observarse en pacientes con hipoxia severa y policitemia compensatoria. El cateterismo cardíaco debería tener lugar idealmente cuando el recuento de plaquetas sea superior a 100 x 109/L, lo que puede requerir transfusión para lograrlo.
Un EKG de 12 derivaciones preoperatorio es importante, particularmente en niños con arritmias conocidas, y actúa como referencia si se desarrollan cambios.
Ayuno
Los pacientes deben estar en ayuno antes de la operación, pero el problema más común en todas partes del mundo es que los líquidos claros se detienen durante demasiado tiempo. El ayuno de líquidos prolongado hará que el niño esté irritable, más propenso a hacer hipoglucemia y, si está deshidratado, más difícil de canular. Es particularmente importante evitar la deshidratación de los pacientes con hipoxia severa que tienen policitemia, ya que aumenta el riesgo de complicaciones trombóticas.2,3 Los pacientes que se encuentran de último en la lista pueden llegar a estar cada vez más deshidratados durante su espera y se le deben dar instrucciones claras sobre el tipo y la cantidad de líquido que pueden recibir (Véase el Tutorial 352 de la ATOTW para más información y los tiempos de ayuno recomendados).
Resumen del equipo al comienzo de la lista
Al igual que con todas las listas, es una buena práctica iniciar la lista en el lab cat con un “resumen del equipo”.4 Esta es una oportunidad para que los miembros del equipo se presenten, revisen cada caso de la lista y confirmen el orden de la lista (véase el Tutorial 325 de la ATOTW). En el Great Ormond Street Hospital debatimos lo siguiente al comienzo de cada lista de cateterismo:
- Revisar todos los pacientes de la lista y discutir cualquier preocupación específica del paciente
- Confirmar si las pruebas cruzadas son requeridas y están disponibles
- Algún equipo especial requerido, incluyendo monitorización invasiva
- Requerimientos de imágenes
- Requerimientos de antibióticos
- Calentamiento
- Quien está operando y quien está asistiendo
- Cualquier otra cuestión como personal o tiempo
Técnica anestésica
Se debe elegir una técnica anestésica que permita una recuperación segura y rápida del paciente y regresar a la sala en el postoperatorio. Esto será determinado por la preferencia local. La técnica habitual de elección es la anestesia balanceada con ventilación controlada, con o sin el uso de un relajante muscular. Los relajantes musculares de acción prolongada como el pancuronio son los que se evitan. La ventilación espontánea sin intubación puede ser una opción, y a menudo se utiliza en países con recursos limitados para casos cortos en los que la ketamina puede ser utilizada como agente único. La anestesia inhalatoria profunda, particularmente con halotano, es mejor evitarla para mantener la estabilidad hemodinámica.5,6
Es esencial obtener un acceso vascular seguro, a pesar de la presión de otros para proceder. El fracaso para asegurar un buen acceso vascular puede lamentarse después si ocurre un evento adverso grave. En algunos niños, el acceso vascular se puede lograr en la sala previamente lo que ahorrará tiempo valioso del lab cat. Alternativamente, el acceso se puede conseguir después de la inducción de la anestesia con un agente inhalatorio o ketamina (5-10 mg/kg IM o 2 mg/kg IV).
Durante el cateterismo, las lecturas directas de la presión cardiaca y arterial se pueden medir como parte del trabajo diagnóstico y se repiten para evaluar cambios post intervención. La concentración de la fracción inspirada oxígeno [FiO2] administrada puede tener efectos significativos sobre la resistencia vascular pulmonar y, como tal, afectará las lecturas de presión tomadas durante el cateterismo. Seguido de una inducción segura, el objetivo es suministrar el mismo requerimiento de oxígeno al que el paciente normalmente estaría expuesto (es decir, cerca de [FiO2] 0,21 si ventila espontáneamente a aire ambiente), pero se comunica con el cardiólogo a la brevedad si se tiene dudas.5,6
Mantenimiento hídrico
El mantenimiento con líquidos isotónicos, como el Ringer Lactato o Hartmann, deben utilizarse para todos los pacientes. Si hay preocupación por la hipoglucemia (p.e., ayuno prolongado), se puede añadir 10-50 ml de glucosa 50% a una bolsa de 500 ml de líquido para preparar una solución de 1-5% de glucosa/Ringer (o Hartmann). Los niveles de glucosa en sangre deben medirse en esta situación. No hay lugar para mantenimiento con líquidos hipotónicos en la práctica moderna de la anestesia pediátrica.7
Cuidados postoperatorios
El niño debe recuperarse completamente antes de regresar a la sala, idealmente después de un período de tiempo en una sala de recuperación con personal, oxígeno, succión y monitoreo disponibles. El sitio de punción vascular debe ser revisado para detectar sangrado antes de regresar a la sala, particularmente donde se ha obtenido el acceso arterial.5,6
SITUATIONES ESPECÍFICAS
Hipertensión Pulmonar
La hipertensión pulmonar (HP) se diagnostica cuando la presión de la arteria pulmonar media en reposo (PAPm) supera los 25 mmHg. Después de la inducción anestésica, la FiO2 debe reducirse lo más cerca posible del aire ambiente o la FiO2 mínima que el paciente puede tolerar con seguridad para permitir las mediciones de la PAP. Se administra 100% de O2 durante 10 minutos y se vuelve a medir la PAP para evaluar la evidencia de reversibilidad de HP, definida como una reducción del 15% en la PAPm frente a la presión arterial media (PAM) [sin un cambio significativo en la PAM]. La FiO2 se debe aumentar durante la prueba si hay hipoxia profunda o se observa cualquier cambio isquémico.8,9
Tetralogía de Fallot (TF)
En muchas situaciones, el diagnóstico completo de pacientes con TF se logra utilizando la ECG. En algunos centros, particularmente donde no se dispone de las habilidades de la ECG, el cateterismo cardíaco puede llevarse a cabo para:
- Evaluar el curso y la gravedad de la obstrucción del tracto de salida del ventrículo derecho (TSVD)
- Mapear el suministro de sangre coronaria y buscar alguna arteria coronaria aberrante cruzando el infundíbulo del
ventrículo derecho (que podría verse comprometida durante la cirugía si no se reconoce) - Identificar las arterias principales aorto-pulmonares colaterales (APAPCs)
El mayor riesgo durante el cateterismo cardíaco de un niño con TF no reparada es un “hechizo” hipercianótico, particularmente si el catéter de angiografía estimula el área infundibular del TSVD. El espasmo infundibular se debe a la contracción de los haces musculares en el TSVD, particularmente si el tono simpático es alto (adrenoceptor beta-1). Esto resulta en un aumento de la derivación derecha a izquierda y a hipoxemia profunda. El riesgo de este hechizo puede minimizarse reduciendo el impulso simpático, incluyendo la premedicación, utilizando anestesia balanceada y analgesia con opioides, y evitando de manera importante la anestesia “ligera”. Se debe evitar la epinefrina, ya que esto empeorará cualquier obstrucción del TSVD.5,6,10
Un hechizo cianótico debe ser tratado de la siguiente manera:
- Aumentar la FiO2
- Dar un bolo de líquido IV de 10ml/kg de solución isotónica, reevaluar y repetir si es necesario. Esto aumentará la postcarga y el flujo sanguíneo pulmonar.
- Fenilefrina (bolos de 1 mcg/kg) o infusión de norepinefrina (0,05-0,1mcg/kg/min). Estos son agonistas de adrenoceptores alfa puros – que aumentan la resistencia vascular sistémica (RVS), que reduce la derivación derecha a izquierda, que a su vez aumentará el flujo a través del TSVD.
- Bloqueadores-Beta p.e. esmolol (0,5mg/kg IV durante 1 min, repetir si es necesario, o infusión de 25- 300mcg/kg/min) o metoprolol (0,1 mg/kg IV durante 5 min, máximo 5mg). Esto debe aliviar el espasmo infundibular y reduce la obstrucción del TSVD.10

Ventrículos únicos
Los niños con fisiología del ventrículo único (por ejemplo, síndrome del corazón izquierdo hipoplásico, atresia tricúspidea) requieren una serie de procedimientos paliativos para la supervivencia a largo plazo. Después de la paliación inicial en el período neonatal para asegurar el flujo sanguíneo sistémico y pulmonar, se requieren procedimientos adicionales para asegurar un flujo sanguíneo pulmonar adecuado a medida que el niño crece. La derivación bidireccional de Glenn (DBG) se forma en la infancia mediante la anastomosis de la vena cava superior (VCS) a la arteria pulmonar, y alrededor de los 2-4 años de edad, la conexión pulmonar caval total (CPCT o circulación Fontan) se forma por la anastomosis de la vena cava inferior (VCI) a la arteria pulmonar a través de un injerto de interposición. El retorno venoso de la VCS y la VCI proporciona entonces el flujo sanguíneo pulmonar en una circulación completamente “en serie” con el único ventrículo como la única bomba. La finalización exitosa de la CPCT requiere que la PAP sea baja, ya que la presión de impulsión para el flujo sanguíneo pulmonar es la presión en la VCS/VCI.11
Se puede llevar a cabo un cateterismo cardíaco diagnóstico como parte del plan de trabajo para una CPCT. Se puede pedir al anestesista que inserte un catéter en la vena yugular interna para medir la presión en la DBG para estimar la PAP. Idealmente, los niños con fisiología de ventrículo único para procedimientos de cateterismo deben mantenerse “bien llenos” para facilitar el retorno venoso y por lo tanto el flujo sanguíneo pulmonar. Es muy importante evitar el ayuno prolongado y la deshidratación en este grupo de pacientes. Durante la anestesia el paciente debe ser intubado y proporcionársele ventilación con presión positiva. Se deben establecer pequeños volúmenes corrientes (≤7ml/kg) para evitar el aumento de la resistencia vascular pulmonar (RVP) observada con grandes volúmenes corrientes. Además, las concentraciones de CO2 al final de la espiración [EtCO2] se deben controlar para evitar cambios no deseados de la RVP de hiper o hipoventilación, y más importante, asegurar un adecuado retorno venoso de la circulación cerebral a la VCS.
Ecocardiografía transesofágica (ETE)
La ETE se utiliza para guiar intervenciones, como la colocación de dispositivos en el DSA secundario, o para mejorar la información diagnóstica cuando se encuentra que la ecocardiografía transtorácica tiene una capacidad diagnóstica inferior, p.e. DSA sinus venosus. Se requiere intubación traqueal y ventilación controlada. Una ETE diagnóstica es generalmente un procedimiento corto que requiere sólo un breve período de intubación. Se puede usar un relajante muscular de acción intermedia para facilitar la intubación, p.e. atracurio, o si no está disponible, suxametonio, que se utiliza con frecuencia en países con recursos limitados. Algunos centros pueden tener el beneficio de tener rocuronio y sugammadex disponibles.5,6,10
PROCEDIMIENTOS INTERVENCIONISTAS
Los procedimientos intervencionistas sólo deben llevarse a cabo en centros en los que el respaldo quirúrgico está disponible inmediatamente para ayudar con las complicaciones, p.e. embolización de un dispositivo de oclusión septal o trauma significativo de una estructura cardíaca.5,6,10,12
La sangre debe tener pruebas cruzadas y estar disponible inmediatamente para procedimientos intervencionistas. La mayoría de las intervenciones intentan cerrar un defecto abierto o no deseado, o agrandar o crear un defecto. Los catéteres intervencionistas tienen diámetros mayores que los utilizados en procedimientos diagnósticos y tienen un mayor riesgo de lesión vascular.
Las intervenciones comunes realizadas en el lab cat incluyen:
- Cierre de DAP
- Cierre del DSA
- Valvulotomía pulmonar
- Valvulotomía aortica
- Septostomía auricular
- Stents vasculares (coartación, vasos pulmonares)
- Oclusión de vasos colaterales
- Inserción de válvula pulmonar
Cierre del ductus arterioso persistente (DAP)
Un ducto arterioso persistente (DAP) con derivación izquierda a derecha conduce a un sobreflujo pulmonar con signos y síntomas de insuficiencia cardíaca congestiva (Figura 1). Los pacientes sufren desde infecciones torácicas repetidas y fracasos hasta prosperar. Pequeños DAPs aislados en bebés y niños mayores son susceptibles para dispositivos de oclusión en el lab cat. La mayoría de los agentes anestésicos reducen la RVS y la derivación a través del DAP. Evitar FiO2 alta en estos pacientes (si es posible), debido a que el O2 reduce la RVP y aumenta el flujo sanguíneo pulmonar a través del conducto. Recomendamos una técnica anestésica balanceada con intubación y ventilación, aunque también es posible manejar estos procedimientos usando ketamina en un paciente con respiración espontánea.5,6,10,12
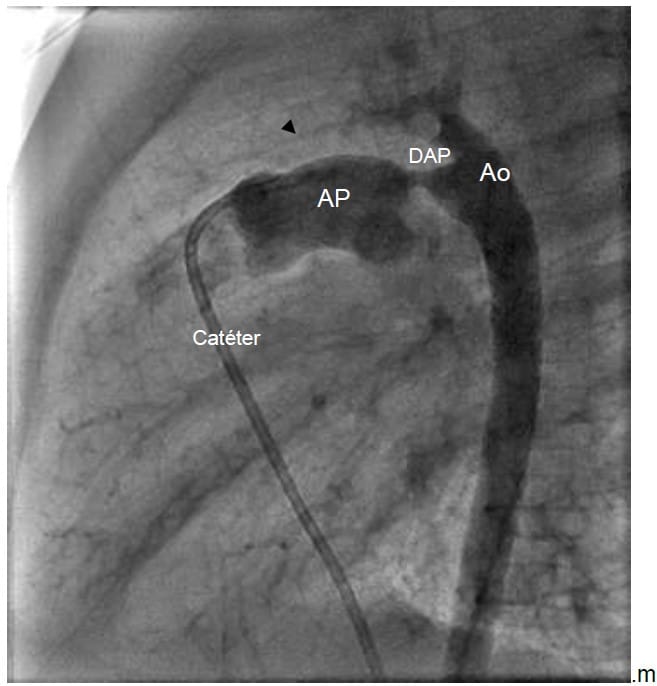
Figura 1. Imagen de cateterismo cardíaco: ductus arterioso persistente
(DAP: ductus arterioso persistente; AP: arteria pulmonar; Ao: Aorta)
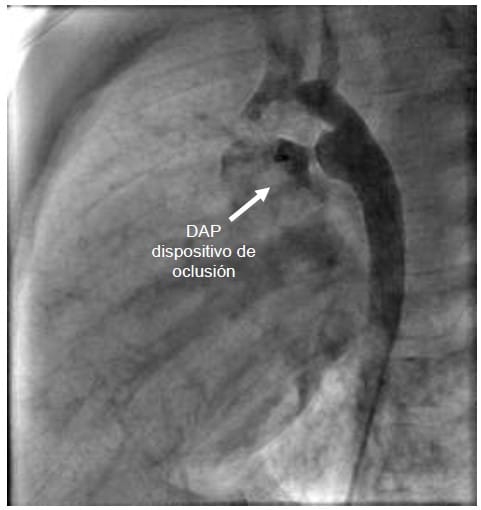
Figura 2. Imagen de cateterismo cardíaco: Posterior al dispositivo de oclusión en el ductus arterioso persistente.
Cierre del defecto septal auricular (DSA)
El DSA se puede cerrar por vía percutánea bajo guía angiográfica y ETE (Fig. 3). Las indicaciones para el cierre del DSA con dispositivo percutáneo se basan en los hallazgos clínicos y ECG. Específicamente, la evaluación del tamaño, anatomía y ubicación del DSA determinarán si el procedimiento es factible. Las indicaciones para el cierre electivo incluyen aquellos con evidencia de sobreflujo pulmonar excesivo desde un shunt significativo [flujo pulmonar [Fp]: índice de flujo sistémico [Fs] > 1.5) y pacientes con sobrecarga ventricular derecha. 5,6
Se deben administrar antibióticos intravenosos profilácticos dentro de los 30 minutos del inicio del procedimiento y el paciente debe estar anticoagulado con heparina de acuerdo con el protocolo local. Si el DSA se considera inadecuado para dispositivo de oclusión guiado por angiografía, se debe revertir la heparina con protamina, guiado por tiempo de coagulación activada (TCA). Se debe tener especial cuidado en verificar el sangrado después del procedimiento si se ha utilizado una vaina grande y se debe comprimir el sitio de punción durante al menos 10 minutos. El dispositivo de oclusión del DSA se asocia con arritmias por manipulación del catéter, trauma de las estructuras cardíacas y embolismo aéreo. Si se produce embolización del oclusor septal, el cardiólogo intervencionista deberá retirar urgentemente el dispositivo y puede implicar de cirugía cardiotorácica si esto no puede lograrse por vía percutánea.5,6,10,12
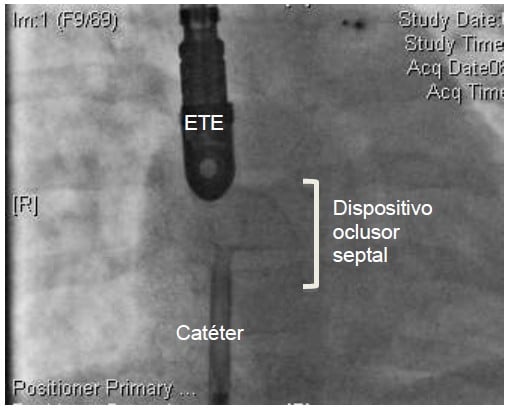
Figura 3. Imagen de cateterismo cardíaco: oclusión del defecto septal auricular (DSA) guiada por ecocardiografía transesofágica (ETE). Todas las imágenes amablemente proporcionadas por el Departamento de Cardiología del Great Ormond Street Hospital.
Valvulotomía Pulmonar
La estenosis significativa de la válvula pulmonar (VP), definida como un gradiente de presión a través de la VP mayor de 50mmHg, es indicación para valvulotomía pulmonar. El área de la VP puede ser muy pequeña o como una hendidura y el flujo de salida del ventrículo derecho (VD) se ocluye fácilmente cuando se realiza el cateterismo. Durante este tiempo, el paciente quedará profundamente desaturado mientras el flujo sanguíneo pulmonar esté obstruido. El catéter debe retirarse hasta que la SpO2 se normalice. Se inserta un catéter con punta de balón bajo control fluoroscópico y se infla el balón momentáneamente para dividir la comisura entre las valvas de la válvula. Por lo general, es aceptable un gradiente de presión posterior al procedimiento a través de la VP inferior a 40mmHg. 5,6,10
Valvulotomía Aortica
Los niños con estenosis aórtica (EA) significativa tendrán hipertrofia ventricular izquierda y pueden demostrar evidencia de una función ventricular izquierda reducida. Debe mantenerse la RVS en pacientes con EA para prevenir isquemia coronaria. La valvulotomía aórtica mediante dilatación con balón está indicada si:
- El gradiente de presión de la válvula aortica (VAo) es > 70mmHg
- Gradiente de presión de la VAo > 50mmHg con síntomas tales como dolor torácico, o si hay signos de isquemia en el EKG
Durante la colocación del catéter con punta de balón a través de la válvula, la sangre que fluye a través del tracto de salida del ventrículo izquierdo puede desplazar el dispositivo de balón lejos de la VAo. La sobreestimulación rápida del ritmo se puede utilizar para reducir el gasto cardíaco durante este procedimiento, para reducir el gasto cardíaco de forma aguda y mejorar el éxito del procedimiento. La incompetencia aórtica (IA) severa por la dilatación excesiva de la VAo puede causar insuficiencia coronaria. 5,6,10,12
Coartación de la aorta (CoA)
La coartación aórtica severa generalmente requiere cirugía en la infancia, pero los grados moderados de coartación o estenosis residual después del tratamiento quirúrgico inicial se pueden tratar en el lab cat. En pacientes jóvenes adecuados, la CoA generalmente se trata con angioplastia con balón. En niños mayores, se puede colocar un stent a través de la coartación si la anatomía es adecuada. Las complicaciones incluyen ruptura aórtica, disección aórtica, eventos cerebrovasculares, traumatismo de la arteria femoral, trombosis y formación de aneurismas. La sangre con pruebas cruzadas debe estar disponible. 5,6,10,12
Los niños mayores a menudo tienen hipertensión en miembros superiores, por lo que es sensato colocar el manguito de presión o una línea arterial en el brazo derecho para obtener una medida real de la presión arterial. La anestesia para el tratamiento de la coartación aórtica debe tener como objetivo mantener la estabilidad hemodinámica, pero no reducir la presión arterial en exceso. En niños más jóvenes, la anestesia inhalatoria con pequeñas dosis de opioide, p.e. fentanilo (1-2mcg/kg) o ketamina (0.5mg/kg), generalmente es una combinación segura. Las técnicas de anestesia total intravenosa pueden ser adecuadas en niños mayores.
Septostomía Auricular con Balón (SAB)
La principal indicación para septostomía auricular es mejorar la mezcla entre las circulaciones sistémica y pulmonar en neonatos con dextro-transposición de grandes arterias (d-TGA) y oxigenación insuficiente, antes de la cirugía correctiva. Los neonatos con TGA suelen presentar hipoxia y acidemia. Aquellos con mejor mezcla, p.e. ductus arterioso persistente (DAP) tienen mayor probabilidad de sobrevivir. La SAB también se puede usar para mejorar la mezcla en otras CC cianóticas potencialmente mortales, p.e. atresia pulmonar con septum ventricular intacto, atresia tricúspidea y síndrome de corazón izquierdo hipoplásico (SCIH). Se pasa un catéter con punta de balón a través del foramen oval desde la aurícula derecha hasta la izquierda y se tira hacia atrás con el globo inflado para crear la septostomía. El procedimiento se lleva a cabo bajo guía ECG con o sin sedación, y es bien tolerado en manos expertas de cardiología.5,6,10
Cierre del defecto septal ventricular (DSV)
El dispositivo de oclusión del DSV es complejo y requiere anestesia general con intubación traqueal y guía con ETE. Existe un alto riesgo de inestabilidad cardiovascular y tiempo operatorio prolongado, y solo debe realizarse en centros con experiencia. 10
Taponamiento cardíaco
El taponamiento cardíaco afecta el retorno venoso y conduce a una reducción del gasto cardíaco (GC). Mantener la frecuencia cardíaca es crucial para evitar la descompensación rápida. Los fármacos vasoactivos (atropina y epinefrina) deben prepararse con anticipación. Los niños con taponamiento severo están muy enfermos y la ketamina es la droga anestésica de elección. El mantenimiento de la precarga es crucial en el taponamiento. La respiración espontánea es mejor tolerada que la ventilación con presión positiva, ya que puede impedir el retorno venoso adicional, aumentar la poscarga del VD y reducir más el GC. Después de drenar el taponamiento (generalmente con un catéter), un retorno repentino en el flujo sanguíneo pulmonar puede precipitar edema pulmonar. El monitoreo invasivo es esencial para estos casos de alto riesgo 5,6,10,12
Estudios Electrofisiológicos (EF)
Los pacientes que tienen arritmias cardíacas sintomáticas debido a vías de conducción patológica pueden tratarse con éxito en el lab cat con ablación por radiofrecuencia o crioablación de las vías de conducción anormales. Los pacientes tendrán que suspender sus fármacos antiarrítmicos antes del estudio, pero la anestesia suprime el impulso simpático endógeno y la provocación de la arritmia durante el procedimiento puede ser más difícil. Hay un equilibrio fino para garantizar que el paciente esté completamente anestesiado, no demasiado profundo bajo anestesia, pero lo que es importante, que no esté consciente. Las arritmias en discusión, p.e. la fibrilación ventricular o la taquicardia ventricular sostenida, aunque poco frecuentes, pueden ocurrir y deben tratarse con desfibrilación. Las taquicardias supraventriculares pueden responder a la adenosina, pero deben ser cardiovertidas si el paciente está comprometido. La anestesia general con intubación traqueal es necesaria para los estudios EF, ya que estos son procedimientos largos con múltiples catéteres intravasculares grandes. La anestesia total intravenosa basada en propofol es una técnica popular. Sevoflurane con uso juicioso de opioides es una opción alternativa. La dexametasona limita el tamaño de la “quemadura” por ablación por radiofrecuencia y no se debe utilizar como antiemético de rutina en estos pacientes. 5,13
COMPLICACIONES COMUNES VISTAS EN EL LAB CAT
Complicaciones relacionadas a la anestesia
Los pacientes pueden tener una reserva funcional pulmonar y cardiovascular limitada. La depresión respiratoria y la hipoxia ocurren rápidamente después de la inducción de la anestesia, especialmente en neonatos e infantes. La monitorización adecuada de la respiración es esencial durante todo el caso.
Todos los agentes anestésicos son depresores cardiovasculares directos. Con la ketamina, su actividad depresora directa del miocardio se ve compensada por su efecto estimulador a través de la inhibición de la recaptación de catecolaminas. Sin embargo, la ketamina está asociada con delirio. Esto puede ser aminorado con midazolam en pacientes mayores. Los opioides como el fentanilo son una excelente opción como parte de una técnica multimodal, pero se asocian comúnmente con náuseas y vómitos postoperatorios, y los antieméticos deben usarse de manera rutinaria en niños mayores. 5,6
Complicaciones relacionadas al entorno
El lab cat es un ambiente frío y la hipotermia puede desarrollarse fácilmente, especialmente en neonatos e infantes. Se debe usar calentamiento activo, con temperatura registrada durante todo el caso. La hipotermia retrasará la recuperación de la anestesia y puede provocar arritmias. 5,6
Complicaciones relacionadas al procedimiento
El acceso vascular con vainas grandes puede comprometer la perfusión distal y puede resultar en una perfusión deficiente o incluso isquemia de las extremidades inferiores. Las arritmias ocurren con frecuencia y se deben principalmente a la presencia de catéteres intracardíacos. Estos generalmente se resuelven con la extracción del catéter. Otras causas incluyen alteraciones electrolíticas, hipercapnia o embolismo aéreo coronario. El contraste es nefrotóxico y puede precipitar reacción alérgica y, ocasionalmente, tos intratable. Es importante limitar la carga de contraste tanto como sea posible.
Otras complicaciones menos comunes incluyen embolización del dispositivo, fractura del catéter, traumatismo valvular, taponamiento cardíaco, trauma vascular y sangrado en los sitios de acceso femoral. La mayoría de las complicaciones se tratan en el lab cat, pero ocasionalmente estas complicaciones más graves requieren cirugía de emergencia. 5,6
SEGURIDAD RADIOLÓGICA
Es importante que cualquier persona que trabaje en el lab cat conozca la seguridad radiológica y los riesgos que representan para los pacientes y los trabajadores de la salud. 5,14 Se debe seguir la guía nacional sobre seguridad radiológica. Todas las niñas en edad fértil deben chequear su estado de embarazo. La dosis de radiación para los pacientes y el personal debe minimizarse tanto como sea posible. Los factores que afectan la dosis de radiación son la distancia, las barreras y el tiempo de exposición:
- Distancia: La dosis de radiación se reduce a medida que aumenta la distancia desde la fuente. El anestesista puede estar expuesto a altas dosis de radiación si permanece cerca del paciente durante el examen.
- Barreras: Se debe usar ropa protectora como delantales de plomo, collar de tiroides y gafas protectoras. El umbral de exposición para formación de cataratas puede alcanzarse en unos pocos años sin las precauciones adecuadas.
- Tiempo: La detección mediante fluoroscopia aumenta en gran medida el riesgo de exposición para el cardiólogo y el anestesista. La exposición máxima a la radiación recomendada para trabajadores médicos es de 5rem/año. Idealmente, la exposición debería ser mucho menor que esto. La exposición durante la fluoroscopia de cine puede ser particularmente alta, por lo que es importante usar un conductor de protección y mantenerse lo más lejos posible de la fuente de radiación durante el estudio…
RESUMEN
- Es importante comprender la anatomía cardíaca individual y la fisiología de cada niño para administrar la anestesia balanceada más segura y efectiva en el lab cat.
- Relacionarse con el cardiólogo para entender sus requerimientos para cada caso los cuales guiarán cualquier medida anestésica necesaria (p.e. ventilar con aire ambiente). Asegurar que cualquier medida tomada no comprometerá la seguridad del paciente. Como en todos los casos, la comunicación es clave.
- En la actualidad, es posible aumentar las técnicas de diagnóstico e intervención en el lab cat, y al igual que en otros sitios anestésicos remotos, debe haber toda la gama de controles de seguridad, incluida la disponibilidad de sangre, para cualquier complicación no deseada que pueda ocurrir.
REFERENCIAS Y LECTURA ADICIONAL
- Association of Anaesthetists of Great Britain and Ireland. Recommendations for standards of monitoring during anaesthesia and recovery 2015. Anaesthesia 2016; 71: 85-93
- Anderson H, Zaren B, Frykholm P. low incidence of pulmonary aspiration in children allowed intake of clear fluids until called to the operating suite. Paediatr Anaesth. 2015 Aug;25(8):770-7
- APA consensus guideline on perioperative fluid management in children: V 1.1 September 2007
- Organization WHO. WHO guidelines for safe surgery: safe surgery saves lives 2009 [cited 2017 1st April]. Available from: http://www.who.int/patientsafety/safesurgery/tools_resources/9789241598552/en/
- Qureshi S, Pushparajah K, Taylor D. Anaesthesia for paediatric diagnostic and interventional cardiological procedures, Contin Educ Anaesth Crit Care Pain 2015;15(1):1-6.
- Lam J, Lin E, Alexy R et al. Anesthesia and the pediatric cardiac catheterization suite: a review. Pediatric anesthesia 2015: 25(2)127–134.
- National Institute for Health and Care Excellence. Intravenous fluids therapy in children. (Clinical guideline NG29.) 2015.
- Tempe DK. Perioperative management of pulmonary hypertension. Annals of Cardiac Anesthesia 2010; 13(2):89-91.
- Goyal P, Kiran U, Chauhan S et al. Efficacy of nitroglycerin inhalation in reducing pulmonary arterial hypertension in children with congenital heart disease. British Journal of Anesthesia 2006; 97(2): 208-14.
- Reddy K, Jagger S, Gillbe C. The anaesthetist and the cardiac catheterisation laboratory, Anaesthesia 2006; 61:1175-1186.
- Feinstein JA, Benson DW, Dubin AM, et al. Hypoplastic Left Heart Syndrome: Current Considerations and Expectations. J Am Coll Cardiol 2012; 59 Suppl S:S1–S42.
- Thangavel P, Muthukumar S, Karthekeyan et al. Anaesthetic Challenges in Cardiac Interventional Procedures, World Journal of Cardiovascular Surgery, 2014, 4, 206-216.
- Ashley E. Anaesthesia for electrophysiology procedures in the cardiac catheter laboratory. Contin Educ Anaesth Crit Care 2012; 12(5):230-236.
- Taylor J, Chandramohan M, Simpson K. Radiation safety for anaesthetists. Contin Educ Anaesth Crit Care Pain 2013; 13(2):59-62.



