Obstetric Anaesthesia
Pontos-chave
- A recuperação sanguínea intraoperatória (RIS) é provavelmente custo-efetiva para mulheres grávidas com fatores de risco para hemorragia pós-parto.
- A RIS não aumenta o risco de embolia amniótica, infecção ou coagulopatia.
- A RIS é aceita por algumas Testemunhas de Jeová.
- Em mulheres Rhesus-negativas, a dose necessária de imunoglobulina anti-D deve ser determinada com o teste de Kleihauer-Betke e administrada dentro de 72 horas.
Introdução
A hemorragia obstétrica é uma causa importante de morbimortalidade materna no mundo (1). A incidência e a gravidade de hemorragia pós-parto (HPP) estão aumentando: a taxa de HPP no Canadá subiu de 5,1% para 6,2% (um aumento de 22%) entre 2003 e 2010. No mesmo período, a incidência de HPP com necessidade de transfusão sanguínea subiu de 37 a 50,4 a cada 10.000 partos (um aumento de 37%) (1,2).
A recuperação sanguínea intraoperatória (RIS) oferece uma alternativa ou complemento à transfusão alogênica (proveniente de doador) em casos de hemorragia obstétrica maciça e é recomendada nas diretrizes da Associação de Anestesistas da Grã-Bretanha e Irlanda (AABGI), da Associação dos Anestesistas Obstétricos (OAA) e do Instituto Nacional de Saúde e Excelência Clínica (NICE) do Reino Unido (3,4). O ensaio randomizado e controlado do grupo SALVO constatou que o uso rotineiro de RIS durante o parto cesariano não alterou significativamente a taxa de transfusão de sangue no pós-operatório, e a recuperação clínica foi semelhante (5). Porém, em estudos em que em que houve maior recuperação de sangue pela RIS (360 mL vs. 260 mL), apesar da amostra pequena e não-randomizada, a taxa pós-operatória de hemoglobina foi maior e a permanência hospitalar foi menor (5,6). Isso sugere que a RIS pode ser mais benéfica em mulheres com fatores de risco para HPP durante o parto cesariano. Em obstetrícia, a RIS mostrou ser segura, benéfica e custo-efetiva (5,7).
O presente tutorial aborda as indicações, contraindicações, vantagens, desvantagens, riscos e fundamentos da RIS em obstetrícia.
Indicações para a recuperação sanguínea intraoperatória
As indicações para RIS podem ser liberais ou restritivas, mas devem incluir mulheres com risco de HPP durante o parto cesariano. A AAGBI, o Colégio Real de Obstetras e Ginecologistas e a NICE definem isso como uma perda sanguínea estimada (PSE) acima de 1.000 mL (3,4). A RIS é mais custo-efetiva quando há grande probabilidade de transfusão de hemácias, p.ex. uma cesariana de repetição no contexto de uma placenta prévia diagnosticada, anemia pré-operatória grave ou implantação anormal da placenta diagnosticada (8). Mulheres com PSE abaixo de 1.000 mL podem também se beneficiar com RIS, porém em grau menor (5,6). A Tabela 1 mostra exemplos de quando se deve considerar usar RIS, mas o uso depende de protocolos e recursos locais. A gravidade da HPP pode ser difícil de prever, mas o benefício potencial da RIS é proporcional ao número de fatores de risco.
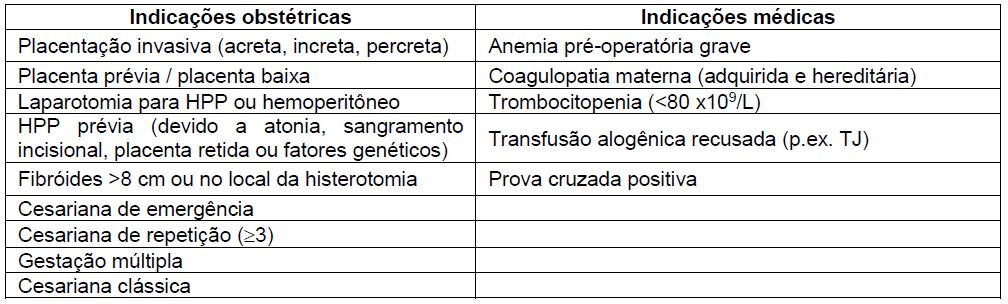
Tabela 1: Indicações obstétricas e médicas para recuperação intraoperatória de sangue durante o parto cesariano. HPP=hemorragia pós-parto; TJ=Testemunhas de Jeová.
Contraindicações para a recuperação sanguínea intraoperatória
- Contaminantes biológicos
- Fezes (obs: urina e líquido amniótico são seguros)
- Contaminantes médicos
- Agentes hemostáticos (Gelfoam™, Avitene™, Surgicel™, Floseal™ etc.)
- Medicação inapropriada para administração intravenosa
- História de plaquetopenia induzida por heparina (9)
- Malignidade
- Anemia falciforme (AF) homozigótica
A reinfusão de sangue recuperado em pacientes com malignidade oferece um risco teórico de disseminação de células malignas, incluindo neoplasias trofoblásticas gestacionais. A RIS foi usada com segurança em pacientes com malignidade urológica, mas não há informação suficiente sobre a segurança em obstetrícia e com outros tipos de malignidade (10).
A RIS não é recomendada em mulheres com AF homozigótica porque as condições de hipóxia no reservatório coletor podem induzir a lise de até 50% dos eritrócitos coletados (11). Em situações que oferecem risco de vida, a RIS pode ser usada em pacientes heterozigóticos. Se uma paciente com AF precisar de RIS, antes de proceder com a reinfusão deve-se preparar com urgência um esfregaço do sangue coletado e determinar o grau de lise (7,11).
Vantagens e desvantagens da recuperação sanguínea intraoperatória
Vantagens
- Sem risco de reações de transfusão alogênica ou infecções transmitidas pelo sangue
- Evita os efeitos imuno-moduladores da transfusão alogênica e infecções hospitalares associadas (12)
- Disponibilidade imediata de sangue
- Prova cruzada positiva na presença de anticorpos
- É aceita por algumas Testemunhas de Jeová
- É seguro administrar junto com medicação (p.ex. uterotônicos e ácido tranexâmico)
- O sangue recuperado é mais fisiológico que o sangue armazenado (veja Tabela 2 abaixo)
- Os níveis de temperatura, bifosfoglicerato, pH e potássio são mais próximos aos valores maternos (7,13,14).

Tabela 2: Comparação de sangue recuperado com hemácias doadas. RIS=recuperação intraoperatória de sangue. * Uma lavagem adequada deixará apenas vestígios de heparina (<10 unidades) no sangue reinfundido (16).
Desvantagens
- Custo do equipamento de RIS e dos insumos
- Custo do treinamento
- O tempo de montagem pode limitar sua utilidade em partos cesarianos de emergência
- O volume de sangue recuperado pode ser insuficiente, sendo necessário complementar com sangue alogênico.
Os custos podem ser reduzidos se o circuito de recuperação for montado somente quando indicado e se o circuito de reinfusão for usado somente em caso de necessidade.
Riscos da recuperação intraoperatória de sangue
No passado, houve preocupação com o uso da RIS em mulheres grávidas devido ao risco teórico de embolia amniótica. Considerava-se a embolia amniótica um processo embólico das células escamosas fetais, mas hoje é vista como uma reação anafilática a antígenos fetais. O nível de células escamosas fetais é o mesmo no sangue recuperado e no sangue materno normal no momento da separação placentária (13). Não existem casos relatados de embolia amniótica atribuída ao uso de RIS em obstetrícia (5,7,13).
A aloimunização ocorre quando uma mulher Rhesus-negativa cria anticorpos ao antígeno D presente em eritrócitos fetais Rhesus-positivos. Toda mãe é exposta a células fetais durante o parto. A carga de células fetais deve ser quantificada com um teste Kleihauer-Betke para determinar a dose de imunoglobulina anti-D a ser administrada à mãe nas primeiras 72 horas após o parto.
Os demais riscos da RIS são semelhantes aos riscos em outras populações cirúrgicas (10), tal como hipotensão devida ao uso de filtros de depleção de leucócitos e o risco de contaminação bacteriana. A hipotensão associada a filtros de depleção de leucócitos é rara e, acredita-se, é causada pela liberação de citocinas pelos leucócitos filtrados. Há relatos de hipotensão resolvida com a suspensão da reinfusão (13). A contaminação bacteriana pós-lavagem de amostras filtradas e não-filtradas é mínima (14); quando é feita profilaxia com antibióticos não parece haver um aumento na taxa de morbidade infecciosa associada à RIS (15).
O circuito de recuperação de sangue
O circuito de RIS inclui um reservatório coletor, um processador e um catéter de reinfusão (Figura 1). O coletor pode ser montado separadamente do circuito de reinfusão.
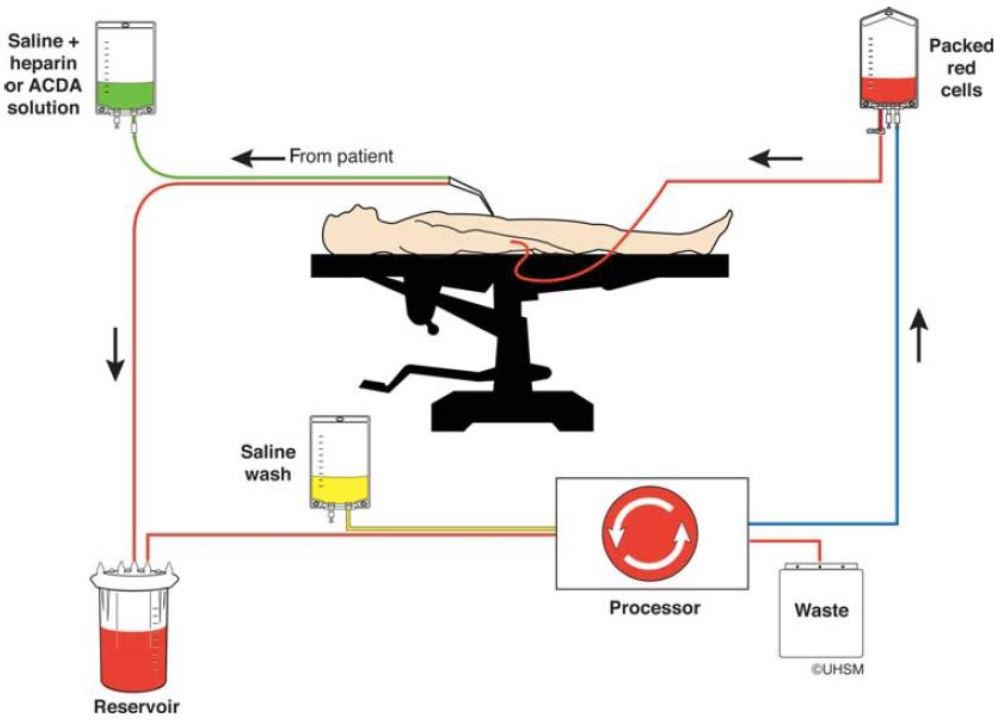
Figura 1: recuperação intraoperatória de sangue (reproduzido com permissão da UK Cell Salvage Action Group). 1) As hemácias são coletadas do campo cirúrgico e/ou de gases com sangue. 2) O sangue é heparinizado, filtrado e lavado com soro antes de ser transferido para o reservatório. 3) Se o volume coletado for o suficiente, o sangue é processado por centrifugação diferencial, suspenso em soro, e reinfundido.
O sangue é coletado no campo cirúrgico através de um sistema de sucção com diâmetro grande e baixa pressão para minimizar danos às células. Pode-se usar uma segunda sucção antes da separação placentária para reduzir a contaminação por líquido amniótico e mecônio. Gases cirúrgicas ensanguentadas podem ser lavadas cuidadosamente com soro isotônico em um recipiente esterilizado, seguido pelo processamento do líquido para um maior rendimento de hemácias. O sangue recuperado deve ser anticoagulado durante a coleta, usualmente com soro heparinizado (16).
A decisão de reinfundir o sangue é baseada na PSE, na hemoglobina pré-operatória e no quadro clínico. O volume de sangue mínimo para iniciar o processamento e reinfusão costuma ser 500 mL, mas depende do equipamento usado. A reinfusão deve ser feita até 4 horas após a coleta.
Caso decida proceder com a reinfusão, o sangue colhido deve ser processado por centrifugação diferencial. A separação é baseada na massa das partículas: são retidos os eritrócitos mais pesados, e são eliminados o plasma, os fatores de coagulação ativados, os complementos e as plaquetas. O sangue é então lavado, transferido para uma bolsa de reinfusão, e administrado à paciente por via intravenosa (16).
A maioria dos equipamentos de RIS usa um filtro padrão de 170-200 micrômetros. Também existem filtros de microagregados (40 micrômetros) e filtros de depleção de leucócitos. Os filtros são montados entre a bolsa de reinfusão e o paciente. O filtro de depleção de leucócitos liga material celular contendo DNA a um filtro de polietileno para melhorar a remoção de contaminantes bacterianos, malignos ou amnióticos. Teoricamente, os filtros de depleção de leucócitos diminuem a contaminação do sangue recuperado (ainda faltam ensaios clínicos), mas já foram associados a taxas mais altas de eventos adversos (5).
Resumo
A RIS é uma ferramenta segura e eficiente de manejo de perda intraoperatória significativa de sangue durante o parto cesariano. O seu uso é mais custo-efetivo e benéfico em mulheres grávidas com fatores de risco para HPP. O benefício não foi comprovado em mulheres com perda de sangue menor que 1.000 mL. Não há relatos de eventos adversos sérios relacionados ao uso da RIS em mulheres grávidas. A RIS evita os riscos da transfusão de sangue proveniente de doador e ajuda a preservar os estoques de sangue doado.
Referências e leitura adicional
- Knight M, Callaghan WM, Berg C et al. Trends in postpartum hemorrhage in high resource countries: a review and recommendations from the International Postpartum Hemorrhage Collaborative Group. BMC Pregnancy Childbirth 2009;9:55.
- Mehrabadi A, Liu S, Bartholomew S et al. Temporal Trends in Postpartum Hemorrhage and Severe Postpartum Hemorrhage in Canada From 2003 to 2010. J Obstet Gynaecol Can. 2014;36:21-33.
- The Association of Anaesthetists of Great Britain and Ireland, Obstetric Anaesthetists’ Association. Guideline for Obstetric Anaesthetic Services 2013. https://www.aagbi.org/sites/default/files/obstetric_anaesthetic_services_2013.pdf (accessed on 06/12/2017)
- National Institute for Health & Care Excellence. Guideline IPG144: Intraoperative blood cell salvage in obstetrics. http://www.nice.org.uk/guidance/ipg144 (accessed 26/11/2017)
- Khan, K, Moore P, Wilson M, et al. Cell Salvage and donor blood transfusion during caesarean section: A pragmatic, multicenter randomized controlled trail (SALVO). PLoS Med 14(12):e1002471. https://doi.org/10.1371/journal.pmed.1002471
- Rainaldi M, Tazzari P, Scagliarini G et al. Blood salvage during caesarean section. Br J Anaesth. 1998;80:195–8.
- Corfe J. Joint guideline on the management of intraoperative cell salvage in obstetrics. 2017. Norfolk and Norwich University Hospitals, Norwich, England. http://www.nnuh.nhs.uk/publication/download/cell-salvage-in-obstetrics-jcg0073-v2/ (accessed 10/11/2017).
- Albright C, Rouse D, Werner E. Cost savings of red cell salvage during caesarean delivery. Obstet Gynecol 2014;124:690-696.
- UK Cell Salvage Action Group. Technical factsheets and frequently asked questions (FAQ). https://www.transfusionguidelines.org/transfusion-practice/uk-cell-salvage-action-group/technical-factsheets-and-frequently-asked-questions-faq (accessed 10/11/2017)
- Kuppurao L, Wee M. Perioperative cell salvage. Cont Edu in Anaesth Crit Care Pain 2010;10:104-108.
- Brajtbord D, Johnson D, Ramsay M et al. Use of the cell saver in patients with sickle cell trait. Anesth 1989;70:878-879.
- Taylor RW, Manganaro L, O’Brien J et al. Impact of allogenic packed red blood cell transfusions on nosocomial infection rates in the critically ill patient. Crit Care Med. 2002;30:2249-2254.
- Goucher H, Wong C, Patel S et al. Cell salvage in obstetrics. Anesth Analg. 2015;121:465-468.
- Thomas D. Cell salvage in trauma. Trans Alt Trans Med. 2005;6:31-36.
- Allam J, Cox M, Yentis SM. Cell Salvage in obstetrics. Int J Obstet Anesth. 2008;17:37-45.
- Water J. Intraoperative blood recovery. 2013. ASAIO J. 2013;59:11-17.



